Clear Sky Science · fr
MEKK3 relie la communication intestin-cerveau et la pathogénie des malformations cavernomateuses cérébrales
Pourquoi l’intestin pourrait compter pour les hémorragies cérébrales
Les malformations cavernomateuses cérébrales sont des amas de vaisseaux sanguins fragiles dans le cerveau qui peuvent fuiter ou saigner, provoquant crises d’épilepsie, maux de tête et AVC. Cet article de synthèse explore un retournement surprenant : de minuscules microbes dans nos intestins et les signaux chimiques qu’ils émettent pourraient influencer la formation ou l’aggravation de ces vaisseaux anormaux. En suivant la chaîne du microbiote intestinal au sang puis au cerveau, les auteurs mettent en lumière un point de relais signalétique appelé MEKK3, présent dans les cellules vasculaires, comme un nœud clé susceptible de transformer des perturbations intestinales en lésions cérébrales dangereuses.
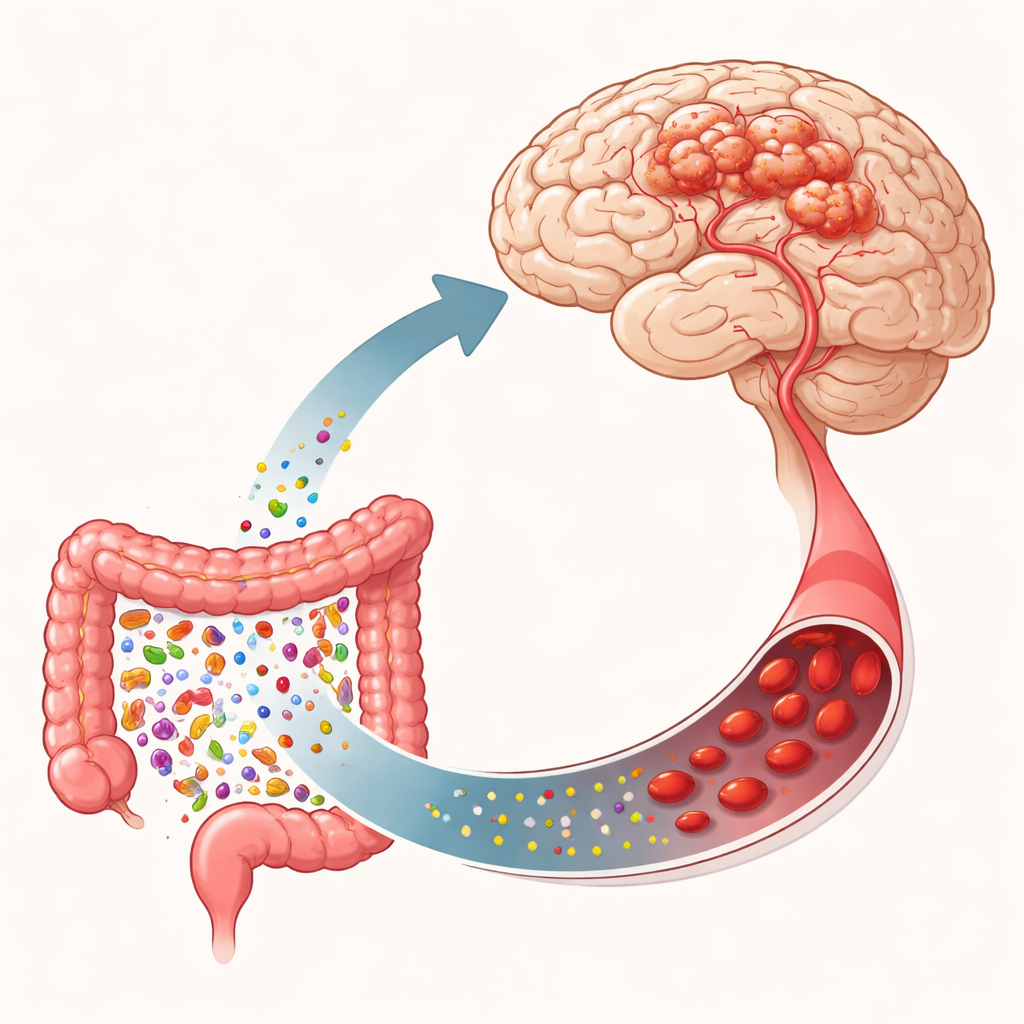
Faiblesses cachées dans les vaisseaux cérébraux
Les malformations cavernomateuses cérébrales (MCC) touchent environ une personne sur quelques centaines, bien que beaucoup l’ignorent. Ces malformations sont constituées de vaisseaux aux parois fines, en forme de poches, susceptibles de se rompre. Certains cas sont sporadiques, apparaissant comme des lésions isolées, tandis que d’autres sont familiaux et comportent de multiples lésions. Les formes héréditaires résultent généralement de modifications délétères dans l’un des trois gènes (souvent appelés CCM1, CCM2 et CCM3) qui contribuent à maintenir l’endothélium vasculaire étroit et stable. Lorsque ces gènes défaillent, les jonctions entre les cellules des vaisseaux se relâchent, les vaisseaux se dilatent de manière anormale et des enchevêtrements de type caverne peuvent se former. Des mutations supplémentaires dans des voies de croissance, telles que PIK3CA, peuvent pousser ces cellules fragiles à proliférer et à se remodeler, rendant les lésions plus volumineuses et agressives.
Un central téléphonique cellulaire nommé MEKK3
Au centre de cette histoire se trouve MEKK3, une protéine présente dans les cellules vasculaires qui joue le rôle d’un central pour de nombreux signaux entrants. Des études génétiques montrent que des altérations spécifiques du gène MEKK3 (MAP3K3) suffisent à déclencher des malformations cavernomateuses dans des modèles animaux, définissant un sous-groupe distinct de patients. L’activité de MEKK3 contrôle d’autres facteurs, KLF2 et KLF4, qui influencent à leur tour l’adhérence cellulaire, la prolifération et la perméabilité de la paroi vasculaire. Lorsque MEKK3 est hyperactif, les jonctions entre cellules endothéliales s’affaiblissent, la barrière qui sépare normalement le sang du tissu cérébral devient poreuse, et les malformations ont davantage de chances de croître et de saigner. MEKK3 n’agit pas isolément ; il croise des signaux de croissance comme VEGF et PI3K ainsi que des voies sensibles au flux sanguin et à l’inflammation.
Comment l’intestin parle au cerveau
L’axe intestin–cerveau est le réseau de communication qui relie l’intestin au système nerveux via des nerfs, des cellules immunitaires, des hormones et des produits microbiels. Cette revue met l’accent sur une voie en particulier : le passage de produits microbiens de l’intestin dans la circulation sanguine, puis vers les vaisseaux du cerveau. Lorsque la communauté intestinale se déséquilibre, certaines bactéries libèrent de la lipopolysaccharide (LPS), composant de leur membrane externe, dans la circulation. Le LPS peut fragiliser la barrière intestinale, augmentant encore sa propre pénétration dans le sang. Une fois dans les vaisseaux cérébraux, le LPS active un détecteur de surface appelé TLR4 sur les cellules endothéliales, ce qui déclenche ensuite MEKK3 et des cascades inflammatoires en aval. Le résultat est une fuite vasculaire accrue, un recrutement de cellules immunitaires et la progression des lésions MCC. D’autres molécules d’origine intestinale, comme les acides gras à courte chaîne, le triméthylamine N‑oxyde (TMAO) et des composés liés à l’indole, peuvent soit soutenir la santé des barrières soit alimenter l’inflammation, selon leur équilibre.
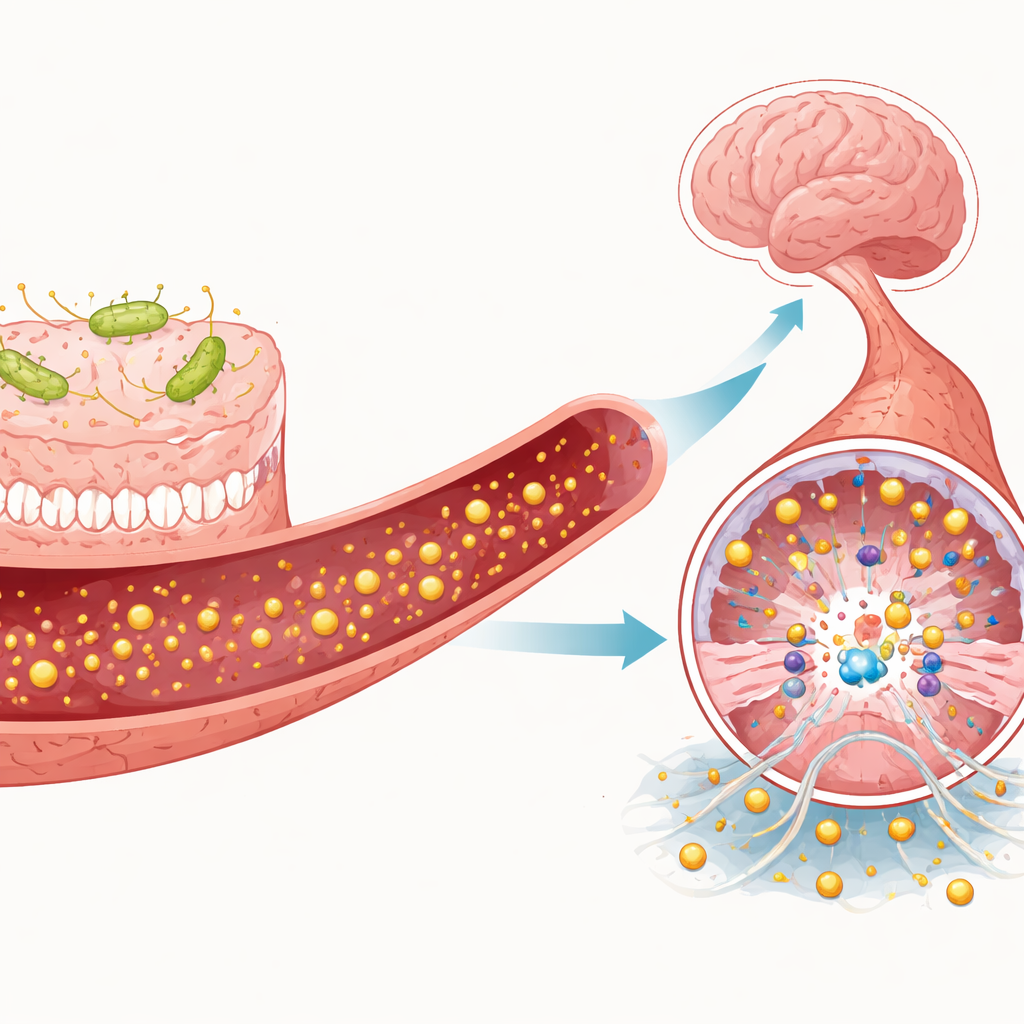
Signaux utiles et nocifs des microbes et des cellules immunitaires
L’article détaille comment des métabolites intestinaux individuels et des cellules immunitaires peuvent orienter la signalisation MEKK3 vers la détérioration ou la protection. Les acides gras à courte chaîne comme le butyrate, produits lorsque les microbes digèrent les fibres alimentaires, semblent renforcer la barrière hémato‑encéphalique et peuvent indirectement atténuer l’activité de TLR4 et de MEKK3. En revanche, le TMAO et certains dérivés de l’indole, tels que le sulfate d’indoxyle, favorisent l’inflammation, le stress oxydatif et un renforcement du signal TLR4, ce qui peut augmenter l’activation de MEKK3. Les cellules immunitaires jouent également un rôle. Les neutrophiles peuvent libérer des filets extracellulaires collants qui stimulent davantage TLR4 sur les cellules vasculaires, tandis que les macrophages pro‑inflammatoires et les cellules T auxiliaires renforcent les voies liées à MEKK3 ; leurs homologues anti‑inflammatoires peuvent les freiner. Ensemble, ces signaux créent un conflit dynamique déterminant si les vaisseaux cérébraux restent stables ou se détériorent en lésions cavernomateuses.
Nouvel horizon pour des traitements plus doux
Les traitements actuels des malformations cavernomateuses cérébrales sont limités, reposant souvent sur la chirurgie ou la radiothérapie ciblée pour les lésions à haut risque. Les auteurs soutiennent que comprendre comment les microbes intestinaux et leurs produits alimentent une signalisation centrée sur MEKK3 ouvre des possibilités nouvelles et moins invasives. En principe, de futures thérapies pourraient combiner des stratégies visant le microbiome — telles que l’alimentation, les probiotiques ou la réduction ciblée des métabolites nocifs — avec des médicaments qui atténuent l’activité de TLR4 ou de MEKK3 dans les vaisseaux cérébraux. Pour un lecteur non spécialiste, la conclusion est que des perturbations intestinales peuvent avoir des effets étendus sur la santé des vaisseaux sanguins du cerveau, et qu’un unique « hub » cellulaire comme MEKK3 pourrait être la clé pour réduire cette conversation nuisible et prévenir des hémorragies cérébrales dangereuses.
Citation: Cheng, P., Han, H., Huang, Y. et al. MEKK3 bridges gut-brain communication and cerebral cavernous malformation pathogenesis. Cell Death Discov. 12, 197 (2026). https://doi.org/10.1038/s41420-026-03062-6
Mots-clés: malformation cavernomateuse cérébrale, axe intestin-cerveau, signalisation MEKK3, métabolites du microbiote intestinal, inflammation neurovasculaire