Clear Sky Science · nl
MEKK3 overbrugt darm-hersencommunicatie en de pathogenese van cerebrale cavernomateuze malformaties
Waarom de darm van belang kan zijn voor hersenbloedingen
Cerebrale cavernomateuze malformaties zijn klonten van kwetsbare bloedvaten in de hersenen die kunnen lekken of bloeden, wat aanvallen, hoofdpijn en beroertes kan veroorzaken. Dit overzichtsartikel onderzoekt een verrassende wending: kleine microben in onze darmen en de chemische signalen die ze afgeven, kunnen beïnvloeden of deze abnormale vaten ontstaan of verergeren. Door de keten van darmbacteriën naar bloed naar hersenen te volgen, belichten de auteurs een signaleringsknooppunt genaamd MEKK3 binnen bloedvatcellen als een belangrijke relaispost die darmstoornissen kan omzetten in gevaarlijke hersenlaesies.
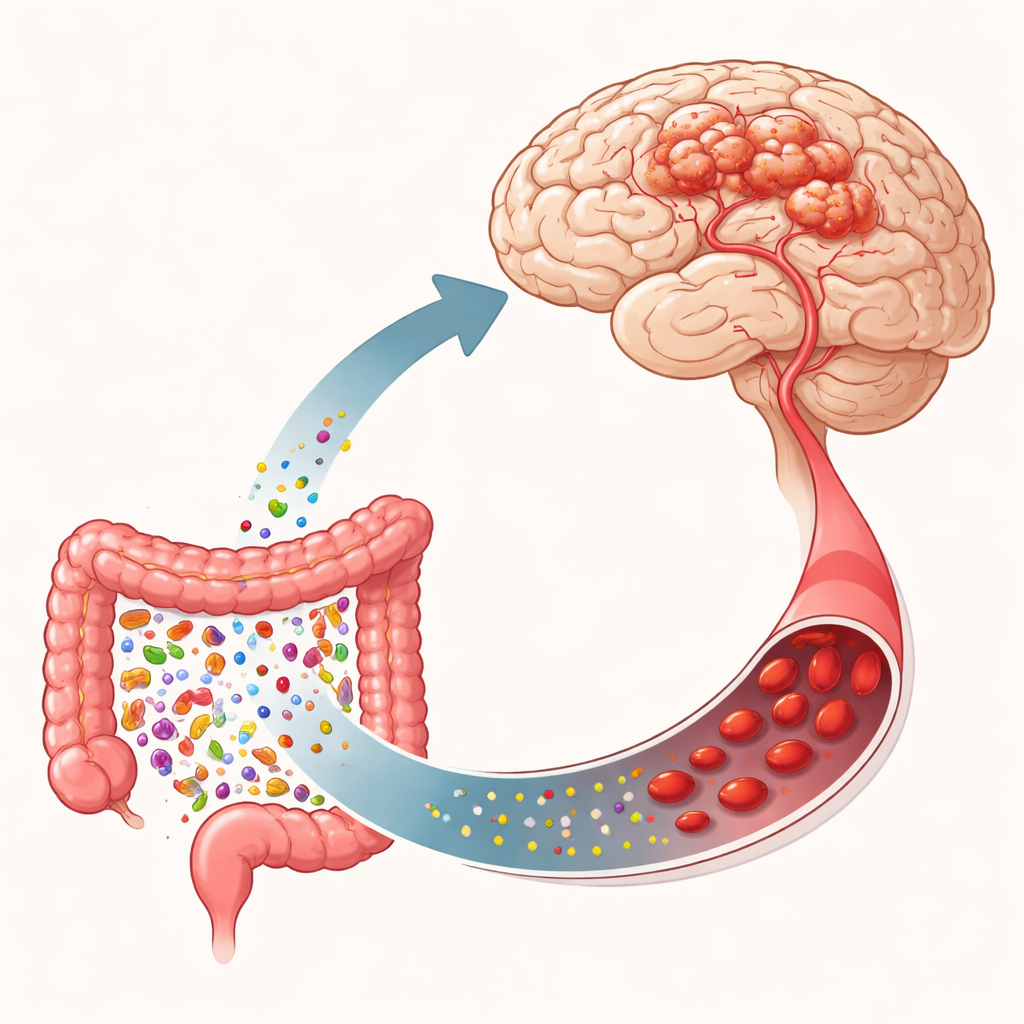
Verborgen zwakke plekken in hersenbloedvaten
Cerebrale cavernomateuze malformaties (CCM) treffen ongeveer één op een paar honderd mensen, hoewel velen nooit weten dat ze ze hebben. Deze malformaties bestaan uit dunwandige, ballonachtige vaten die kunnen scheuren. Sommige gevallen zijn sporadisch en verschijnen als een enkele laesie, terwijl andere in families voorkomen en meerdere laesies omvatten. Geërfde vormen ontstaan meestal door schadelijke veranderingen in een van drie genen (vaak CCM1, CCM2 en CCM3 genoemd) die helpen de bekleding van bloedvaten strak en stabiel te houden. Wanneer deze genen falen, verslappen de verbindingen tussen vaatcellen, verwijden de vaten zich abnormaal en kunnen cavernachtige kluwens ontstaan. Aanvullende mutaties in groeipaden, zoals PIK3CA, kunnen deze kwetsbare cellen stimuleren te delen en te herbouwen, waardoor laesies groter en agressiever worden.
Een cellulair schakelpaneel genaamd MEKK3
Centraal in dit verhaal staat MEKK3, een eiwit in bloedvatcellen dat fungeert als een schakelpaneel voor vele binnenkomende signalen. Genetische studies tonen aan dat specifieke veranderingen in het MEKK3-gen (MAP3K3) voldoende zijn om cavernomateuze malformaties te veroorzaken in diermodellen, waarmee een duidelijke patiëntengroep wordt gedefinieerd. MEKK3-activiteit regelt andere factoren, KLF2 en KLF4, die op hun beurt beïnvloeden hoe strak cellen aan elkaar hechten, hoeveel ze prolifereren en hoe lek de vaatwand wordt. Wanneer MEKK3 overactief is, verzwakken de verbindingen tussen endotheelcellen, wordt de barrière die bloed van hersenweefsel scheidt poreus, en is de kans groter dat malformaties groeien en bloeden. MEKK3 werkt niet geïsoleerd; het kruist groeisignalen zoals VEGF en PI3K en paden die reageren op fysieke bloedstroom en ontsteking.
Hoe de darm met de hersenen praat
De darm-hersen-as is het communicatienetwerk dat de darm verbindt met het zenuwstelsel via zenuwen, immuuncellen, hormonen en microbiële chemicaliën. Dit overzicht legt de nadruk op één route in het bijzonder: het transport van microbiële producten uit de darm naar de bloedbaan en vervolgens naar de bloedvaten van de hersenen. Wanneer de darmgemeenschap uit balans raakt, scheiden bepaalde bacteriën lipopolysaccharide (LPS) af, een component van hun buitenmembraan, in de circulatie. LPS kan de darmbarriere verslappen en zo zijn eigen passage naar het bloed verder vergroten. Eenmaal in de vaten van de hersenen activeert LPS een oppervlaktesensor genaamd TLR4 op endotheelcellen, wat vervolgens MEKK3 en daaropvolgende inflammatoire cascade activeert. Het resultaat is meer vaatlekkage, aantrekken van immuuncellen en voortgang van CCM-laesies. Andere darmafgeleide moleculen, zoals korteketenvetzuren, trimethylamine N-oxide (TMAO) en indool-gerelateerde verbindingen, kunnen afhankelijk van hun balans de barrière ondersteunen of ontsteking aanwakkeren.
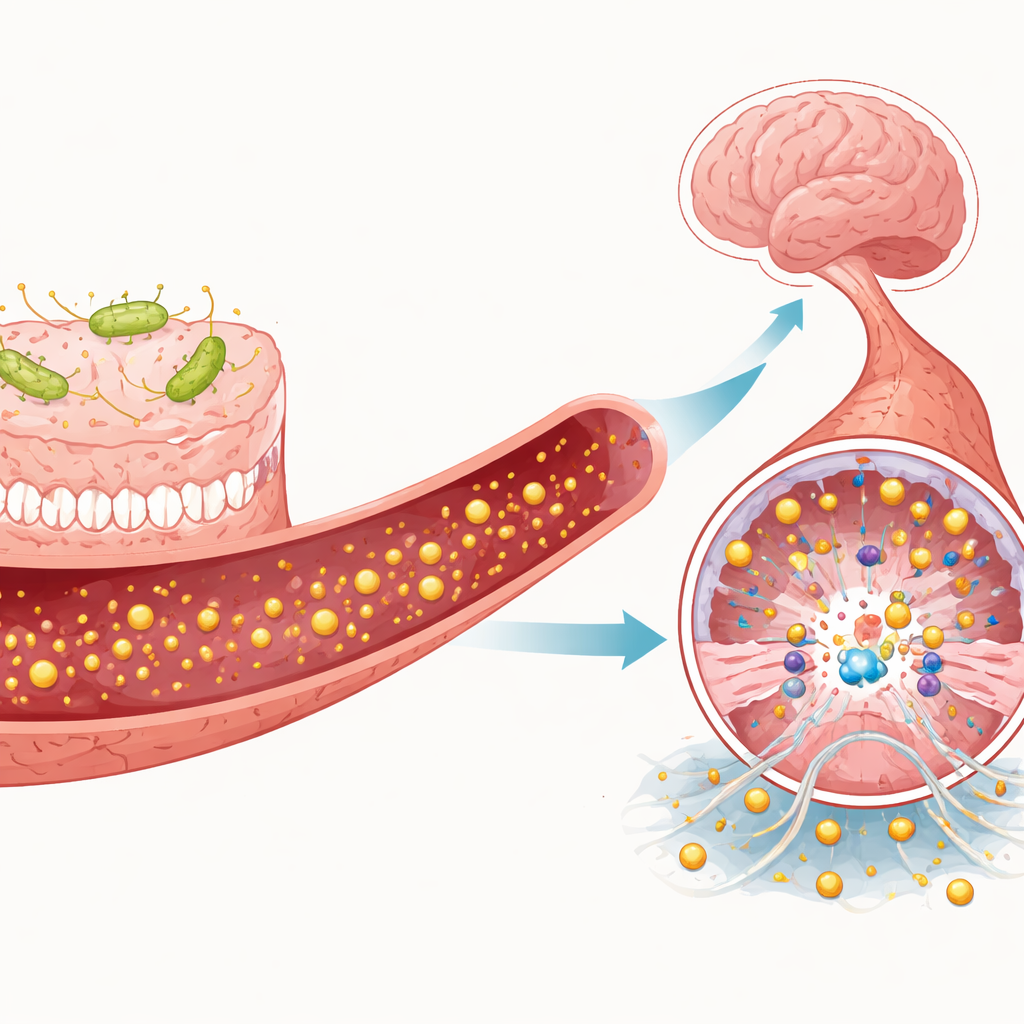
Behulpzame en schadelijke signalen van microben en immuuncellen
Het artikel beschrijft hoe individuele darmmetabolieten en immuuncellen MEKK3-signaleringsroutes naar schade of bescherming kunnen duwen. Korteketenvetzuren zoals butyraat, geproduceerd wanneer microben voedingsvezel verteren, lijken de bloed-hersenbarriere te versterken en kunnen indirect TLR4- en MEKK3-activiteit dempen. Daarentegen bevorderen TMAO en bepaalde indoolderivaten, zoals indoxylsulfaat, ontsteking, oxidatieve stress en sterkere TLR4-signalisering, wat MEKK3-activatie kan verhogen. Immuuncellen spelen ook een rol. Neutrofielen kunnen kleverige extracellulaire webs loslaten die TLR4 op vatcellen verder stimuleren, terwijl pro-inflammatoire macrofagen en T-helpercellen MEKK3-gekoppelde paden versterken; anti-inflammatoire tegenhangers kunnen deze remmen. Samen vormen deze signalen een dynamische touwtrekwedstrijd over de vraag of hersenvaten stabiel blijven of verslechteren tot cavernachtige laesies.
Nieuwe wegen naar mildere behandelingen
Huidige behandelingen voor cerebrale cavernomateuze malformaties zijn beperkt en berusten vaak op chirurgie of gerichte bestraling voor hoogrisicolaesies. De auteurs betogen dat inzicht in hoe darmmicroben en hun producten in MEKK3-centrische signalering vloeien, nieuwe, minder invasieve mogelijkheden opent. In principe zouden toekomstige therapieën microbiome-gerichte strategieën kunnen combineren — zoals dieet, probiotica of gerichte vermindering van schadelijke metabolieten — met geneesmiddelen die TLR4- of MEKK3-activiteit in hersenbloedvaten temperen. De kernboodschap voor een niet-specialistische lezer is dat problemen in de darm verstrekkende gevolgen kunnen hebben voor de gezondheid van hersenbloedvaten, en dat een enkel cellulair “knooppunt” zoals MEKK3 de sleutel zou kunnen zijn om dit schadelijke gesprek te dempen en gevaarlijke hersenbloedingen te voorkomen.
Bronvermelding: Cheng, P., Han, H., Huang, Y. et al. MEKK3 bridges gut-brain communication and cerebral cavernous malformation pathogenesis. Cell Death Discov. 12, 197 (2026). https://doi.org/10.1038/s41420-026-03062-6
Trefwoorden: cerebrale cavernomateuze malformatie, darm-hersen-as, MEKK3-signaleringspad, metabolieten van de darmmicrobiota, neurovasculaire ontsteking