Clear Sky Science · zh
核孔蛋白TPR将MAPK信号与促丝裂原诱导的转录程序整合
细胞如何决定何时生长
我们的细胞不断接收“前进或停止”的信号,告诉它们何时分裂、休眠或对环境作出反应。这些指令中有许多通过一条著名的蛋白链——MAPK通路——传递,而该通路在癌症中常常过度活跃。这项研究揭示了位于细胞核入口处的一个意想不到的参与者——名为TPR的大型支架蛋白——它有助于微调生长信号如何被转换为瞬时的基因活性爆发。理解这一额外的调控层可能为读取并最终调节患者中与癌症相关的信号提供新途径。
位于细胞核边缘的守门员
每个细胞核表面分布着数千个核孔——大型通道允许分子进出。TPR是一种附着在核孔内侧的长型结构蛋白。人们已知它参与RNA输出和维持基因组稳定性等任务,但其在生长控制中的作用尚不清楚,尽管其表达水平在多种癌症中异常。作者们提出疑问:TPR是否不仅仅是核孔的一个被动组成部分,而是一个能够将进入的生长信号连接到核内深处基因活动变化的响应元件。
在核孔处“倾听”生长信号
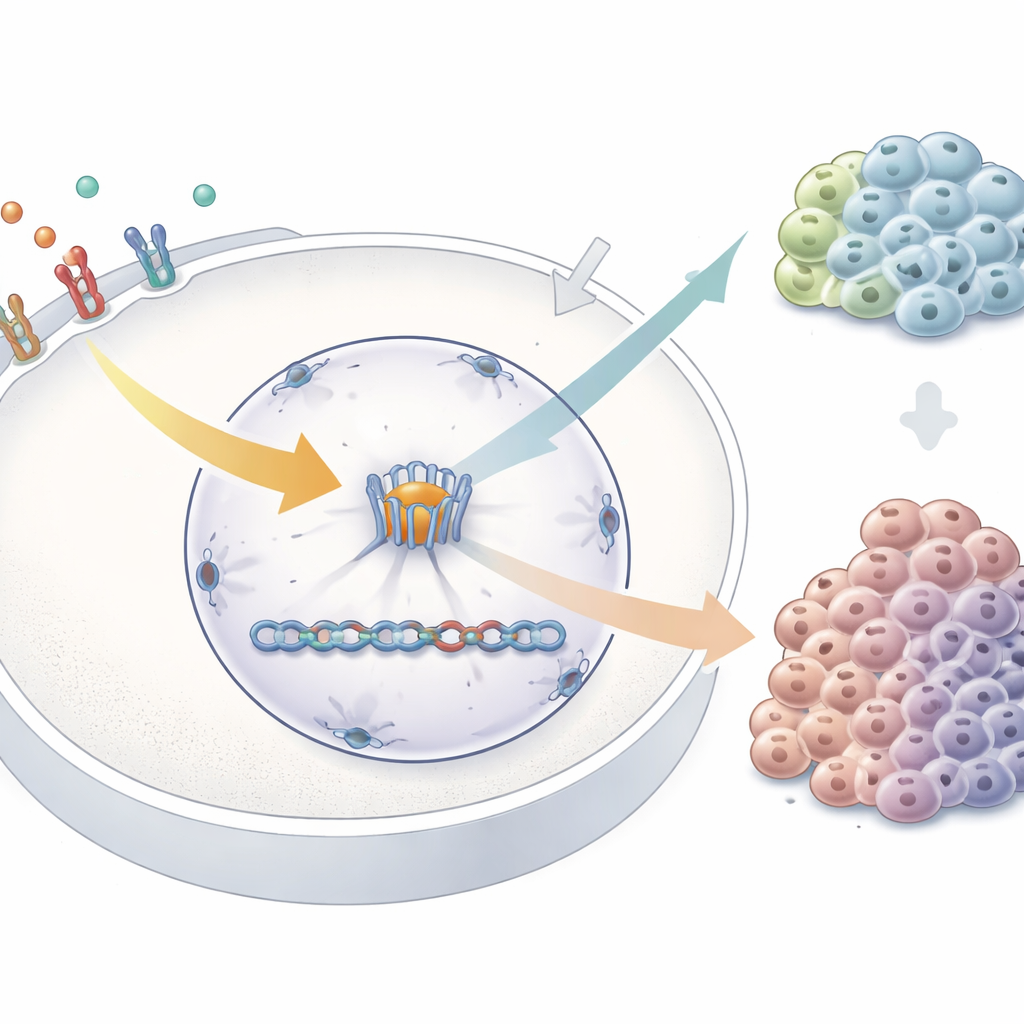
为探讨这一想法,研究者在人体癌细胞中降低了TPR水平,然后用表皮生长因子刺激细胞,这是一种经典的MAPK通路触发物。通过RNA测序,他们比较了在静息状态和刺激后,正常细胞与TPR耗竭细胞的基因活性。结果发现,当TPR缺失时有数百个基因的行为发生变化,其中包括许多与MAPK通路本身相关的基因。有些与促进生长和反馈控制相关的基因在未刺激的细胞中就已改变,而另一些仅在生长信号到来后才发生变化。值得注意的是,一个名为FOS的即刻早期基因——MAPK激活最快的反应者之一——在TPR耗竭时被更强烈地激活,这种超调依赖于活跃的生长因子信号。在功能层面,缺乏TPR的细胞对持续刺激的反应异常,表现为细胞周期进程的模式发生了偏移。
TPR上的化学开关
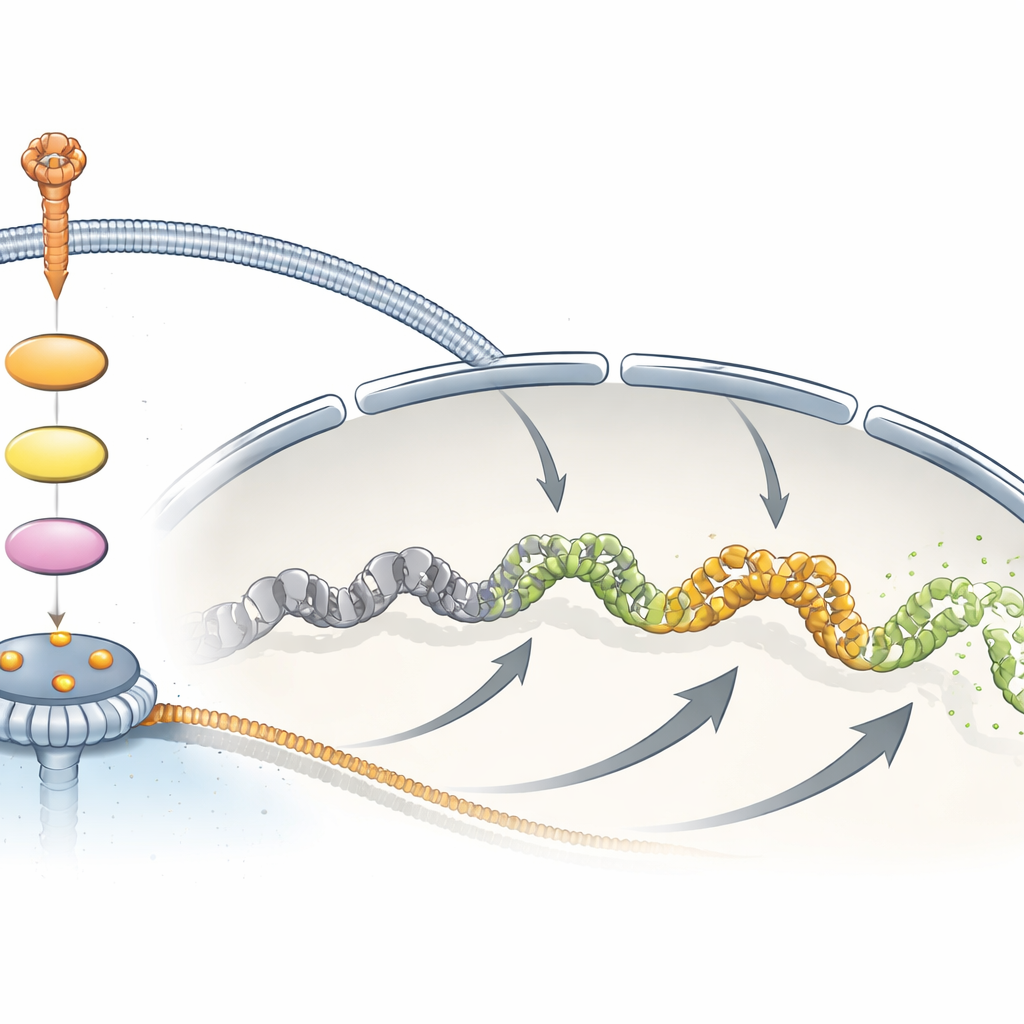
团队随后寻找MAPK信号与TPR之间的物理联系。早期的大规模蛋白调查提示,TPR上的一个特定位点——称为Ser2155的氨基酸——在生长因子处理后会被磷酸化,也就是被化学标记。作者制备了一种高度特异性的抗体,仅识别在该位点被磷酸化的TPR,从而使他们能够随时间和不同体系追踪这一修饰。在多种人类细胞类型中,生长因子刺激迅速而短暂地增加了Ser2155的磷酸化,且其变化与关键MAPK酶ERK的活化密切对应。阻断上游生长因子受体或抑制MEK‑ERK步骤都会明显降低这种磷酸化。共同去除ERK1和ERK2几乎消除了该修饰,而消除TPR本身并不改变ERK活性,这将TPR明确定位在MAPK级联反应的下游,而非作为核心信号成分。
从小鼠到人类肿瘤
为检验这一联系是否在细胞系之外也有意义,研究者构建了仅保留一个功能性Tpr基因拷贝的小鼠;完全丧失在发育过程中致死。在这些小鼠的脾脏——一种免疫细胞通过抗原受体而非生长因子受体激活MAPK通路的组织——整体基因活动模式发生了变化,同样富集了与MAPK相关的基因并抑制了若干对该通路的自然制动。当来自这些小鼠的脾细胞通过T细胞受体刺激时,它们产生的Fos信使RNA比正常动物的细胞更多,反映了人类细胞培养结果。研究团队随后检查了人类肿瘤样本。在大多数浆液性卵巢癌以及一大部分三阴性乳腺癌中,Ser2155位点磷酸化的TPR染色较为常见,尽管乳腺肿瘤在不同病例之间显示更大的可变性,这与其通路激活模式的混杂性一致。
这对癌症与治疗意味着什么
总体而言,这些发现将TPR描绘为一个位于核孔处、可响应MAPK通路化学调节的核因子。TPR并非开关式地开启或关闭该通路,而是帮助塑造随生长或免疫刺激而来的转录爆发的振幅和性质,尤其是对像FOS这样被快速诱导的基因。由于许多癌症依赖持续的MAPK活性,TPR的存在及其磷酸化状态可能作为评估肿瘤中通路参与度的有用读数,其失调也可能促成异常的生长反应。这项工作将我们对核孔的视角从静态的关口扩展为细胞解读促丝裂信号时的积极参与者。
引用: Liu, J., Zheng, Y., Xiong, Y. et al. Nucleoporin TPR integrates MAPK signaling with mitogen-induced transcriptional programs. Cell Death Dis 17, 400 (2026). https://doi.org/10.1038/s41419-026-08760-8
关键词: 核孔, MAPK信号传导, TPR蛋白, 生长因子信号, 癌症转录