Clear Sky Science · ar
البروتين النوكليوبورين TPR يربط إشارات MAPK ببرامج النسخ المحفزة بالعوامل المُنَمية
كيف تقرر الخلايا متى تنمو
تتلقى خلايانا باستمرار إشارات «انطلق أو توقف» تخبرها متى تنقسم ومتى ترتاح أو متى تتفاعل مع بيئتها. تنتقل العديد من هذه الأوامر عبر سلسلة بروتينية معروفة باسم مسار MAPK، الذي يكون نشطًا بشكل مفرط في كثير من السرطانات. تكشف هذه الدراسة عن لاعب غير متوقع عند بوابة نواة الخلية — بروتين هيكلي كبير يُدعى TPR — يساعد على ضبط كيفية ترجمة إشارات النمو إلى دفعات من نشاط الجينات. قد يفتح فهم هذه الطبقة الإضافية من التنظيم سبلًا جديدة لقراءة، وفي نهاية المطاف تعديل، إشارات مرتبطة بالسرطان لدى المرضى.
حارس عند حافة النواة
تحتوي كل نواة خلوية على آلاف من المسامات النووية — قنوات ضخمة تسمح للجزيئات بالتحرك داخل وخارج النواة. يرتبط TPR بالجانب الداخلي لتلك المسامات ويشكل بروتينًا طويلاً هيكليًا. كان معروفًا أنه يساعد في مهام مثل تصدير الحمض النووي الريبي والحفاظ على استقرار الجينوم، لكن دوره في التحكم بالنمو كان غير واضح، مع أن مستوياته تكون غير طبيعية في عدة أنواع من السرطان. تساءل المؤلفون عما إذا كان TPR ليس جزءًا سلبيًا من المسام فحسب، بل عنصرًا متجاوبًا يربط إشارات النمو الواردة بالتغيرات في نشاط الجينات داخل النواة.
الاستماع لإشارات النمو عند المسام النووية
لاختبار هذه الفكرة، خفّض الباحثون مستويات TPR في خلايا سرطانية بشرية ثم حفزوها بعامل النمو البطاني (EGF)، وهو محفز كلاسيكي لسلسلة إشارات MAPK. باستخدام تسلسل الحمض النووي الريبي، قارنوا نشاط الجينات في خلايا طبيعية مقابل خلايا ناقصة TPR، سواء في حالة الراحة أو بعد التحفيز. وجدوا أن مئات الجينات غيّرت سلوكها عند غياب TPR، بما في ذلك الكثير المرتبطة بمسار MAPK نفسه. بعض الجينات المرتبطة بتعزيز النمو والضوابط الراجعة كانت متغيرة بالفعل في الخلايا غير المحفَّزة، بينما تغيرت أخرى فقط بعد وصول إشارة النمو. ولاحظوا أن جينًا فوريًا يُدعى FOS — أحد أسرع المستجيبين لتنشيط MAPK — أُنشط بشكل أقوى عند نقص TPR، وكان هذا الإفراط معتمدًا على وجود إشارات عوامل نمو نشطة. وظيفيًا، استجابت الخلايا الخالية من TPR بشكل غير طبيعي للتحفيز المطوَّل، مظهرة نمطًا مُزاحًا لتقدم دورة الخلية.
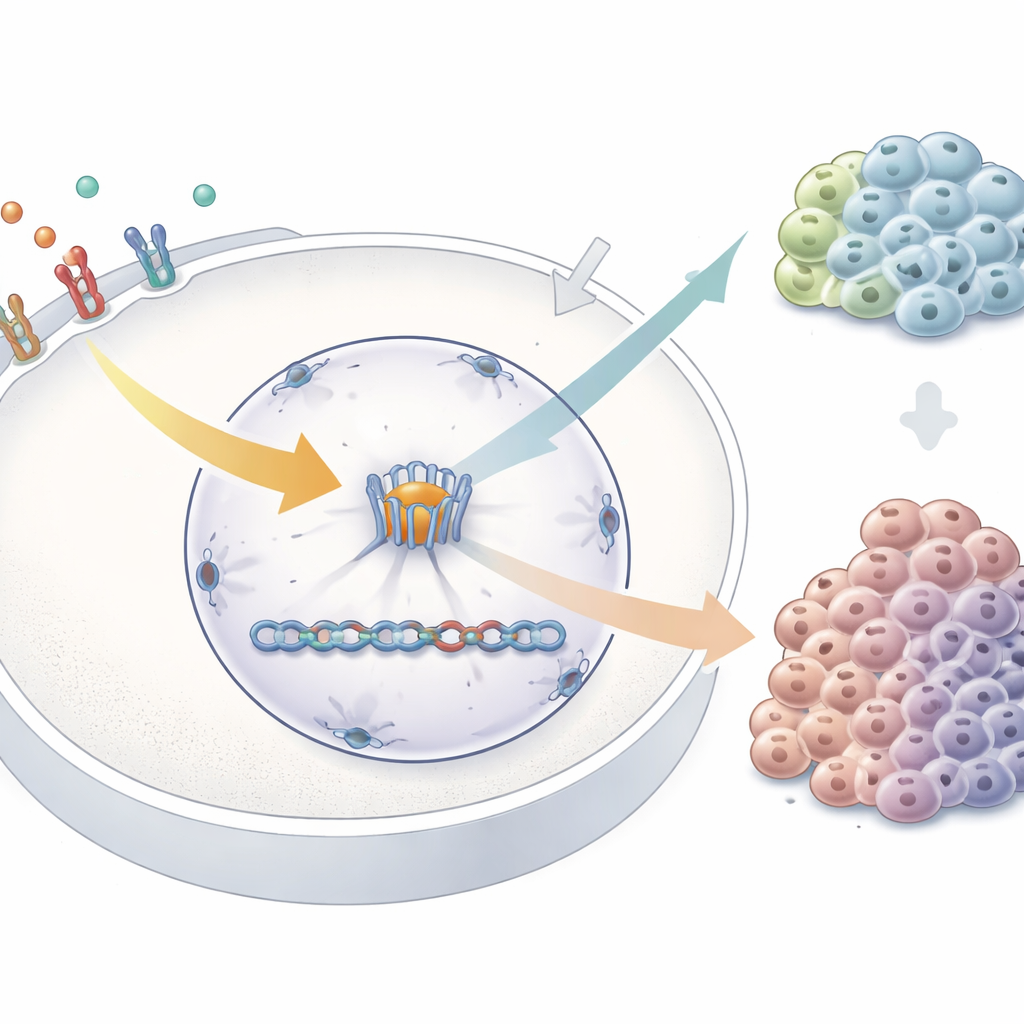
مفتاح كيميائي على TPR
بحث الفريق لاحقًا عن صلة فيزيائية بين إشارات MAPK وTPR. أشارت دراسات بروتينية واسعة النطاق السابقة إلى أن موضعًا معينًا على TPR، حمض أميني يُسمى Ser2155، يتعرض للفوسفرة — أي وسم كيميائي — بعد معالجة بعوامل النمو. صنع المؤلفون جسمًا مضادًا عالي التخصيص يتعرف على TPR فقط عندما يكون هذا الموقع مفوسفَرًا، ما أتاح لهم تتبع هذا التعديل عبر الزمن وفي أنظمة متعددة. في عدة أنواع خلوية بشرية، زادت فسفرة Ser2155 بسرعة وبشكل عابر بعد تحفيز عوامل النمو، متتبعة تنشيط ERK، وهو إنزيم مركزي في مسار MAPK. أدى حجب مستقبل عوامل النمو أو خطوات MEK–ERK في المسار إلى خفض حاد في هذه الفسفرة. إزالة ERK1 وERK2 معًا قضت عليها تقريبًا، بينما لم يغيّر التخلص من TPR نشاط ERK، ما يضع TPR بوضوح في موقع متأثر بتدفق الشلال MAPK وليس كمكوّن أساسي في التوصيل الإشاري ذاته.
من الفئران إلى أورام البشر
لاختبار ما إذا كانت هذه الصلة مهمة خارج خطوط الخلايا، أنتج الباحثون فئرانًا تملك نسخة واحدة فقط عاملة من جين Tpr؛ لأن الفقد الكامل كان مميتًا أثناء التطور. في طحال هذه الفئران — نسيج تنشط فيه الخلايا المناعية مسار MAPK عبر مستقبلات المستضد بدلاً من مستقبل عوامل النمو — تغيّر النمط العام لنشاط الجينات، مع إثراء مرة أخرى للجينات المرتبطة بـMAPK وكبت عدة عوامل كابحة طبيعية للمسار. عندما حُفزت الخلايا الطحالية من هذه الفئران عبر مستقبلات الخلايا التائية، أنتجت كمية أكبر من حمض Fos الرسول مقارنة بخلايا الحيوانات الطبيعية، معاكسةً نتائج مزرعة الخلايا البشرية. ثم فحص الفريق عينات أورام بشرية. في معظم سرطانات المبيض المصحوبة بسائل (serous)، وفي جزء كبير من سرطانات الثدي الثلاثية السالبة، كان وجود TPR المفوسفَر على Ser2155 شائعًا، رغم أن أورام الثدي أظهرت تباينًا أكبر من حالة إلى أخرى، بما يتوافق مع أنماط تفعيل المسار المتباينة فيها.
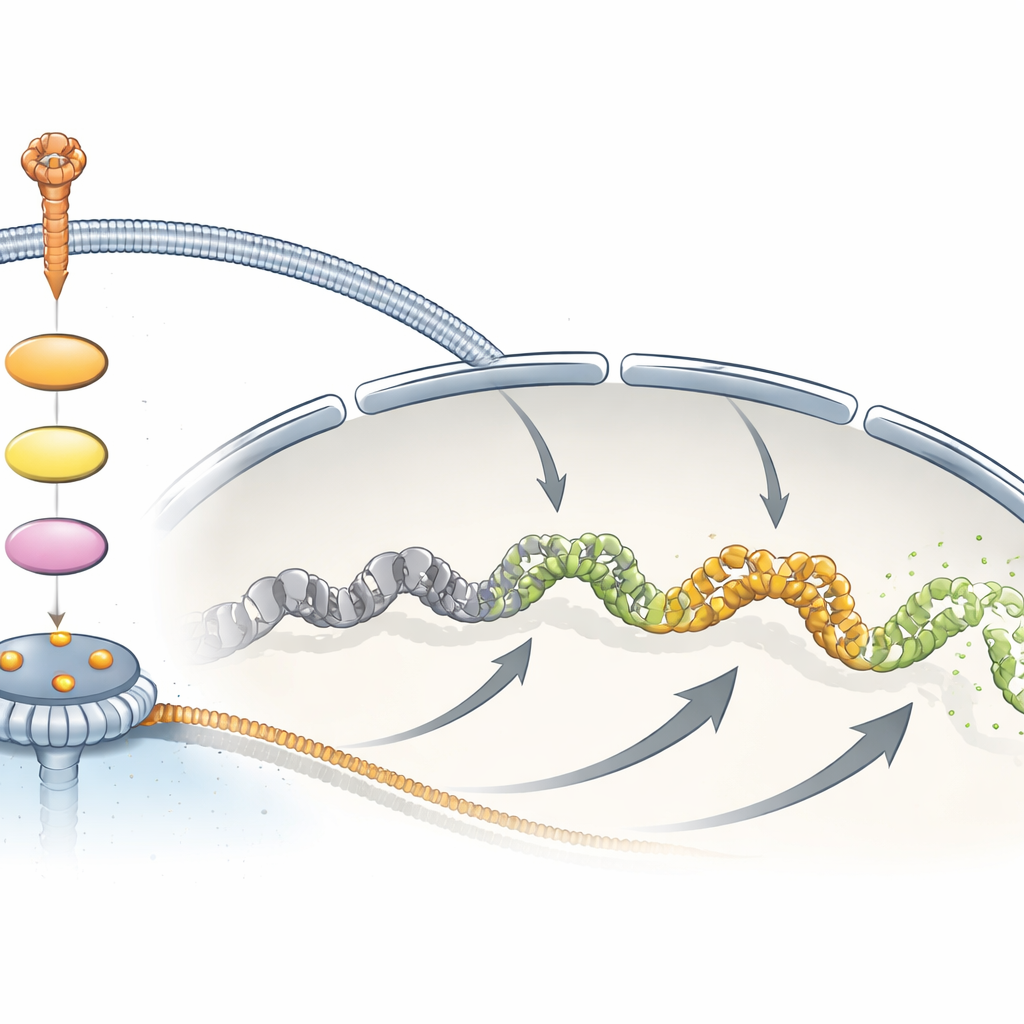
لماذا يهم هذا بالنسبة للسرطان والعلاج
تُصوِّر النتائج مجتمعةً TPR كعامل نووي متجاوب يجلس عند المسام النووية ويتوافق كيميائيًا مع مسار MAPK. بدلاً من تشغيل المسار أو إيقافه، يساعد TPR في تشكيل سعة وجودة انفجار النسخ الذي يتبع التحفيز بالنمو أو بالمناعة، خصوصًا للجينات المستحثة بسرعة مثل FOS. وبما أن العديد من السرطانات تعتمد على نشاط MAPK المستمر، فقد يكون وجود TPR وحالة فسفره مؤشرًا مفيدًا على انخراط المسار في الأورام، وقد يساهم اختلال تنظيمه في استجابات نمو مشوّهة. توسع هذه الدراسة رؤيتنا للمسامات النووية من بوابات ثابتة إلى مشاركين فاعلين في كيفية تفسير الخلايا للإشارات الميتوجينية.
الاستشهاد: Liu, J., Zheng, Y., Xiong, Y. et al. Nucleoporin TPR integrates MAPK signaling with mitogen-induced transcriptional programs. Cell Death Dis 17, 400 (2026). https://doi.org/10.1038/s41419-026-08760-8
الكلمات المفتاحية: المسامات النووية, إشارات MAPK, بروتين TPR, إشارات عوامل النمو, نسخ السرطان