Clear Sky Science · ru
Нуклеопориновый белок TPR интегрирует сигналы MAPK с митоген‑индуцированными транскрипционными программами
Как клетки решают, когда расти
Наши клетки постоянно получают сигналы «иди‑или‑стоп», указывающие, когда делиться, отдыхать или реагировать на окружающую среду. Многие из этих команд проходят через хорошо известную цепь белков, называемую MAPK‑путём, который часто гиперактивен при раке. В этом исследовании обнаруживается неожиданный участник у входа в ядро клетки — большой каркасный белок TPR, который помогает тонко настраивать перевод сигналов роста в всплески активности генов. Понимание этого дополнительного уровня контроля может открыть новые пути для считывания и, в перспективе, коррекции сигнальной активности, связанной с раком у пациентов.
Страж у границы ядра
Поверхность каждого клеточного ядра усыпана тысячами ядерных пор — массивных каналов, через которые молекулы перемещаются внутрь и наружу. TPR — длинный структурный белок, прикреплённый к внутренней стороне этих пор. Ранее ему приписывали функции экспорта РНК и поддержания стабильности генома, но его роль в контроле роста оставалась неясной, хотя уровни TPR нарушены при нескольких типах рака. Авторы задали вопрос, не является ли TPR просто пассивной частью поры, а также отзывчивым элементом, связывающим поступающие сигналы роста с изменениями в активности генов глубоко внутри ядра.
Прослушивание сигналов роста у ядерной поры
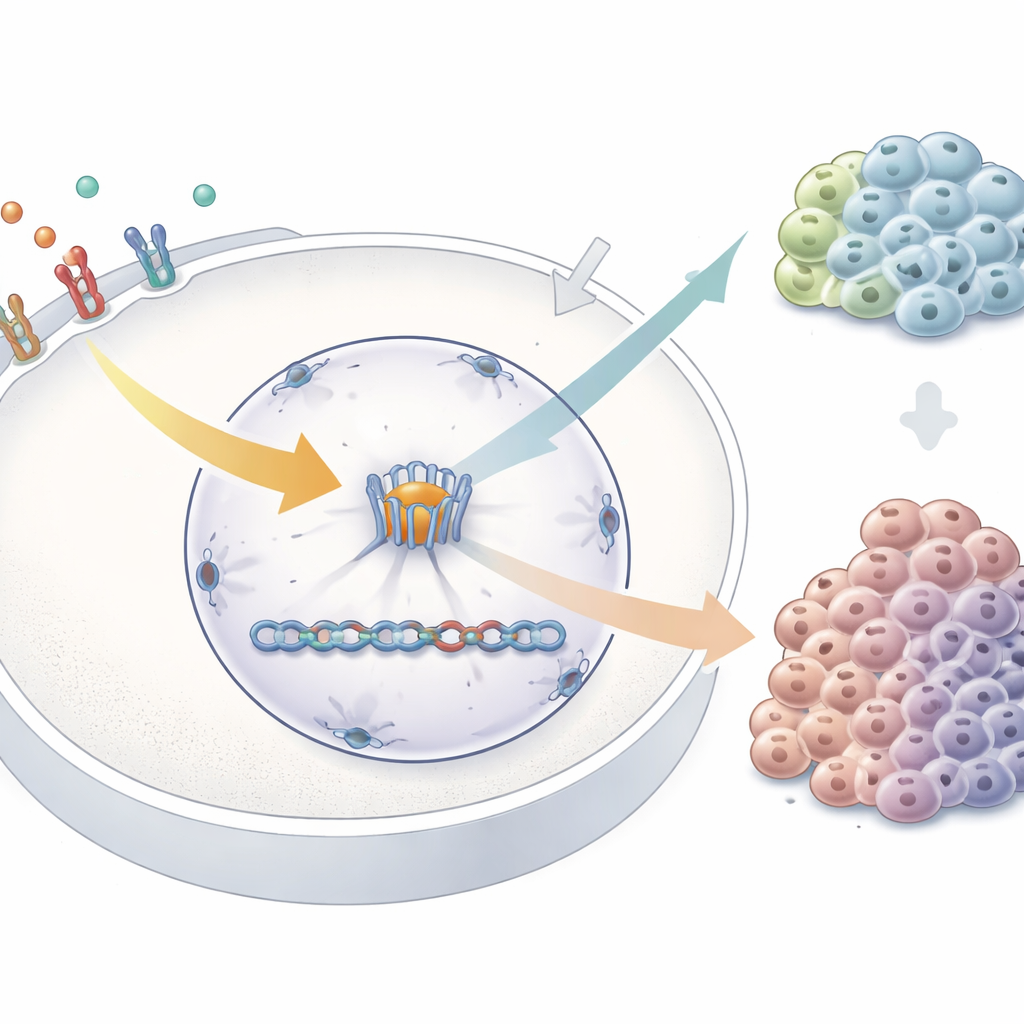
Чтобы проверить эту идею, исследователи уменьшили уровень TPR в человеческих раковых клетках и затем стимулировали их эпидермальным фактором роста, классическим инициатором MAPK‑цепочки. С помощью РНК‑секвенирования они сравнили активность генов в нормальных и лишённых TPR клетках как в состоянии покоя, так и после стимуляции. Они обнаружили, что при отсутствии TPR поведение сотен генов изменялось, включая многие, связанные непосредственно с путём MAPK. Некоторые гены, вовлечённые в продвижение роста и механизмы обратной связи, уже были нарушены в нестимулированных клетках, тогда как другие изменяли активность только после поступления сигнала роста. Примечательно, что ген немедленного ответа FOS — один из самых быстрых реагентов на активацию MAPK — включался сильнее при дефиците TPR, и это превышение зависело от активной сигнализации фактора роста. Функционально клетки без TPR по‑другому реагировали на длительную стимуляцию, демонстрируя смещённый профиль прохождения клеточного цикла.
Химический переключатель на TPR
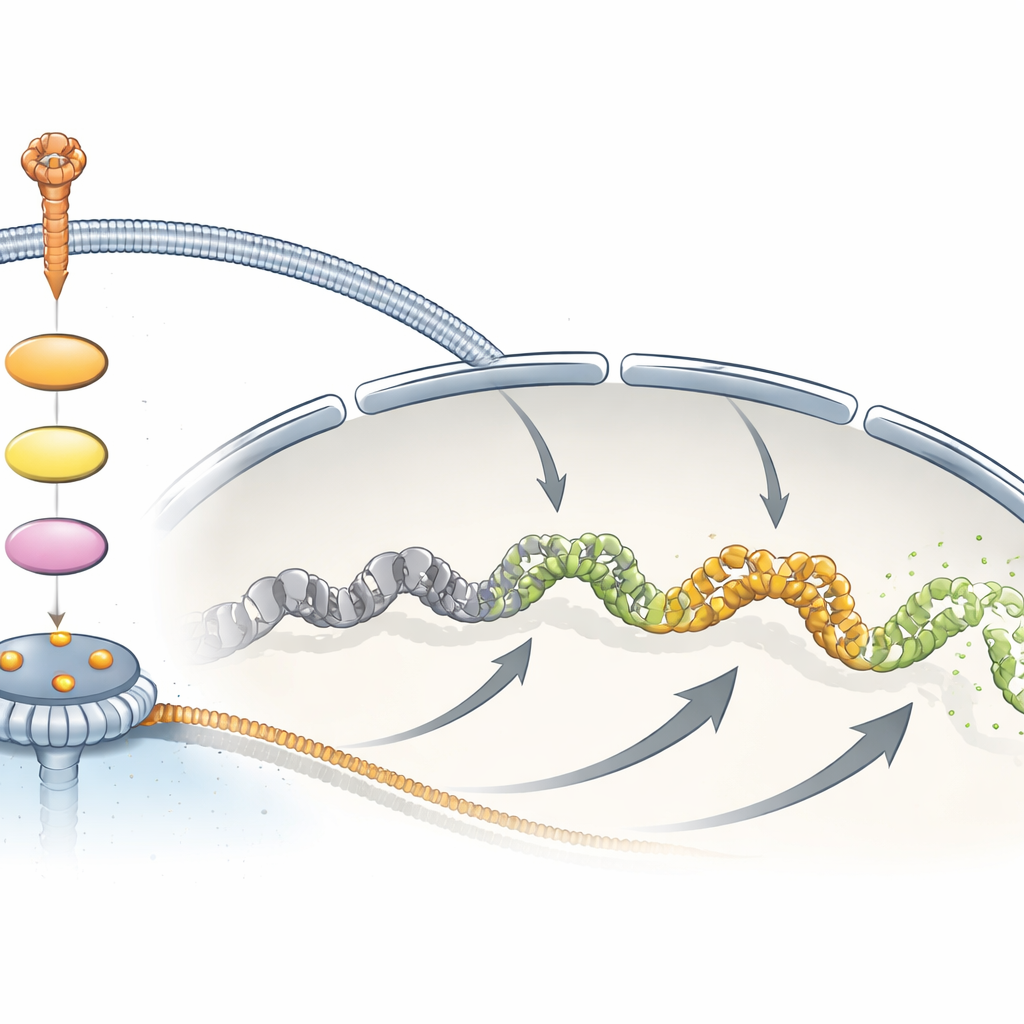
Команда затем искала физическую связь между MAPK‑сигнализацией и TPR. Ранее в больших протеомных скринингах указывалось, что конкретный сайт на TPR — аминокислота Ser2155 — становится фосфорилированным, то есть химически помеченным, после обработки фактором роста. Авторы создали высокоспецифичную антитело, распознающее TPR только при фосфорилировании в этой позиции, что позволило отслеживать эту модификацию во времени и в разных системах. В нескольких типах человеческих клеток стимуляция фактором роста быстро и транзиторно увеличивала фосфорилирование Ser2155, чётко коррелируя с активацией ERK — ключевого фермента MAPK. Блокирование рецептора фактора роста вверх по цепочке или ступеней MEK‑ERK резко снижало это фосфорилирование. Совместное удаление ERK1 и ERK2 почти полностью его устраняло, тогда как устранение самого TPR не изменяло активности ERK, что однозначно помещает TPR ниже по ходу MAPK‑каскада, а не в качестве основного сигнального компонента.
От мышей до человеческих опухолей
Чтобы проверить, важна ли эта связь вне клеточных линий, исследователи создали мышей с одной рабочей копией гена Tpr; полная утрата оказывалась летальной на этапе развития. В их селезёнках — ткани, где иммунные клетки активируют MAPK‑путь через антигенные рецепторы, а не через рецепторы фактора роста — общий профиль активности генов изменился, вновь обогащаясь генами, связанными с MAPK, и ослабляя несколько естественных тормозов этого пути. Когда спленоциты этих мышей были стимулированы через T‑клеточные рецепторы, они производили больше матричной РНК Fos, чем клетки от нормальных животных, повторяя результаты, полученные на человеческих культурах. Команда затем проанализировала образцы человеческих опухолей. В большинстве серозных опухолей яичника и в большой подгруппе тройных негативных раков молочной железы окрашивание в сторону фосфорилированного TPR на Ser2155 было обычным явлением, хотя опухоли молочной железы демонстрировали гораздо большую изменчивость от случая к случаю, что согласуется с их разнородными паттернами активации пути.
Почему это важно для рака и терапии
В сумме полученные данные рисуют TPR как отзывчивый ядерный фактор, расположенный у ядерной поры и химически регулируемый MAPK‑путём. Вместо того чтобы включать или выключать путь, TPR помогает формировать амплитуду и характер транскрипционного всплеска, который следует за стимуляцией ростом или иммунным сигналом, особенно для быстро индуцируемых генов, таких как FOS. Поскольку многие опухоли зависят от постоянной активности MAPK, наличие и состояние фосфорилирования TPR могут служить полезным маркером вовлечённости пути в опухолях, а нарушение его регуляции может способствовать искажённым ростовым реакциям. Эта работа расширяет наше представление о ядерных порах от статичных ворот до активных участников в том, как клетки интерпретируют митогенные сигналы.
Цитирование: Liu, J., Zheng, Y., Xiong, Y. et al. Nucleoporin TPR integrates MAPK signaling with mitogen-induced transcriptional programs. Cell Death Dis 17, 400 (2026). https://doi.org/10.1038/s41419-026-08760-8
Ключевые слова: ядерная пора, MAPK‑сигнализация, белок TPR, сигнализация факторов роста, транскрипция при раке