Clear Sky Science · sv
Nukleoporin TPR kopplar ihop MAPK‑signalering med mitogeninducerade transkriptionsprogram
Hur celler bestämmer när de ska växa
Våra celler tar ständigt emot gå‑ eller stanna‑signaler som talar om när de ska dela sig, vila eller reagera på sin omgivning. Många av dessa kommandon färdas via en välkänd kedja av proteiner kallad MAPK‑vägen, som ofta är överaktiv i cancer. Denna studie avslöjar en oväntad aktör vid porten till cellkärnan — ett stort scaffold‑protein med namnet TPR — som hjälper till att finjustera hur tillväxtsignaler översätts till utbrott av genaktivitet. Att förstå detta extra kontrollager kan öppna nya vägar för att avläsa, och så småningom justera, cancerrelaterad signalering hos patienter.
En grindvakt vid kärnans kant
Varje cellkärna är täckt av tusentals kärnporer — massiva kanaler som låter molekyler röra sig in och ut. TPR är ett långsträckt strukturellt protein som är fäst på den inre sidan av dessa porer. Det var känt för att hjälpa till med uppgifter som RNA‑export och att upprätthålla genomstabilitet, men dess roll i tillväxtkontroll var oklar, trots att dess nivåer är onormala i flera cancerformer. Författarna undrade om TPR inte bara är en passiv del av poren utan också ett responsivt element som kopplar inkommande tillväxtsignaler till förändringar i genaktivitet djupt inne i kärnan.
Lyssna på tillväxtsignaler vid kärnporen
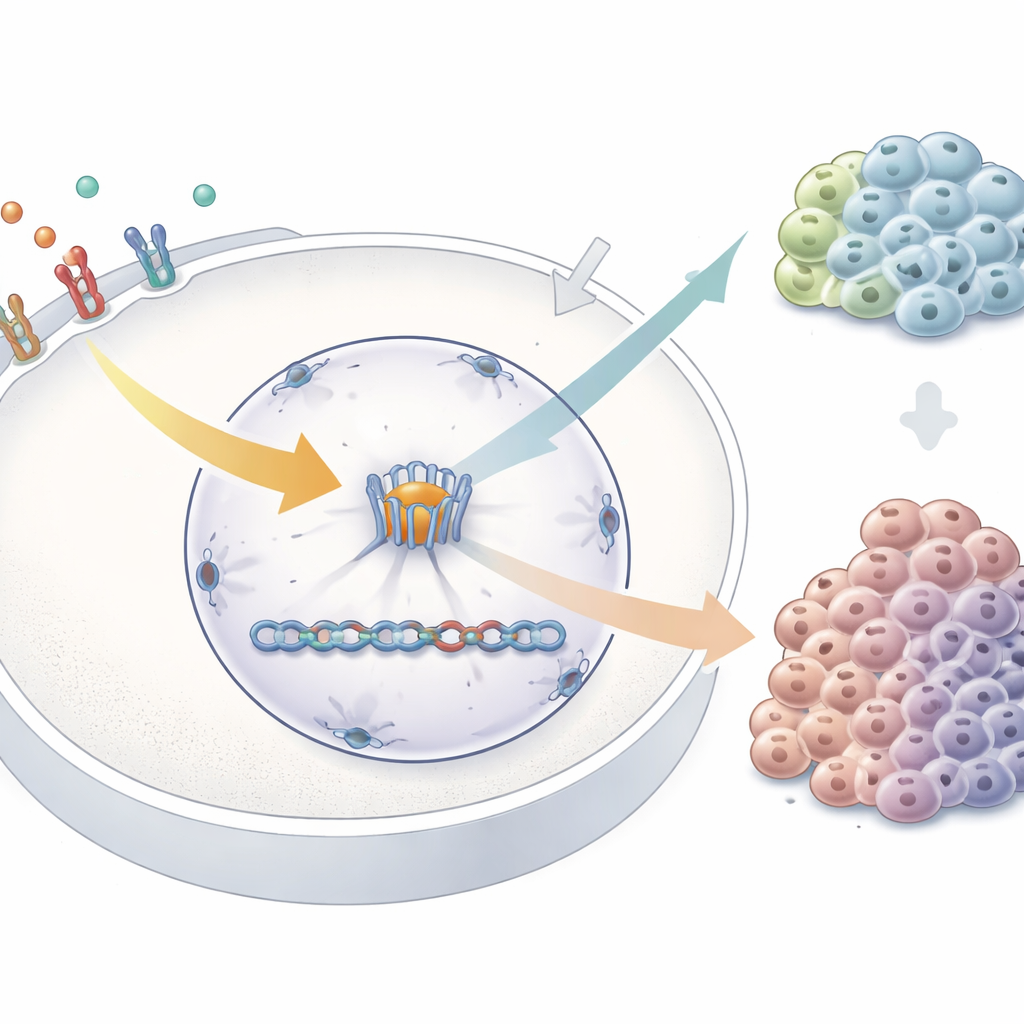
För att pröva idén minskade forskarna TPR‑nivåerna i mänskliga cancerceller och stimulerade dem sedan med epidermal tillväxtfaktor, en klassisk utlösare av MAPK‑signalkedjan. Med RNA‑sekvensering jämförde de genaktivitet i normala respektive TPR‑utarmade celler, både i vila och efter stimulans. De fann att hundratals gener ändrade sitt beteende när TPR saknades, inklusive många kopplade till själva MAPK‑vägen. Vissa gener kopplade till tillväxtfrämjande processer och feedback‑kontroll var redan förändrade i ostimulerade celler, medan andra ändrade sig först efter att tillväxtsignalen anlänt. Noterbart var att en omedelbar‑tidig gen kallad FOS — en av de snabbaste respondenterna på MAPK‑aktivering — slogs på starkare när TPR var utarmat, och denna överreaktion berodde på aktiv tillväxtfaktor‑signalering. Funktionellt reagerade celler utan TPR onormalt på förlängd stimulans och visade ett förskjutet mönster av cellcykelprogression.
En kemisk brytare på TPR
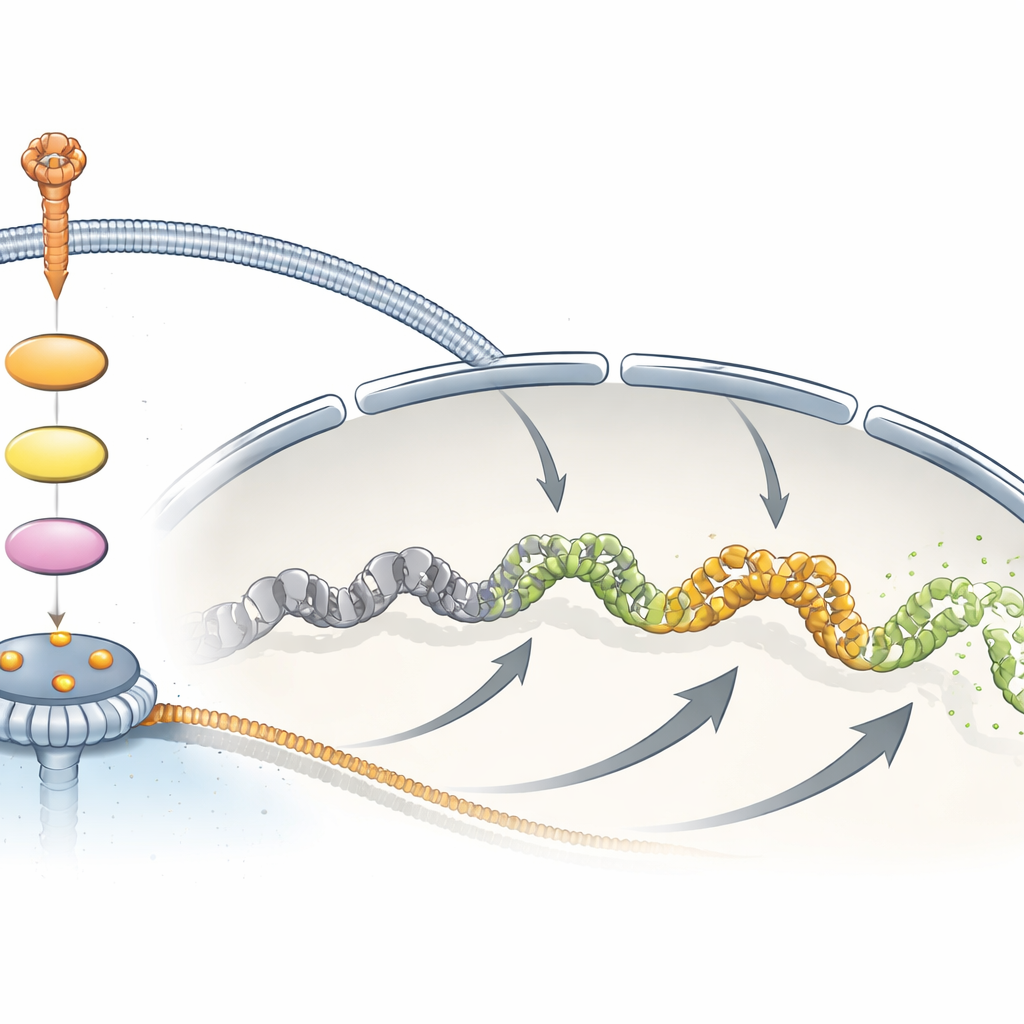
Teamet letade därefter efter en fysisk koppling mellan MAPK‑signalering och TPR. Tidigare storskaliga proteinskanningar hade antytt att en specifik plats på TPR, en aminosyra kallad Ser2155, blir fosforylerad — det vill säga kemiskt märkt — efter behandling med tillväxtfaktor. Författarna framställde en högspecifik antikropp som känner igen TPR endast när denna plats är fosforylerad, vilket gjorde det möjligt att följa denna modifiering över tid och i olika system. I flera humana celltyper ökade fosforyleringen vid Ser2155 snabbt och transient efter tillväxtfaktorstimulans, i nära samspel med aktiveringen av ERK, ett centralt MAPK‑enzym. Blockering av den uppströms tillväxtfaktorreceptorn, eller MEK‑ERK‑stegen i vägen, minskade denna fosforylering kraftigt. Att ta bort både ERK1 och ERK2 nästan eliminerade fosforyleringen, medan eliminering av TPR i sig inte förändrade ERK‑aktiviteten, vilket placerar TPR tydligt nedströms i MAPK‑kaskaden snarare än som en kärnsignalbeståndsdel.
Från möss till humana tumörer
För att testa om denna koppling är viktig bortom cellinjer skapade forskarna möss med endast en fungerande kopia av Tpr‑genen; fullständig förlust var dödlig under utvecklingen. I deras mjält — en vävnad där immunceller aktiverar MAPK‑vägen via sina antigena receptorer snarare än genom tillväxtfaktorreceptorer — skiftade det övergripande mönstret av genaktivitet, återigen med en berikning för MAPK‑relaterade gener och en dämpning av flera naturliga bromsar i vägen. När splenocyter från dessa möss stimulerades via sina T‑cellsreceptorer producerade de mer Fos‑mRNA än celler från normala djur, och speglade resultaten från humana cellkulturer. Teamet undersökte sedan humana tumörprover. I de flesta serösa ovarietumörerna och i en stor delmängd av trippelnegativa bröstcancerfall var färgning för fosforylerat TPR vid Ser2155 vanlig, även om brösttumörerna uppvisade mycket större variation mellan fall, förenligt med deras blandade aktiveringsmönster av vägen.
Varför detta är viktigt för cancer och terapi
Sammantaget framställer resultaten TPR som en responsiv nukleär faktor som sitter vid kärnporen och kemiskt fininställs av MAPK‑vägen. Istället för att slå på eller av vägen hjälper TPR till att forma amplituden och kvaliteten av det transkriptionella utbrott som följer tillväxt‑ eller immunstimulans, särskilt för snabbt inducerade gener som FOS. Eftersom många cancerformer är beroende av ihållande MAPK‑aktivitet kan närvaron och fosforyleringsstatusen hos TPR fungera som en användbar avläsning av vägens engagemang i tumörer, och dess felreglering kan bidra till förvrängda tillväxtsvar. Detta arbete vidgar vår bild av kärnporer från statiska portar till aktiva deltagare i hur celler tolkar mitogena signaler.
Citering: Liu, J., Zheng, Y., Xiong, Y. et al. Nucleoporin TPR integrates MAPK signaling with mitogen-induced transcriptional programs. Cell Death Dis 17, 400 (2026). https://doi.org/10.1038/s41419-026-08760-8
Nyckelord: kärnpor, MAPK‑signalering, TPR‑protein, tillväxtfaktor‑signalering, cancer‑transkription