Clear Sky Science · zh
Alox8 基因敲除加剧依米喹莫德诱导的类银屑病炎症
为什么这个皮肤故事重要
银屑病远不止干燥、脱屑的皮肤。它是一种慢性炎性疾病,可能伴随疼痛、污名化,并与关节炎和心脏病等问题相关。本研究探讨了小鼠皮肤中一种鲜为人知的酶 Alox8,该酶参与将脂肪代谢为化学信使。通过关闭该酶,研究人员揭示了皮肤脂质的微小变化如何将愈合与失控炎症之间的平衡推向一端,为理解银屑病加重的原因及可能的缓解手段提供了新的线索。
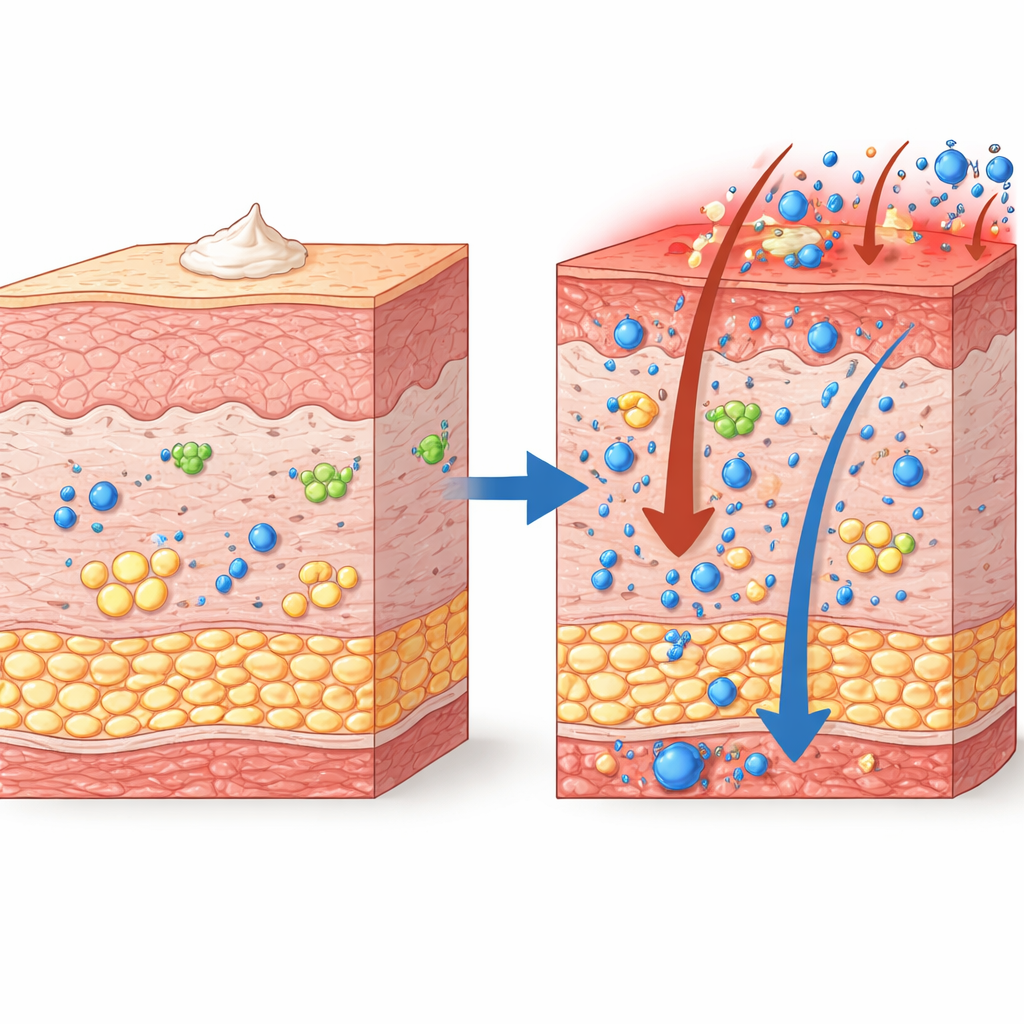
一位不起眼却重要的酶
我们的皮肤富含脂质——脂肪和油脂——它们不仅形成防水屏障,还能作为免疫细胞的信号。称为脂氧合酶的酶将多不饱和脂肪转化为短寿命的信使分子,这些分子可以促进或消除炎症。Alox8 是小鼠中对应人类酶 ALOX15B 的同源物,ALOX15B 在银屑病患者皮肤中表达增高,似乎有助于关闭炎症。然而在这项工作之前,Alox8 在活体动物和类银屑病病程中的作用尚不清楚,部分原因是缺乏合适的敲除小鼠模型。
在小鼠中探索类银屑病
作者构建了在活性位点上功能性失活的 Alox8 缺陷小鼠。随后他们采用一种标准的类银屑病皮肤模型——用能激活免疫的依米喹莫德膏剂涂抹背部皮肤,诱发发红、增厚和脱屑。首先,他们绘制了 Alox8 的常见表达部位,发现其在皮肤、皮脂腺以及卵巢、唾液腺等某些组织中高表达。在健康动物中,Alox8 将多不饱和脂肪转化为特定产物,但在敲除小鼠中这些由 Alox8 产生的脂质显著减少,证实了该酶活性的丧失。
当刹车失效,炎症更猛烈
与正常小鼠相比,缺失 Alox8 的动物在依米喹莫德处理后出现更严重且持续时间更长的类银屑病改变。它们的皮肤更增厚、更发红,外层细胞表现出过度增殖的迹象,而非有序成熟。显微镜下可见增殖细胞数量增加、出现与 DNA 损伤相关细胞死亡的细胞减少,这些共同解释了表皮增厚的现象。免疫表型分析显示多种免疫细胞大量浸润,尤其是一类称为 γδ T 细胞的子集,这类细胞已知可在皮肤中产生强效的促炎细胞因子。
在分子水平上,Alox8 缺失重塑了皮肤的脂质格局。非靶向脂质组学显示多类脂质发生广泛变化,包括对角鲨烷和鞘磷脂等分子减少,这些分子对屏障结构和抑制细胞增殖很重要。与此同时,促炎通路被激活。环氧合酶-2(Cox2)——合成前列腺素的酶——在敲除小鼠中更早更高地上调,并伴随前列腺素 E2 产生增加。该脂质信使已知可促进 γδ T 细胞产生白细胞介素-17,与之相应,敲除小鼠显示白细胞介素-17 和白细胞介素-22 水平升高,以及吸引更多免疫细胞到皮肤的趋化因子上调。
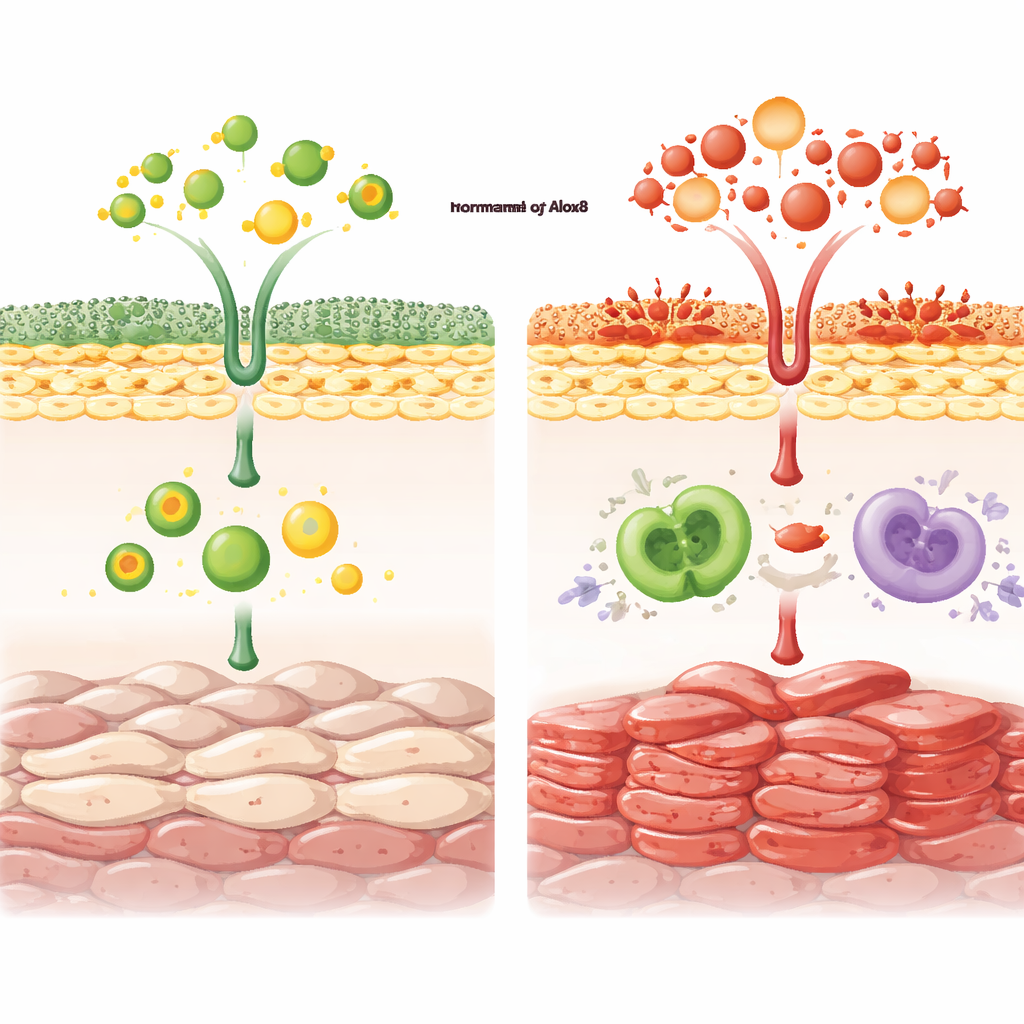
氧化脂质:并非总是“反派”
一个有趣的发现涉及 4-羟基壬烯醛(4-HNE),它是脂质过氧化的标志,常与氧化应激和细胞死亡相关。在正常小鼠中,依米喹莫德会增加表皮中的这种氧化脂质,但在 Alox8 敲除小鼠中这种增加被削弱。尽管损伤标志物减少,敲除动物的疾病更严重,这表明某些受控的脂质氧化形式可能实际上有助于清除受损细胞并促进炎症的消退。Alox8 的丧失似乎扰乱了这一微妙平衡,减少了程序性细胞死亡,同时偏向增殖和慢性免疫激活。
这对理解银屑病意味着什么
综合来看,这项工作将 Alox8 描绘为一种体内制动系统的一部分,帮助小鼠皮肤从炎性损伤中恢复。没有这种酶,特定的脂质信使下降、更广泛的脂质环境失序,并且通过前列腺素和 T 细胞细胞因子的信号传导被放大。结果是皮肤更增厚、更炎性,且需要更长时间才能平息。虽然小鼠并非人类,Alox8 与其人类同源 ALOX15B 的化学特性也不完全相同,但该研究强化了这样一种观点:在皮肤中微调脂质代谢可能是预防或缩短银屑病发作的有力策略,并提示增强这一通路的活性或其产物,有朝一日或可成为局部作用新疗法的基础。
引用: Palmer, M.A., Kirchhoff, R., Hahnefeld, L. et al. Alox8 knockout exacerbates imiquimod-induced psoriasis-like inflammation. Cell Death Dis 17, 390 (2026). https://doi.org/10.1038/s41419-026-08727-9
关键词: 银屑病, 皮肤炎症, 脂质介质, 免疫细胞, 前列腺素