Clear Sky Science · pt
Remoção de Alox8 agrava a inflamação tipo psoríase induzida por imiquimode
Por que essa história da pele importa
Psoríase é muito mais do que pele seca e escamosa. É uma doença inflamatória crônica que pode ser dolorosa, estigmatizante e associada a problemas como artrite e doenças cardíacas. Este estudo investiga uma enzima pouco conhecida na pele de camundongos, chamada Alox8, que ajuda a processar gorduras em mensageiros químicos. Ao desativar essa enzima, os pesquisadores revelaram como pequenas mudanças nos lipídios cutâneos podem desequilibrar o processo entre cura e inflamação descontrolada, oferecendo pistas novas sobre por que a psoríase entra em crise e o que poderia acalmá-la.
Uma enzima discreta com papel importante
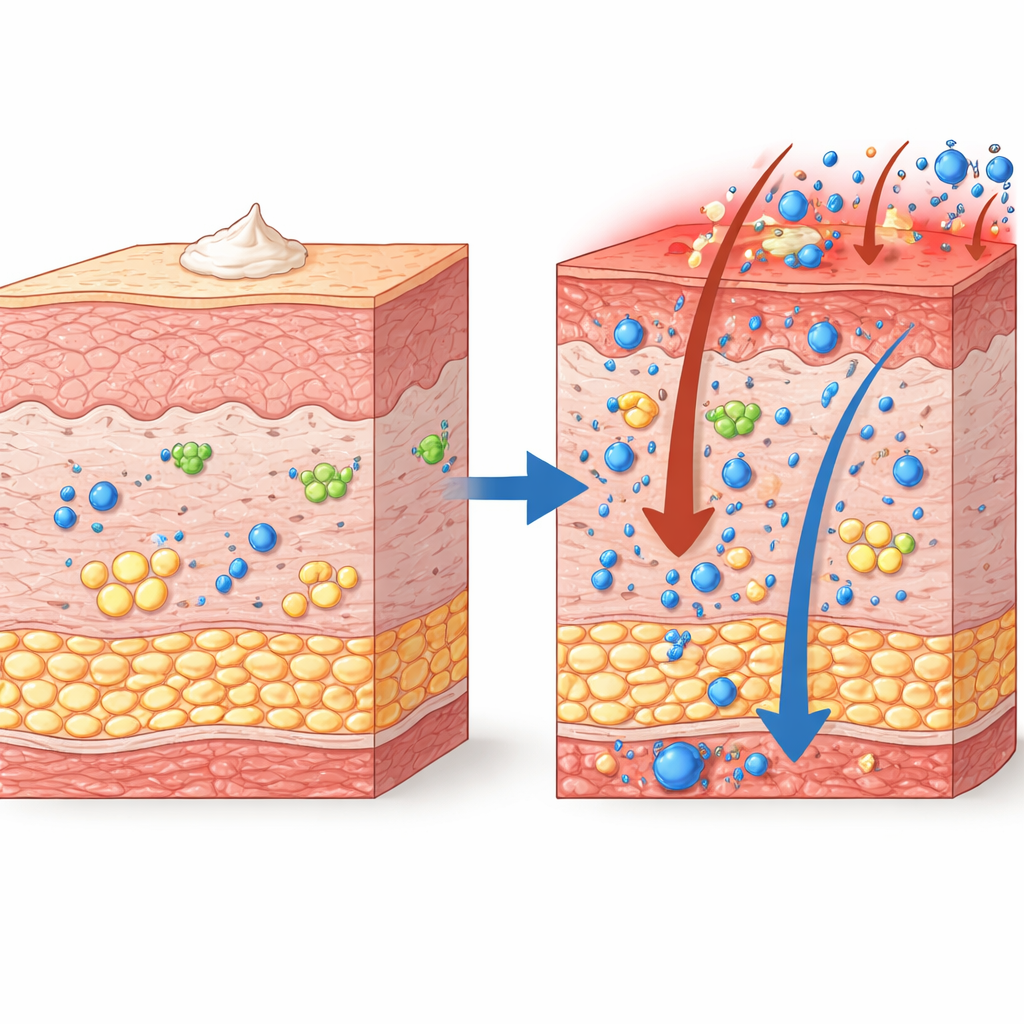
Nossa pele é rica em lipídios — gorduras e óleos — que não só formam uma barreira impermeável, mas também atuam como sinais para células imunes. Enzimas chamadas lipoxigenases convertem gorduras poli-insaturadas em mensageiros de curta duração que podem tanto alimentar quanto resolver a inflamação. Alox8 é o equivalente em camundongo de uma enzima humana, ALOX15B, que está aumentada na pele de pessoas com psoríase e parece ajudar a desligar a inflamação. Antes deste trabalho, porém, o papel de Alox8 em animais vivos e em doença tipo psoríase era incerto, em parte porque camundongos com o gene adequado não existiam.
Investigando a psoríase em camundongos
Os autores produziram camundongos nos quais Alox8 foi funcionalmente desativada em seu sítio ativo. Em seguida, usaram um modelo padrão de doença cutânea tipo psoríase, aplicando imiquimode nas costas — um creme que ativa o sistema imune e provoca vermelhidão, espessamento e descamação. Primeiro, mapearam onde Alox8 é normalmente ativa e encontraram forte expressão na pele, em glândulas sebáceas e em outros tecidos como ovário e glândula salivar. Em animais saudáveis, Alox8 transformava gorduras poli-insaturadas em produtos específicos, mas esses lipídios derivados de Alox8 foram fortemente reduzidos nos camundongos knockout, confirmando que a atividade da enzima foi efetivamente perdida.
Quando o freio some, a inflamação esquenta
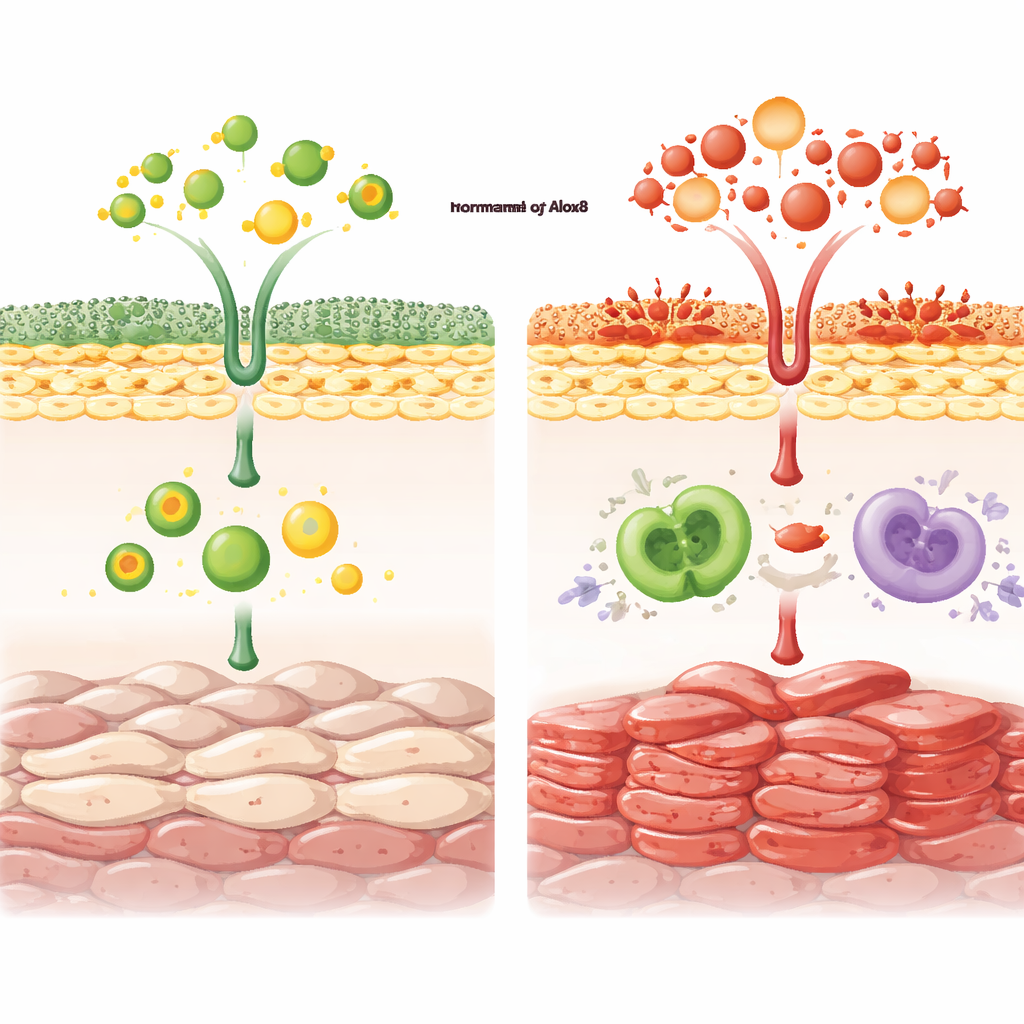
Em comparação com camundongos normais, os animais sem Alox8 desenvolveram alterações tipo psoríase mais graves e duradouras após o imiquimode. A pele ficou mais espessa e mais avermelhada, e as camadas externas de células exibiram sinais de hiperproliferação em vez de maturação ordenada. A microscopia revelou mais células em divisão e menos células sofrendo morte associada a dano de DNA, o que ajuda a explicar a epiderme espessada. A análise imune mostrou infiltração maior por vários tipos de células imunes, especialmente um subconjunto de células T chamado células T γδ, conhecidas por produzir citocinas inflamatórias potentes na pele.
No nível molecular, a deficiência de Alox8 remodelou o panorama lipídico da pele. Lipidômica não direcionada mostrou mudanças amplas em muitas classes lipídicas, incluindo reduções em ceramidas e esfingomielinas, moléculas importantes para a estrutura da barreira e para restringir o crescimento celular. Ao mesmo tempo, vias pró-inflamatórias ganharam intensidade. Níveis de cicloxigenase-2 (Cox2), uma enzima que produz prostaglandinas, aumentaram mais cedo e em maior grau nos camundongos knockout, acompanhados por maior produção de prostaglandina E2. Esse mensageiro lipídico é conhecido por aumentar a produção de interleucina-17 por células T γδ e, coerente com isso, os camundongos knockout exibiram níveis elevados de interleucina-17 e interleucina-22, assim como quimiocinas que atraem mais células imunes para a pele.
Gorduras oxidadas: nem sempre vilãs
Uma descoberta intrigante envolveu 4-hidroxinonenal, um marcador de peroxidação lipídica frequentemente associado ao estresse oxidativo e à morte celular. Em camundongos normais, o imiquimode aumentou esse lipídio oxidado na epiderme, mas essa elevação foi atenuada nos knockout de Alox8. Apesar de terem menos desse marcador de dano, os animais knockout apresentaram doença mais grave, sugerindo que algumas formas de oxidação lipídica controlada podem na verdade favorecer a remoção de células danificadas e ajudar a resolver a inflamação. A perda de Alox8 parece perturbar esse equilíbrio delicado, reduzindo a morte celular programada enquanto favorece a proliferação e a ativação imune crônica.
O que isso significa para entender a psoríase
Em conjunto, o trabalho descreve Alox8 como parte de um sistema de freio interno que ajuda a pele de camundongo a recuperar-se de insultos inflamatórios. Sem essa enzima, mensageiros lipídicos específicos diminuem, o ambiente lipídico mais amplo se desordena e a sinalização via prostaglandinas e citocinas de células T se torna exagerada. O resultado é pele mais espessa e inflamada que demora mais a se acalmar. Embora camundongos não sejam humanos, e a química de Alox8 e de sua equivalente humana ALOX15B não seja idêntica, o estudo reforça a ideia de que ajustar finamente o metabolismo lipídico na pele pode ser uma estratégia poderosa para prevenir ou encurtar surtos de psoríase, e sugere que aumentar a atividade ou os produtos dessa via poderia um dia formar a base de novos tratamentos de ação local.
Citação: Palmer, M.A., Kirchhoff, R., Hahnefeld, L. et al. Alox8 knockout exacerbates imiquimod-induced psoriasis-like inflammation. Cell Death Dis 17, 390 (2026). https://doi.org/10.1038/s41419-026-08727-9
Palavras-chave: psoríase, inflamação cutânea, mediadores lipídicos, células imunes, prostaglandinas