Clear Sky Science · pl
Usunięcie Alox8 nasila imiquimodem wywołane zapalenie podobne do łuszczycy
Dlaczego ta skórna historia ma znaczenie
Łuszczyca to znacznie więcej niż sucha, łuszcząca się skóra. To przewlekła choroba zapalna, która może być bolesna, stygmatyzująca i powiązana z problemami, takimi jak zapalenie stawów czy choroby serca. W tym badaniu zbadano mało znany enzym w skórze myszy, nazwany Alox8, który pomaga przetwarzać tłuszcze na cząsteczki sygnałowe. Wyłączając ten enzym, badacze odsłonili, jak niewielkie zmiany w lipidach skórnych mogą przechylić równowagę między gojeniem a wymykającym się spod kontroli zapaleniem, dostarczając nowych wskazówek, dlaczego występują zaostrzenia łuszczycy i co mogłoby je złagodzić.
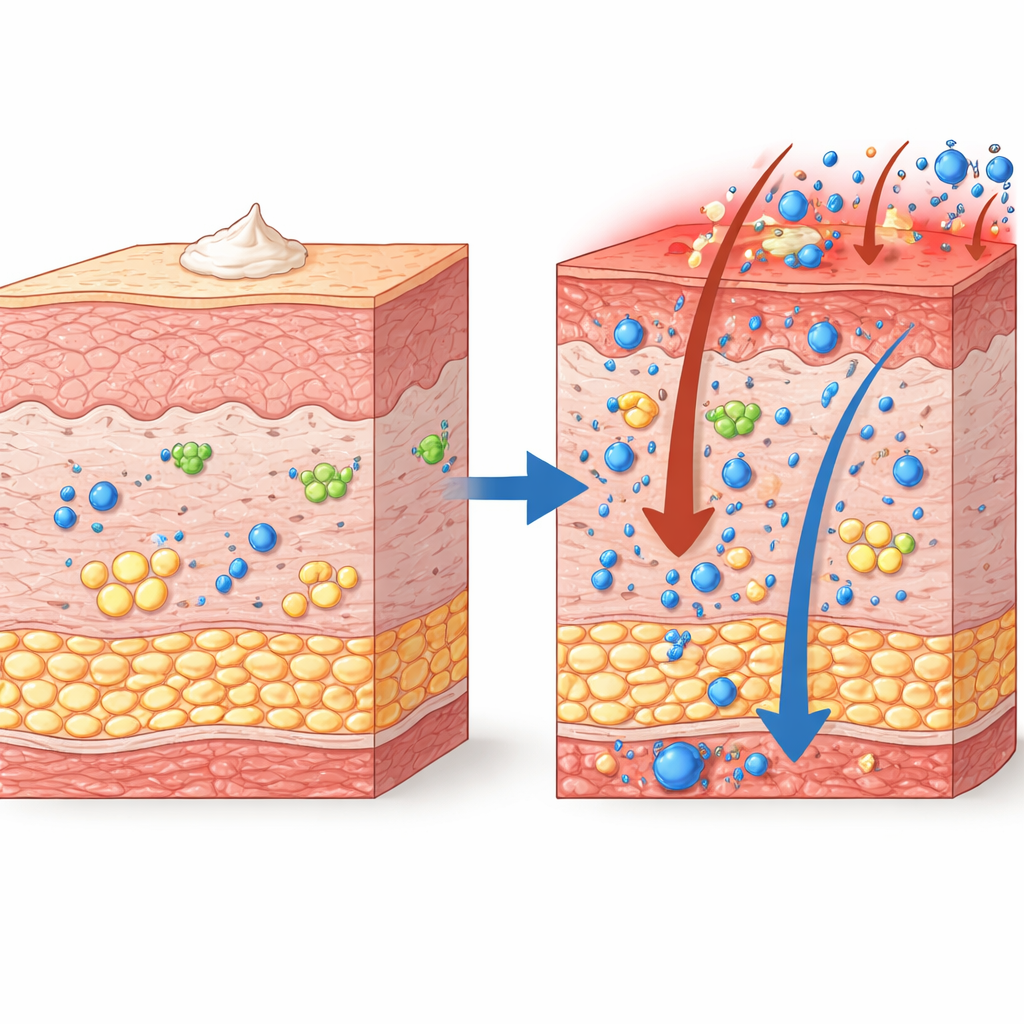
Cichy enzym o dużej roli
Nasza skóra jest pełna lipidów — tłuszczów i olejów — które nie tylko tworzą wodoodporną barierę, lecz także działają jako sygnały dla komórek odpornościowych. Enzymy zwane lipoksygenazami przekształcają wielonienasycone kwasy tłuszczowe w krótkotrwałe przekaźniki, które mogą zarówno napędzać, jak i wygaszać zapalenie. Alox8 to mysia odpowiedniczka enzymu ludzkiego, ALOX15B, którego poziom jest podwyższony w skórze osób z łuszczycą i który wydaje się pomagać w wyłączaniu stanu zapalnego. Jednak przed tym badaniem rola Alox8 u żywych zwierząt i w chorobie podobnej do łuszczycy była niejasna, częściowo dlatego, że nie istniały odpowiednie myszy z wyciszonym genem.
Badanie łuszczycy u myszy
Badacze zaprojektowali myszy, u których Alox8 został funkcjonalnie unieszkodliwiony w miejscu aktywnym. Następnie zastosowali standardowy model choroby skóry podobnej do łuszczycy, nakładając na skórę grzbietu imiquimod — krem aktywujący odporność, który wywołuje zaczerwienienie, pogrubienie i łuszczenie. Najpierw zmapowali, gdzie Alox8 jest normalnie aktywny i stwierdzili silną ekspresję w skórze, gruczołach łojowych oraz w niektórych innych tkankach, takich jak jajniki i gruczoł ślinowy. U zdrowych zwierząt Alox8 przekształcał wielonienasycone tłuszcze w określone produkty, ale te lipidy pochodzące od Alox8 były wyraźnie zmniejszone u myszy z wyciszonym genem, co potwierdzało, że aktywność enzymu została skutecznie utracona.
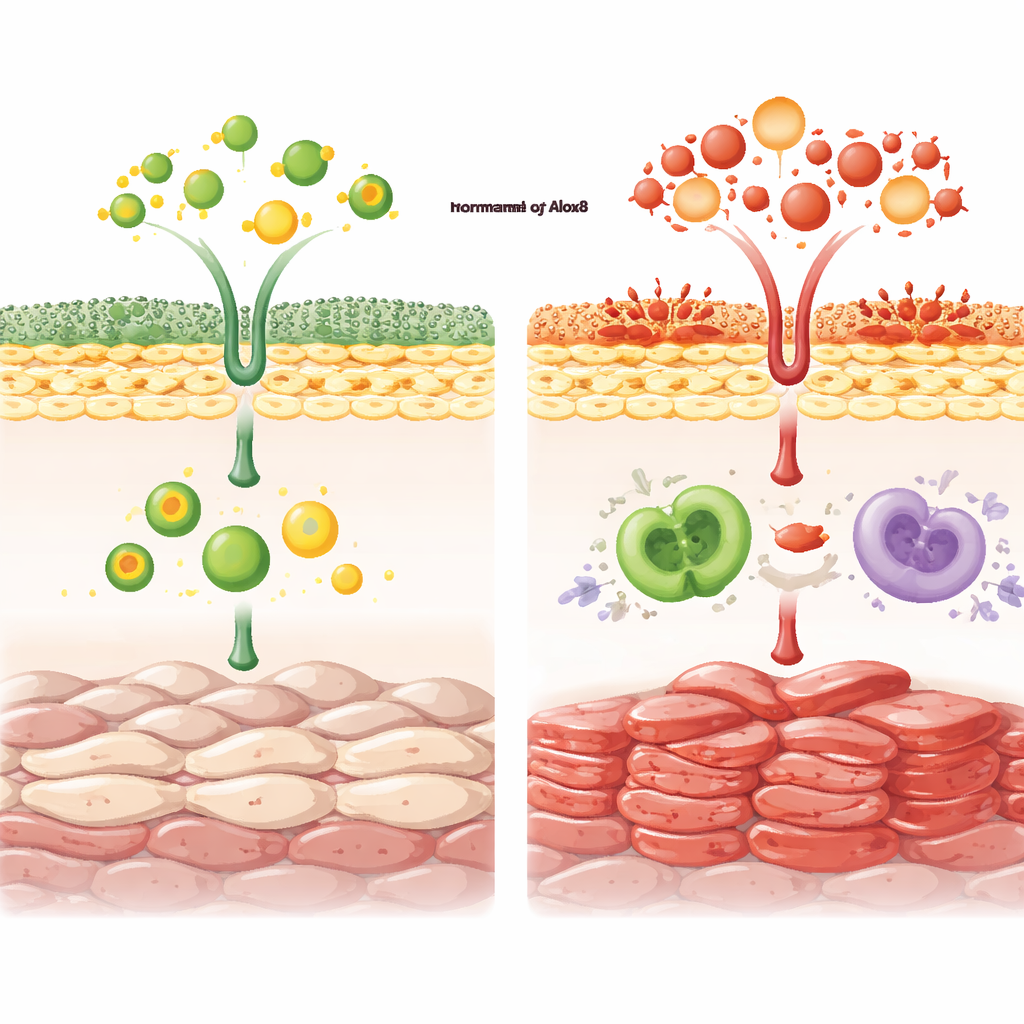
Gdy hamulec znika, zapalenie przybiera na sile
W porównaniu z normalnymi myszami zwierzęta pozbawione Alox8 rozwijały poważniejsze i dłużej utrzymujące się zmiany skórne przypominające łuszczycę po zastosowaniu imiquimodu. Ich skóra stała się grubsza i bardziej zaczerwieniona, a zewnętrzne warstwy komórek wykazywały oznaki nadmiernej proliferacji zamiast uporządkowanej dojrzewającej keratynizacji. Mikroskopia ujawniła zwiększoną liczbę dzielących się komórek i mniejszą liczbę komórek poddających się śmierci związanej z uszkodzeniem DNA, co wspólnie pomaga wyjaśnić pogrubiony naskórek. Profilowanie komórek odpornościowych wykazało silniejszą infiltrację przez kilka typów komórek odpornościowych, szczególnie podzbiór limfocytów T zwanych γδ T, które są znane z produkcji silnych cytokin zapalnych w skórze.
Na poziomie molekularnym brak Alox8 przekształcił krajobraz lipidowy skóry. Nieskierowana lipidomika wykazała szerokie przesunięcia w wielu klasach lipidów, w tym obniżenia w ceramidach i sfingomielinach — cząsteczkach ważnych dla struktury bariery i hamowania wzrostu komórek. Jednocześnie nasiliły się szlaki prozapalne. Poziomy cyklooksygenazy-2 (Cox2), enzymu wytwarzającego prostaglandyny, wzrosły wcześniej i do wyższych wartości u myszy z wyciszonym genem, któremu towarzyszyła zwiększona produkcja prostaglandyny E2. Ten lipidowy przekaźnik jest znany z pobudzania produkcji interleukiny-17 przez γδ T, i zgodnie z tym myszy z wyciszonym Alox8 wykazywały podwyższone poziomy interleukiny-17 i interleukiny-22 oraz chemokin przyciągających dodatkowe komórki odpornościowe do skóry.
Utlenione tłuszcze: nie zawsze złoczyńcy
Jednym z intrygujących odkryć było dotyczące 4-hydroksynonenalu, markera peroksydacji lipidów często kojarzonego ze stresem oksydacyjnym i śmiercią komórek. U normalnych myszy imiquimod zwiększał ten utleniony lipid w naskórku, ale ten wzrost był stłumiony u myszy bez Alox8. Pomimo mniejszej ilości tego markera uszkodzenia, myszy z wyciszonym genem miały gorszy przebieg choroby, co sugeruje, że niektóre formy kontrolowanej oksydacji lipidów mogą faktycznie wspierać usuwanie uszkodzonych komórek i pomagać w wygaszaniu zapalenia. Utrata Alox8 wydaje się zaburzać tę delikatną równowagę, zmniejszając zaprogramowaną śmierć komórek przy jednoczesnym sprzyjaniu proliferacji i przewlekłej aktywacji układu odpornościowego.
Co to oznacza dla zrozumienia łuszczycy
Podsumowując, praca przedstawia Alox8 jako element wewnętrznego hamulca, który pomaga skórze myszy odzyskiwać równowagę po zapalnych urazach. Bez tego enzymu konkretne lipidowe przekaźniki maleją, szersze środowisko lipidowe ulega zaburzeniu, a sygnalizacja za pośrednictwem prostaglandyn i cytokin T komórek zostaje wyolbrzymiona. W efekcie skóra staje się grubsza, bardziej zapalna i dłużej potrzebuje czasu, by się uspokoić. Chociaż myszy nie są ludźmi, a chemia Alox8 i jego ludzkiego odpowiednika ALOX15B nie jest identyczna, badanie wzmacnia ideę, że precyzyjne modulowanie metabolizmu lipidów w skórze może być silną strategią zapobiegania lub skracania zaostrzeń łuszczycy i sugeruje, że wzmocnienie aktywności lub produktów tego szlaku mogłoby pewnego dnia stanowić fundament nowych, miejscowo działających terapii.
Cytowanie: Palmer, M.A., Kirchhoff, R., Hahnefeld, L. et al. Alox8 knockout exacerbates imiquimod-induced psoriasis-like inflammation. Cell Death Dis 17, 390 (2026). https://doi.org/10.1038/s41419-026-08727-9
Słowa kluczowe: łuszczyca, zapalenie skóry, mediatory lipidowe, komórki układu odpornościowego, prostaglandyny