Clear Sky Science · de
Alox8-Knockout verschärft imiquimod‑induzierte psoriasisähnliche Entzündung
Warum diese Hautgeschichte wichtig ist
Psoriasis ist weit mehr als trockene, schuppende Haut. Es handelt sich um eine chronische Entzündungserkrankung, die schmerzhaft sein, stigmatisieren und mit Problemen wie Arthritis und Herzkrankheiten verknüpft sein kann. Diese Studie untersucht ein wenig beachtetes Enzym in der Maushaut, Alox8, das Fette in chemische Botenstoffe umwandelt. Durch das Abschalten dieses Enzyms zeigten die Forschenden, wie kleine Veränderungen in Hautlipiden das Gleichgewicht zwischen Heilung und unkontrollierter Entzündung kippen können, und liefern neue Hinweise darauf, warum Psoriasis aufflammt und wie man sie beruhigen könnte.
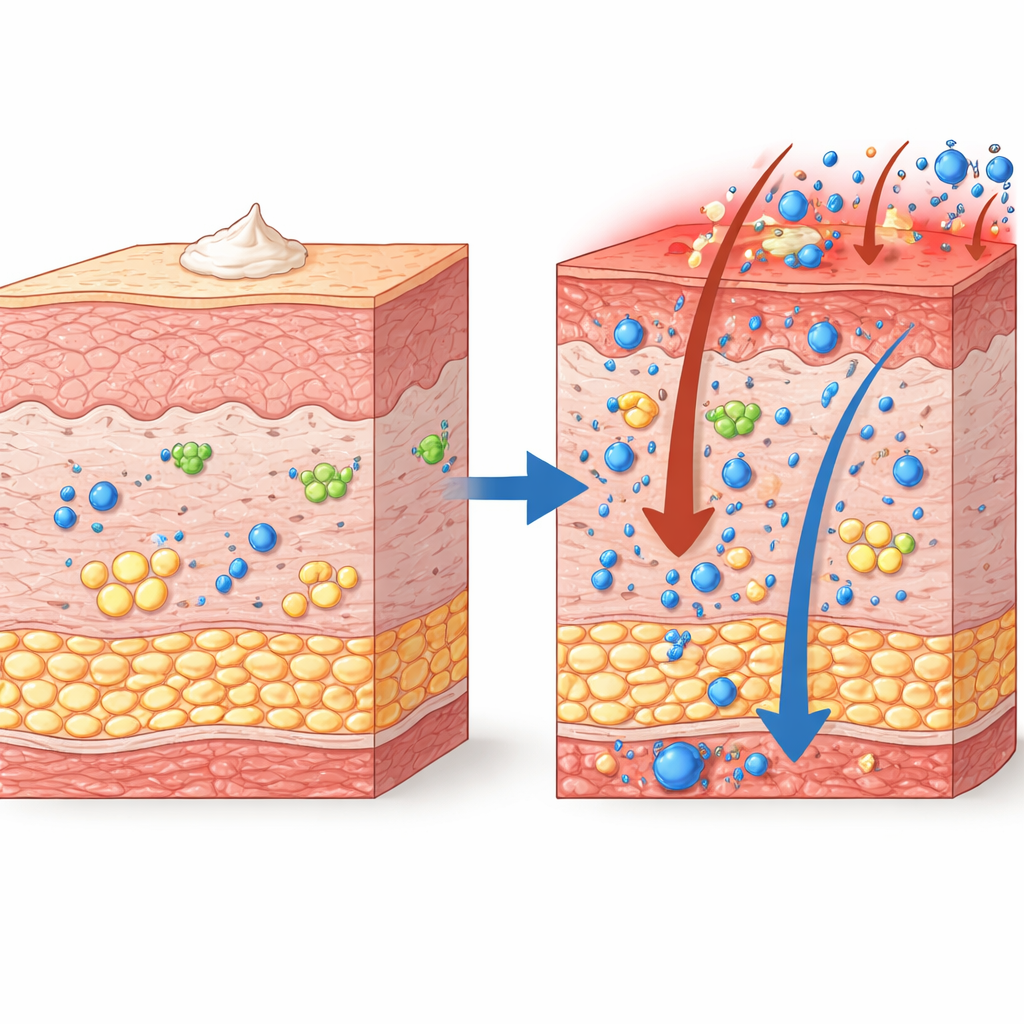
Ein stilles Enzym mit großer Aufgabe
Unsere Haut ist reich an Lipiden – Fetten und Ölen –, die nicht nur eine wasserdichte Barriere bilden, sondern auch als Signale für Immunzellen dienen. Lipoxygenase-Enzyme wandeln mehrfach ungesättigte Fette in kurzlebige Botenstoffe um, die Entzündungen entweder anheizen oder beenden können. Alox8 ist das Mausäquivalent des menschlichen Enzyms ALOX15B, das in der Haut von Psoriasispatienten erhöht ist und offenbar hilft, Entzündungen abzuschalten. Vor dieser Arbeit war die Rolle von Alox8 in lebenden Tieren und bei psoriasisähnlichen Erkrankungen unklar, zum Teil weil geeignete Knockout-Mäuse nicht existierten.
Psoriasis bei Mäusen untersuchen
Die Autorinnen und Autoren erzeugten Mäuse, in denen Alox8 an seiner aktiven Stelle funktionslos gemacht wurde. Anschließend verwendeten sie ein standardisiertes Modell für psoriasisähnliche Hauterkrankungen, bei dem die Rückenhaut mit Imiquimod bestrichen wird, einer immunaktivierenden Creme, die Rötung, Verdickung und Schuppung auslöst. Zunächst kartierten sie, wo Alox8 normalerweise aktiv ist, und fanden starke Expression in der Haut, in Talgdrüsen und in bestimmten anderen Geweben wie Eierstock und Speicheldrüse. In gesunden Tieren wandelte Alox8 mehrfach ungesättigte Fette in spezifische Produkte um, diese Alox8‑abgeleiteten Lipide waren in Knockout‑Mäusen stark reduziert, was bestätigt, dass die Enzymaktivität effektiv verloren war.
Wenn die Bremse weg ist, läuft die Entzündung heißer
Im Vergleich zu normalen Mäusen entwickelten Tiere ohne Alox8 nach Imiquimod ausgeprägtere und länger anhaltende psoriasisähnliche Veränderungen. Ihre Haut wurde dicker und röter, und die äußeren Zellschichten zeigten Zeichen von Hyperproliferation statt geordneter Reifung. Die Mikroskopie offenbarte mehr teilende Zellen und weniger Zellen mit DNA‑Schadens‑vermittelter Zelltod‑Markierung, was zusammen die verdickte Epidermis erklärt. Die Immunprofilierung zeigte stärkere Infiltration durch mehrere Immunzelltypen, vor allem durch eine Untergruppe von T‑Zellen, die γδ‑T‑Zellen genannt werden und in der Haut potente entzündliche Zytokine produzieren können.
Auf molekularer Ebene veränderte Alox8‑Mangel die lipidische Landschaft der Haut. Ungezielte Lipidomik zeigte weitreichende Verschiebungen in vielen Lipidklassen, einschließlich Abnahmen von Ceramiden und Sphingomyelinen, Molekülen, die für die Barrierestruktur und zur Begrenzung von Zellwachstum wichtig sind. Gleichzeitig fuhren proinflammatorische Wege hoch. Die Spiegel von Cyclooxygenase‑2 (Cox2), einem Enzym zur Bildung von Prostaglandinen, stiegen bei den Knockout‑Mäusen früher und stärker an, begleitet von erhöhter Produktion von Prostaglandin E2. Dieser Lipidbotenstoff ist dafür bekannt, die Produktion von Interleukin‑17 durch γδ‑T‑Zellen zu fördern; dementsprechend zeigten die Knockout‑Mäuse erhöhte Werte von Interleukin‑17 und Interleukin‑22 sowie Chemokine, die zusätzliche Immunzellen in die Haut locken.
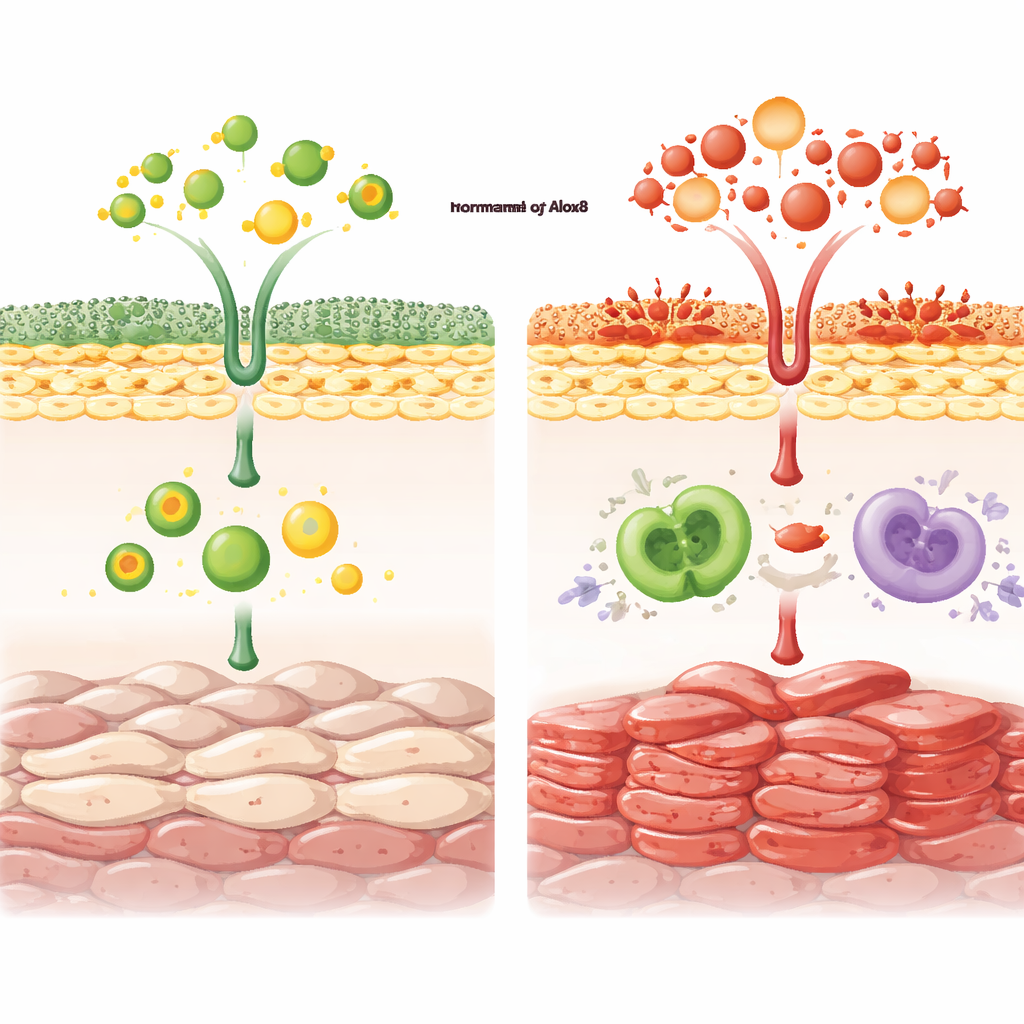
Oxidierte Fette: nicht immer die Bösewichte
Ein interessantes Ergebnis betraf 4‑Hydroxynonenal, einen Marker für Lipidperoxidation, der oft mit oxidativem Stress und Zelltod in Verbindung gebracht wird. In normalen Mäusen erhöhte Imiquimod dieses oxidierte Lipid in der Epidermis, aber dieser Anstieg war in Alox8‑Knockouts abgeschwächt. Trotz geringerer Mengen dieses Schadensmarkers hatten die Knockout‑Tiere schwerere Erkrankungen, was darauf hindeutet, dass bestimmte Formen kontrollierter Lipidoxidation tatsächlich die Entfernung geschädigter Zellen unterstützen und zur Auflösung von Entzündungen beitragen können. Der Verlust von Alox8 scheint dieses empfindliche Gleichgewicht zu stören, reduziert programmierten Zelltod und begünstigt Proliferation sowie chronische Immunaktivierung.
Was das für das Verständnis von Psoriasis bedeutet
In der Summe zeichnet die Arbeit Alox8 als Teil eines internen Bremssystems, das der Maushaut hilft, sich von entzündlichen Reizen zu erholen. Ohne dieses Enzym gehen bestimmte Lipidbotenstoffe zurück, das breitere Lipidmilieu gerät durcheinander und die Signalgebung über Prostaglandine und T‑Zell‑Zytokine wird übersteigert. Das Resultat ist dichtere, stärker entzündete Haut, die länger braucht, um sich zu beruhigen. Zwar sind Mäuse keine Menschen und die Chemie von Alox8 und seinem menschlichen Gegenstück ALOX15B ist nicht identisch, doch die Studie stützt die Vorstellung, dass eine feinabgestimmte Lipidstoffwechselregulation in der Haut eine wirksame Strategie sein könnte, Psoriasis‑Schübe zu verhindern oder zu verkürzen, und legt nahe, dass die Stärkung der Aktivität oder der Produkte dieses Weges eines Tages die Grundlage für neue lokal wirkende Therapien bilden könnte.
Zitation: Palmer, M.A., Kirchhoff, R., Hahnefeld, L. et al. Alox8 knockout exacerbates imiquimod-induced psoriasis-like inflammation. Cell Death Dis 17, 390 (2026). https://doi.org/10.1038/s41419-026-08727-9
Schlüsselwörter: Psoriasis, Hautentzündung, Lipidmediatoren, Immunzellen, Prostaglandine