Clear Sky Science · zh
KDM5C在多发性骨髓瘤中通过PERK‒Nrf2轴赋予硼替佐米耐药性的非常规作用
对患者及其家庭为何重要
多发性骨髓瘤是一种血液癌症,得益于现代药物特别是蛋白酶体抑制剂硼替佐米,治疗效果已有显著改善。然而许多患者最终会复发,因为癌细胞学会对药物产生耐受。该研究揭示了髓瘤细胞保护自身免受硼替佐米伤害的一种此前未被认识的机制,核心是被称为KDM5C的蛋白。了解这种隐藏的生存策略为延长治疗有效期提供了新的思路。
抗体制造细胞内部的应激问题
髓瘤起源于浆细胞,即体内的抗体工厂。由于它们产生大量蛋白,这些细胞持续给内质网——负责折叠和加工新生蛋白的细胞区室——施加压力。当负荷过重时,会触发一种保护性机制,称为未折叠蛋白反应。硼替佐米利用这一脆弱点,通过阻断蛋白降解,进一步超负荷内质网并将髓瘤细胞推向致命应激。然而,癌细胞可以重编程这一应激装置以求生存。作者怀疑KDM5C——一种通常通过修饰与DNA相关蛋白来控制基因活性的蛋白——可能是这类重编程的关键开关之一。
可预测侵袭性疾病和差预后药物反应的蛋白
研究者通过大规模患者数据和骨髓样本发现,髓瘤细胞中KDM5C水平远高于正常细胞。肿瘤中KDM5C表达较高的患者更可能处于晚期、治疗后复发且整体生存期更短。在被诱导对硼替佐米产生耐药的体外髓瘤细胞系中,KDM5C显著升高。当在这些细胞中降低或删除KDM5C时,其生长减缓并且对硼替佐米的敏感性显著增加——无论在培养皿内还是在小鼠肿瘤模型中均如此。这些观察结果将KDM5C定位为推动髓瘤进展的因子以及硼替佐米耐药的分子标志物。
KDM5C如何构建促生存的应激回路
为探明KDM5C如何产生这种作用,研究组检测了在关闭KDM5C时发生变化的基因。许多被改变的基因属于帮助细胞应对内质网应激的通路。其中一个基因PERK尤其下降。PERK是内质网上的一个感受器,激活后会将信号传递给名为Nrf2的因子,后者增强抗氧化防御及其他生存程序。研究表明,KDM5C维持PERK的高表达,从而允许强烈的Nrf2激活。当KDM5C被去除时,PERK水平下降,Nrf2信号减弱,髓瘤细胞应对应激的能力下降,更易被硼替佐米杀死。在缺失KDM5C的细胞中恢复PERK能挽救Nrf2活性和细胞生长,证明PERK是KDM5C与药物耐受之间的关键环节。
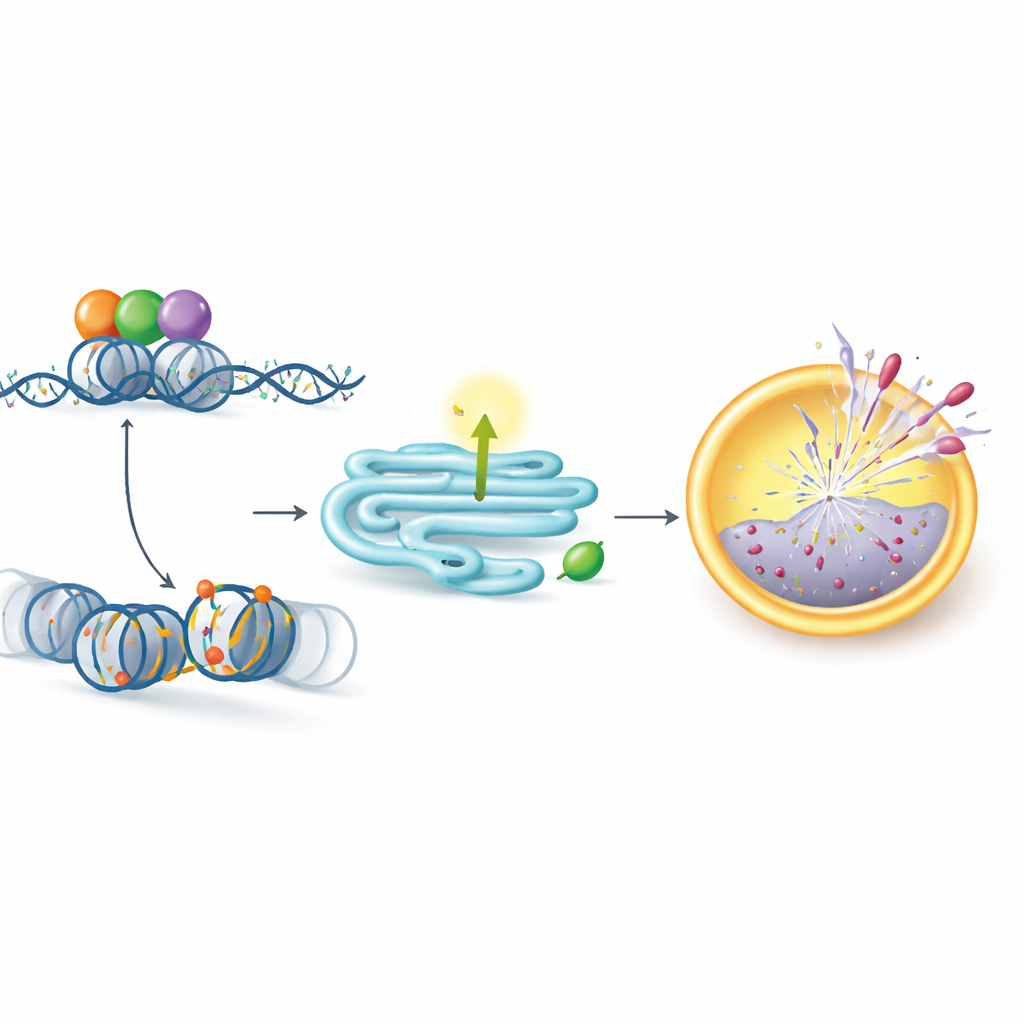
作为支架的作用重写基因活性
出人意料的是,KDM5C并非通过其传统的化学催化功能发挥作用。相反,它表现为一个支架,能将另外两种蛋白——主控生长的MYC和在关键基因开关处对组蛋白施加“开启”标记(乙酰化)的酶CBP——聚合在一起。作者显示,KDM5C、MYC和CBP形成一个大型复合体,结合在PERK基因附近并增加该位点的乙酰化,从而激活PERK。去除任一组成蛋白都会降低该位点的乙酰化并降低PERK表达。对KDM5C特定区域PHD2结构域的突变破坏了其组装复合体并激活PERK的能力,即便蛋白的其余部分保持完整。值得注意的是,一种阻断KDM5酶常规活性的药物并不影响PERK,强调该耐药通路依赖于KDM5C的结构性支架作用而非其典型的酶学功能。
这对未来治疗可能意味着什么
对于多发性骨髓瘤患者而言,这些发现突出了KDM5C作为对抗复发和硼替佐米耐药的有前景新靶点。通过帮助MYC和CBP开启PERK和Nrf2,KDM5C使髓瘤细胞能度过本应致死的严重蛋白质应激。由于这种支持并不依赖其传统的化学活性,治疗策略可能需要超越简单的酶抑制剂,而直接去除KDM5C蛋白本身——例如利用新兴的蛋白降解技术。将此类方法与硼替佐米联合使用可削弱癌细胞的应激防御,延长治疗有效期,最终改善患者结局。
引用: Lu, P., Shangguan, W., Qian, W. et al. Noncanonical role of KDM5C in conferring bortezomib resistance via the PERK‒Nrf2 axis in multiple myeloma. Cell Death Dis 17, 339 (2026). https://doi.org/10.1038/s41419-026-08591-7
关键词: 多发性骨髓瘤, 硼替佐米耐药, KDM5C, PERK Nrf2通路, 表观遗传调控