Clear Sky Science · es
Papel no canónico de KDM5C en conferir resistencia a bortezomib mediante el eje PERK‒Nrf2 en el mieloma múltiple
Por qué esto importa para pacientes y familias
El mieloma múltiple es un cáncer de la sangre que se ha vuelto mucho más tratable gracias a fármacos modernos, en particular el inhibidor del proteasoma bortezomib. Sin embargo, muchos pacientes acaban recurriendo porque las células cancerosas desarrollan resistencia al fármaco. Este estudio descubre una forma hasta ahora no reconocida en la que las células de mieloma se protegen frente al bortezomib, centrada en una proteína llamada KDM5C. Comprender este truco oculto de supervivencia apunta a nuevas estrategias para mantener la eficacia del tratamiento durante más tiempo.
Un problema de estrés dentro de las células productoras de anticuerpos
El mieloma surge de las células plasmáticas, las fábricas de anticuerpos del organismo. Debido a que producen grandes cantidades de proteína, estas células someten constantemente a tensión a un compartimento celular llamado retículo endoplásmico, que pliega y procesa las proteínas nuevas. Cuando la carga de trabajo se vuelve excesiva, se activa un sistema protector conocido como respuesta ante proteínas mal plegadas. El bortezomib explota esta vulnerabilidad bloqueando la degradación de proteínas, sobrecargando aún más el sistema y empujando a las células de mieloma hacia un estrés letal. Sin embargo, las células cancerosas pueden reconfigurar esta maquinaria de estrés para sobrevivir. Los autores sospecharon que KDM5C, una proteína que habitualmente modifica proteínas asociadas al ADN para controlar la actividad génica, podría ser uno de los interruptores clave en esta reconfiguración.
Una proteína que predice enfermedad agresiva y mala respuesta al fármaco
Analizando grandes bases de datos de pacientes y muestras de médula ósea, los investigadores hallaron que los niveles de KDM5C eran mucho más altos en las células de mieloma que en las células normales. Los pacientes cuyos tumores expresaban más KDM5C tenían más probabilidades de presentar enfermedad avanzada, de recaer tras el tratamiento y de tener una supervivencia global más corta. En líneas celulares de mieloma de laboratorio que se volvieron resistentes al bortezomib, KDM5C estaba fuertemente elevada. Cuando KDM5C se redujo o eliminó en estas células, su crecimiento se ralentizó y se volvieron notablemente más sensibles al bortezomib, tanto en cultivos como en modelos tumorales en ratones. Estas observaciones sitúan a KDM5C tanto como impulsor de la progresión del mieloma como marcador molecular de resistencia al bortezomib.
Cómo KDM5C construye un circuito de estrés pro‑supervivencia
Para ver cómo ejerce este efecto, el equipo examinó qué genes cambiaban cuando se apagaba KDM5C. Muchos pertenecían a vías que ayudan a las células a afrontar el estrés en el retículo endoplásmico. Un gen, PERK, destacó por su marcada reducción. PERK es un sensor en el retículo endoplásmico que, al activarse, envía señales a un factor llamado Nrf2, que a su vez potencia las defensas antioxidantes y otros programas de supervivencia. El estudio mostró que KDM5C es necesario para mantener altos los niveles de PERK, permitiendo una activación robusta de Nrf2. Cuando se eliminó KDM5C, los niveles de PERK cayeron, la señalización de Nrf2 se debilitó y las células de mieloma fueron menos capaces de compensar el estrés y más fácilmente eliminadas por el bortezomib. Restaurar PERK en células deficientes en KDM5C recuperó tanto la actividad de Nrf2 como el crecimiento celular, demostrando que PERK es un nexo crucial entre KDM5C y la resistencia al fármaco.
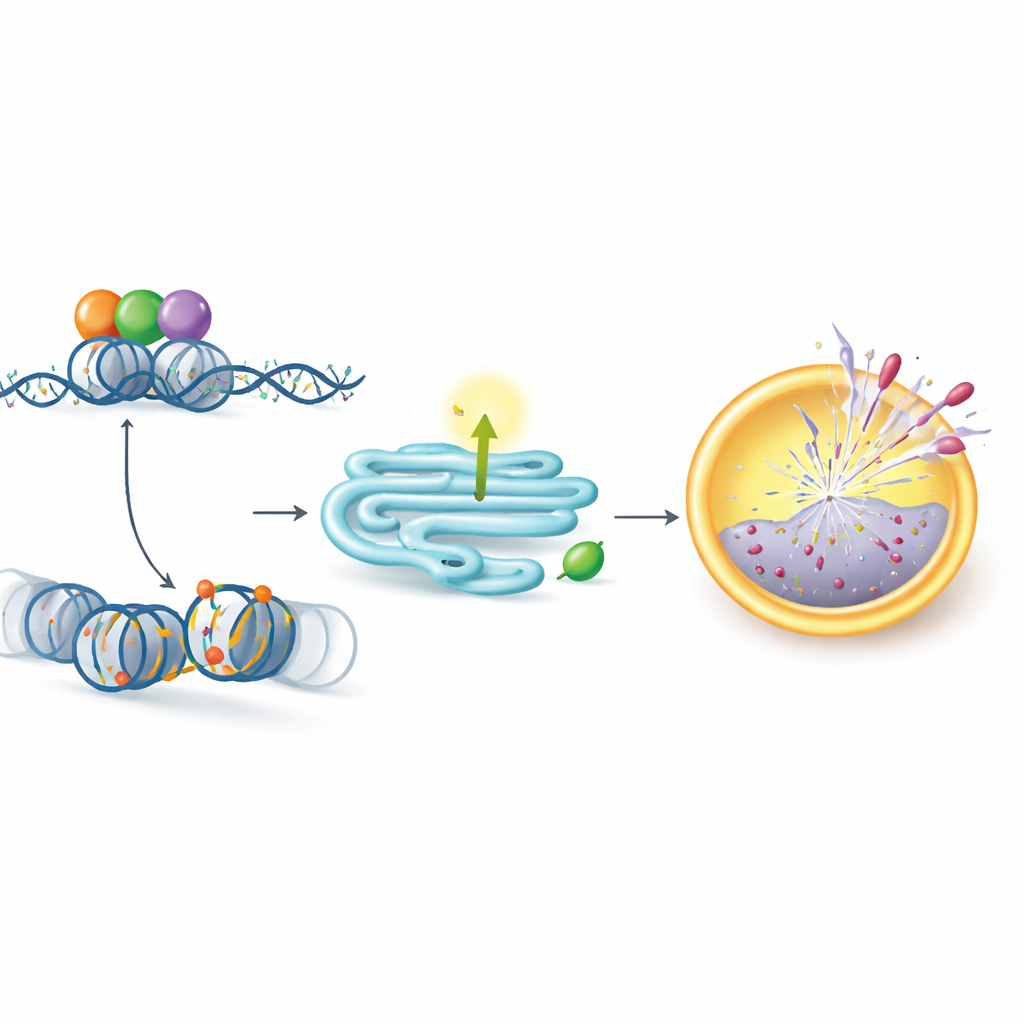
Un papel de andamiaje que reescribe la actividad génica
Sorprendentemente, KDM5C no actuó mediante su función química tradicional. En su lugar, se comportó como un andamio que reúne a otras dos proteínas: el regulador maestro del crecimiento MYC y la enzima CBP, que coloca una marca de “encendido” (acetilación) en las histonas en interruptores génicos clave. Los autores mostraron que KDM5C, MYC y CBP forman un complejo grande que se une cerca del gen PERK y aumenta la acetilación en ese sitio, activando PERK. Eliminar cualquiera de los tres socios redujo esta acetilación y disminuyó la expresión de PERK. Mutar una región específica de KDM5C, denominada dominio PHD2, perturbó su capacidad para ensamblar el complejo y activar PERK, aunque el resto de la proteína permaneciera intacto. Cabe destacar que un fármaco que bloquea la actividad habitual de las enzimas KDM5 no afectó a PERK, lo que subraya que esta vía de resistencia depende del papel estructural de KDM5C más que de su función enzimática clásica.
Qué podría significar esto para tratamientos futuros
Para las personas que conviven con mieloma múltiple, estos hallazgos señalan a KDM5C como un objetivo prometedor para combatir la recaída y la resistencia al bortezomib. Al ayudar a MYC y CBP a activar PERK y Nrf2, KDM5C permite que las células de mieloma soporten el severo estrés proteico que normalmente las mataría. Dado que este apoyo no depende de su química convencional, las terapias podrían necesitar ir más allá de los inhibidores enzimáticos simples y, en su lugar, eliminar la propia proteína KDM5C —por ejemplo, usando tecnologías emergentes de degradadores. Combinar tales enfoques con bortezomib podría debilitar las defensas de estrés del cáncer, mantener la eficacia del tratamiento por más tiempo y, en última instancia, mejorar los resultados para los pacientes.
Cita: Lu, P., Shangguan, W., Qian, W. et al. Noncanonical role of KDM5C in conferring bortezomib resistance via the PERK‒Nrf2 axis in multiple myeloma. Cell Death Dis 17, 339 (2026). https://doi.org/10.1038/s41419-026-08591-7
Palabras clave: mieloma múltiple, resistencia a bortezomib, KDM5C, vía PERK Nrf2, regulación epigenética