Clear Sky Science · it
Ruolo non canonico di KDM5C nella conferimento della resistenza al bortezomib tramite l’asse PERK‒Nrf2 nel mieloma multiplo
Perché questo è importante per pazienti e famiglie
Il mieloma multiplo è un tumore del sangue che è diventato molto più trattabile grazie ai farmaci moderni, in particolare l’inibitore del proteasoma bortezomib. Tuttavia molti pazienti vanno incontro a recidiva perché le cellule tumorali sviluppano resistenza al farmaco. Questo studio rivela un meccanismo finora non riconosciuto con cui le cellule del mieloma si proteggono dal bortezomib, incentrato su una proteina chiamata KDM5C. Comprendere questo stratagemma di sopravvivenza nascosto indica nuove strategie per mantenere l’efficacia del trattamento più a lungo.
Un problema di stress all’interno delle cellule produttrici di anticorpi
Il mieloma origina dalle plasmacellule, le “fabbriche” di anticorpi dell’organismo. Poiché producono enormi quantità di proteine, queste cellule sollecitano costantemente un compartimento cellulare chiamato reticolo endoplasmatico, che ripiega e processa le proteine neoformate. Quando il carico di lavoro diventa eccessivo, viene attivato un sistema protettivo noto come risposta alle proteine mal ripiegate (unfolded protein response). Il bortezomib sfrutta questa vulnerabilità bloccando la degradazione delle proteine, sovraccaricando ulteriormente il sistema e spingendo le cellule del mieloma verso uno stress letale. Tuttavia le cellule tumorali possono riprogrammare questa macchina di gestione dello stress per sopravvivere. Gli autori hanno ipotizzato che KDM5C, una proteina che di norma modifica le proteine associate al DNA per controllare l’attività genica, potesse essere uno degli interruttori chiave in questa riorganizzazione.
Una proteina che predice malattia aggressiva e scarsa risposta al farmaco
Analizzando ampi set di dati di pazienti e campioni di midollo osseo, i ricercatori hanno scoperto che i livelli di KDM5C erano molto più elevati nelle cellule del mieloma rispetto alle cellule normali. I pazienti i cui tumori esprimevano più KDM5C avevano maggior probabilità di presentare malattia avanzata, di recidivare dopo il trattamento e di avere una sopravvivenza complessiva più breve. In linee cellulari di mieloma rese resistenti al bortezomib, KDM5C risultava fortemente aumentata. Quando KDM5C veniva ridotta o eliminata in queste cellule, la loro crescita rallentava e diventavano nettamente più sensibili al bortezomib, sia in coltura che in modelli tumorali murini. Queste osservazioni collocano KDM5C sia come motore della progressione del mieloma sia come marcatore molecolare della resistenza al bortezomib.
Come KDM5C costruisce un circuito di stress pro‑sopravvivenza
Per capire come KDM5C produca questo effetto, il gruppo ha esaminato quali geni cambiavano quando KDM5C veniva spenta. Molti appartenevano a vie che aiutano le cellule a fronteggiare lo stress nel reticolo endoplasmatico. Un gene, PERK, è emerso come particolarmente ridotto. PERK è un sensore sul reticolo endoplasmatico che, quando attivato, invia segnali a un fattore chiamato Nrf2, che a sua volta potenzia le difese antiossidanti e altri programmi di sopravvivenza. Lo studio ha mostrato che KDM5C è necessario per mantenere alti i livelli di PERK, permettendo una robusta attivazione di Nrf2. Quando KDM5C veniva rimosso, i livelli di PERK calavano, la segnalazione di Nrf2 si indeboliva e le cellule del mieloma erano meno in grado di contrastare lo stress e venivano uccise più facilmente dal bortezomib. Ripristinare PERK nelle cellule carenti di KDM5C recuperava sia l’attività di Nrf2 sia la crescita cellulare, dimostrando che PERK è un collegamento cruciale tra KDM5C e la resistenza al farmaco.
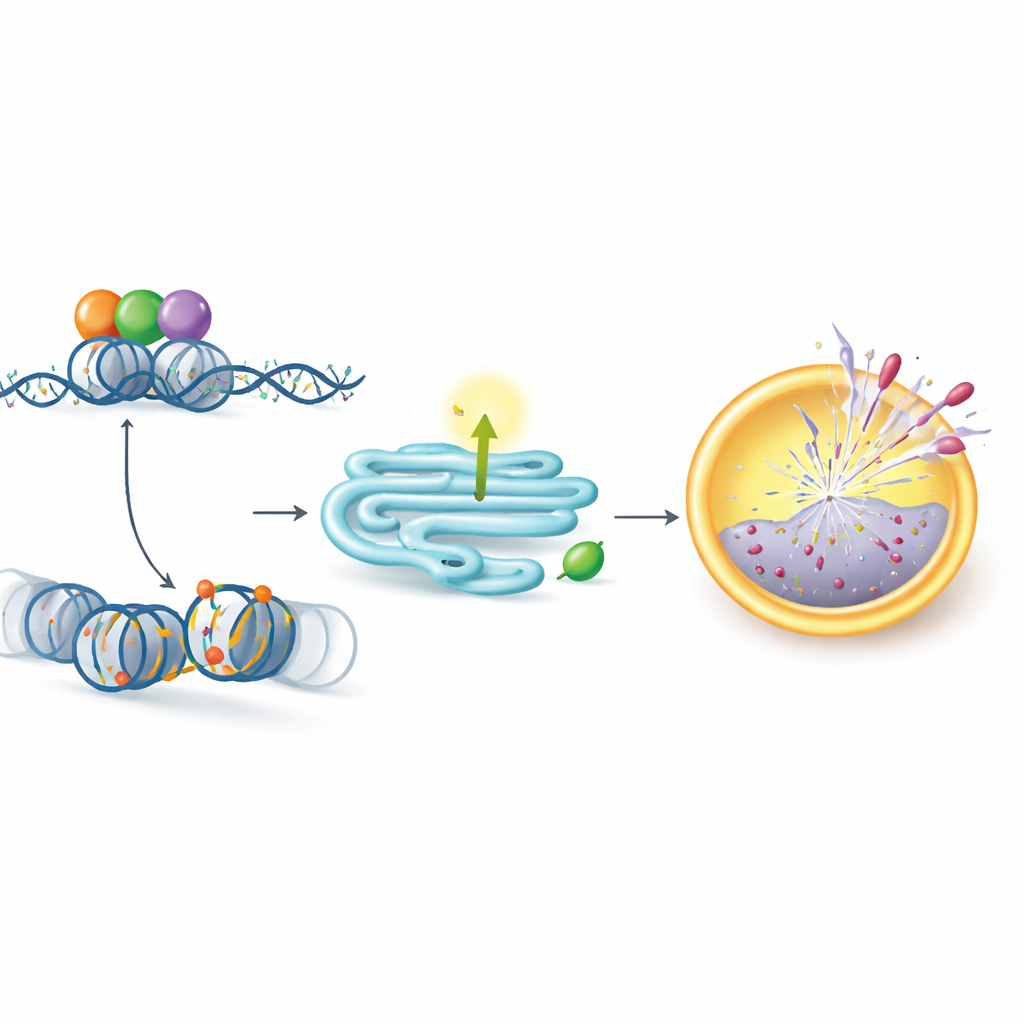
Un ruolo di impalcatura che riscrive l’attività genica
Sorprendentemente, KDM5C non agiva tramite la sua funzione chimica tradizionale. Piuttosto, si comportava come una impalcatura che mette insieme due altre proteine: il principale regolatore della crescita MYC e l’enzima CBP, che pone un marchio di “accensione” (acetilazione) sulle proteine istoniche in corrispondenza di interruttori genici chiave. Gli autori hanno dimostrato che KDM5C, MYC e CBP formano un grande complesso che si lega vicino al gene PERK e aumenta l’acetilazione in questo sito, attivando PERK. Rimuovere uno qualsiasi dei tre partner riduceva questa acetilazione e abbassava l’espressione di PERK. La mutazione di una regione specifica di KDM5C, chiamata dominio PHD2, comprometteva la sua capacità di assemblare il complesso e di attivare PERK, sebbene il resto della proteina rimanesse intatto. È notevole che un farmaco che blocca l’attività enzimica abituale delle chinasi KDM5 non influenzasse PERK, sottolineando che questa via di resistenza dipende dal ruolo strutturale di KDM5C piuttosto che dalla sua funzione enzimatica classica.
Cosa può significare per i trattamenti futuri
Per le persone che vivono con il mieloma multiplo, questi risultati puntano a KDM5C come a un nuovo bersaglio promettente per combattere le recidive e la resistenza al bortezomib. Facilitando a MYC e CBP l’accensione di PERK e Nrf2, KDM5C permette alle cellule del mieloma di superare lo stress proteico grave che normalmente le ucciderebbe. Poiché questo supporto non si basa sulla chimica convenzionale della proteina, le terapie potrebbero dover andare oltre i semplici inibitori enzimatici e mirare invece a eliminare la proteina KDM5C stessa—for example, utilizzando le nuove tecnologie degradative emergenti. Combinare tali approcci con il bortezomib potrebbe indebolire le difese antistress del tumore, prolungare l’efficacia del trattamento e, in definitiva, migliorare gli esiti per i pazienti.
Citazione: Lu, P., Shangguan, W., Qian, W. et al. Noncanonical role of KDM5C in conferring bortezomib resistance via the PERK‒Nrf2 axis in multiple myeloma. Cell Death Dis 17, 339 (2026). https://doi.org/10.1038/s41419-026-08591-7
Parole chiave: mieloma multiplo, resistenza al bortezomib, KDM5C, via PERK Nrf2, regolazione epigenetica