Clear Sky Science · ar
دور غير تقليدي لـ KDM5C في منح مقاومة لبورتزوميب عبر محور PERK‒Nrf2 في المايلوما المتعددة
لماذا يهم هذا للمرضى والعائلات
المايلوما المتعددة هي نوع من سرطانات الدم أصبح قابلاً للعلاج بدرجة أكبر بفضل الأدوية الحديثة، لا سيما مثبط البروتيازوم بورتزوميب. ومع ذلك، يعاود المرضى الانتكاس في كثير من الأحيان لأن خلايا السرطان تتعلّم مقاومة الدواء. تكشف هذه الدراسة عن آلية لم تكن معروفة سابقاً تستخدمها خلايا المايلوما لتحمي نفسها من بورتزوميب، ويرتكز ذلك على بروتين يُدعى KDM5C. فهم هذه الحيلة الخفية للبقاء يشير إلى استراتيجيات جديدة للحفاظ على فعالية العلاج لفترة أطول.
مشكلة توتر داخل خلايا صناعة الأجسام المضادة
تنشأ المايلوما من الخلايا البلازمية، مصانع الأجسام المضادة في الجسم. وبسبب إنتاجها كميات ضخمة من البروتين، تعاني هذه الخلايا باستمرار من ضغط على مقصورة خلوية تُسمى الشبكة الإندوبلازمية، التي تطوي وتعالج البروتينات الجديدة. عندما يصبح عبء العمل ثقيلاً جداً، يُفعَّل نظام وقائي يعرف باسم استجابة البروتين غير المطوي. يستغل بورتزوميب هذه النقطة الضعيفة عن طريق حجب تحطيم البروتين، مما يزيد التحميل على النظام ويدفع خلايا المايلوما إلى ضغوط مميتة. ومع ذلك، يمكن للخلايا السرطانية إعادة توصيل هذه الآلية لمواجهة الضغوط والبقاء. ظنّ المؤلفون أن KDM5C، وهو بروتين عادةً يغيّر بروتينات مرتبطة بالحمض النووي للتحكم بنشاط الجينات، قد يكون واحداً من مفاتيح هذا الإصلاح.
بروتين يتنبّأ بمرض عدواني واستجابة دوائية ضعيفة
باستخدام مجموعات بيانات كبيرة من المرضى وعينات نخاع العظم، وجد الباحثون أن مستويات KDM5C كانت أعلى بكثير في خلايا المايلوما مقارنة بالخلايا الطبيعية. كان المرضى الذين أعربت أورامهم عن مستويات أعلى من KDM5C أكثر عرضة لوجود مرض متقدم، وللانتكاس بعد العلاج، وللعيش لفترة أقصر إجمالاً. في خطوط خلايا المايلوما المعدّة مخبرياً لتكون مقاومة لبورتزوميب، ارتفع KDM5C بشكل قوي. عندما قلّل الباحثون من KDM5C أو حذفوه من هذه الخلايا، تباطأ نموها وأصبحت أكثر حساسية بكثير لبورتزوميب، سواء في أطباق الزرع أو في نماذج الورم بالفئران. تضع هذه الملاحظات KDM5C كسائق لتقدم المايلوما وكمؤشر جزيئي لمقاومة بورتزوميب.
كيف يبني KDM5C دائرة ضغط داعمة للبقاء
لمعرفة كيف يؤثر KDM5C، فحص الفريق الجينات التي تغيرت عند إيقاف KDM5C. كان العديد منها جزءاً من مسارات تساعد الخلايا على التعامل مع الضغوط في الشبكة الإندوبلازمية. برز جين واحد، PERK، على أنه انخفض بشكل خاص. يعتبر PERK مستقبلًا على الشبكة الإندوبلازمية، فعند تنشيطه يرسل إشارات إلى عامل يُدعى Nrf2، والذي بدوره يعزز الدفاعات المضادة للأكسدة وبرامج بقاء أخرى. أظهرت الدراسة أن KDM5C ضروري للحفاظ على مستويات عالية من PERK، مما يسمح بتفعيل قوي لـ Nrf2. عندما أُزيل KDM5C، انخفضت مستويات PERK، ضعفت إشارة Nrf2، وأصبحت خلايا المايلوما أقل قدرة على مواجهة الضغوط وأكثر عرضة للموت بفعل بورتزوميب. إعادة PERK في الخلايا الناقصة لـ KDM5C أعادت نشاط Nrf2 ونمو الخلايا، مما يثبت أن PERK حلقة حاسمة تربط بين KDM5C والمقاومة الدوائية.
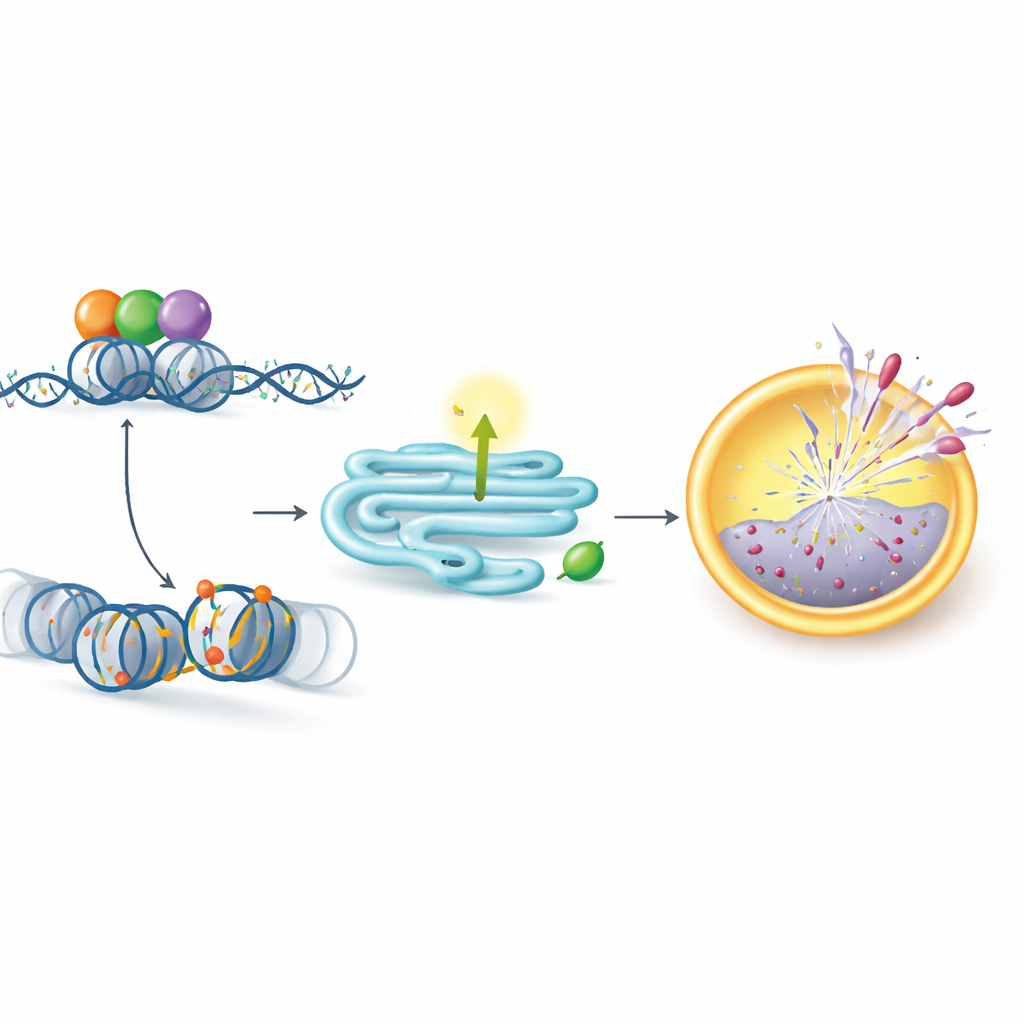
دور كسقالة يعيد كتابة نشاط الجينات
بشكل مفاجئ، لم يعمل KDM5C من خلال وظيفته الكيميائية التقليدية. بل تصرّف كسقالة تجمع بين بروتينين آخرين: المنظم الرئيسي للنمو MYC والإنزيم CBP، الذي يضع علامة "تشغيل" (أسيتلة) على بروتينات الهيستون عند مفاتيح جينية رئيسية. أظهر المؤلفون أن KDM5C وMYC وCBP يشكلون مركباً كبيراً يرتبط بالقرب من جين PERK ويزيد الأسيتلة في هذا الموقع، مما يُشغّل PERK. إزالة أي من الشركاء الثلاثة خفّضت هذه الأسيتلة وانخفضت تعبيرات PERK. طفرَة في منطقة محددة من KDM5C تسمى دومين PHD2 عطّلت قدرته على تجميع المركب وتنشيط PERK، مع بقاء باقي البروتين سليماً. واللافت أن دواءً يثبط النشاط المعتاد لإنزيمات KDM5 لم يؤثر على PERK، مما يبرز أن هذا المسار المقاوم يعتمد على الدور البنيوي لـ KDM5C لا على وظيفته الإنزيمية الكلاسيكية.
ماذا قد يعني هذا للعلاج المستقبلي
بالنسبة للأشخاص المصابين بالمايلوما المتعددة، تُظهر هذه النتائج أن KDM5C هدف واعد لمكافحة الانتكاس ومقاومة بورتزوميب. عبر مساعدة MYC وCBP على تشغيل PERK وNrf2، يتيح KDM5C لخلايا المايلوما تحمل ضغوط البروتين الشديدة التي عادةً ما تقتلها. وبما أن هذا الدعم لا يعتمد على كيميائه التقليدية، قد تحتاج العلاجات أن تتجاوز مثبطات الإنزيم البسيطة وتستهدف إزالة بروتين KDM5C نفسه — على سبيل المثال باستخدام تقنيات التحلل الناشئة. قد يؤدي دمج مثل هذه الاستراتيجيات مع بورتزوميب إلى إضعاف دفاعات السرطان ضد الضغوط، وإطالة فعالية العلاج، وتحسين النتائج النهائية للمرضى.
الاستشهاد: Lu, P., Shangguan, W., Qian, W. et al. Noncanonical role of KDM5C in conferring bortezomib resistance via the PERK‒Nrf2 axis in multiple myeloma. Cell Death Dis 17, 339 (2026). https://doi.org/10.1038/s41419-026-08591-7
الكلمات المفتاحية: المايلوما المتعددة, مقاومة لبورتزوميب, KDM5C, مسار PERK Nrf2, التنظيم فوق الجيني