Clear Sky Science · zh
将低甲基化药物与现成的靶向CD70的嵌合抗原受体工程化自然杀伤T细胞协同用于急性髓系白血病治疗
将机体防御转向血液癌
急性髓系白血病是一种进展迅速的血液癌,老年患者尤其致命,且许多患者无法耐受强烈的化疗。本研究探讨了一种两步策略:先用现有药物“软化”白血病细胞,随后用一种新型的现成免疫细胞疗法将其清除,展示了未来治疗如何在更强效的同时更安全的可能路径。
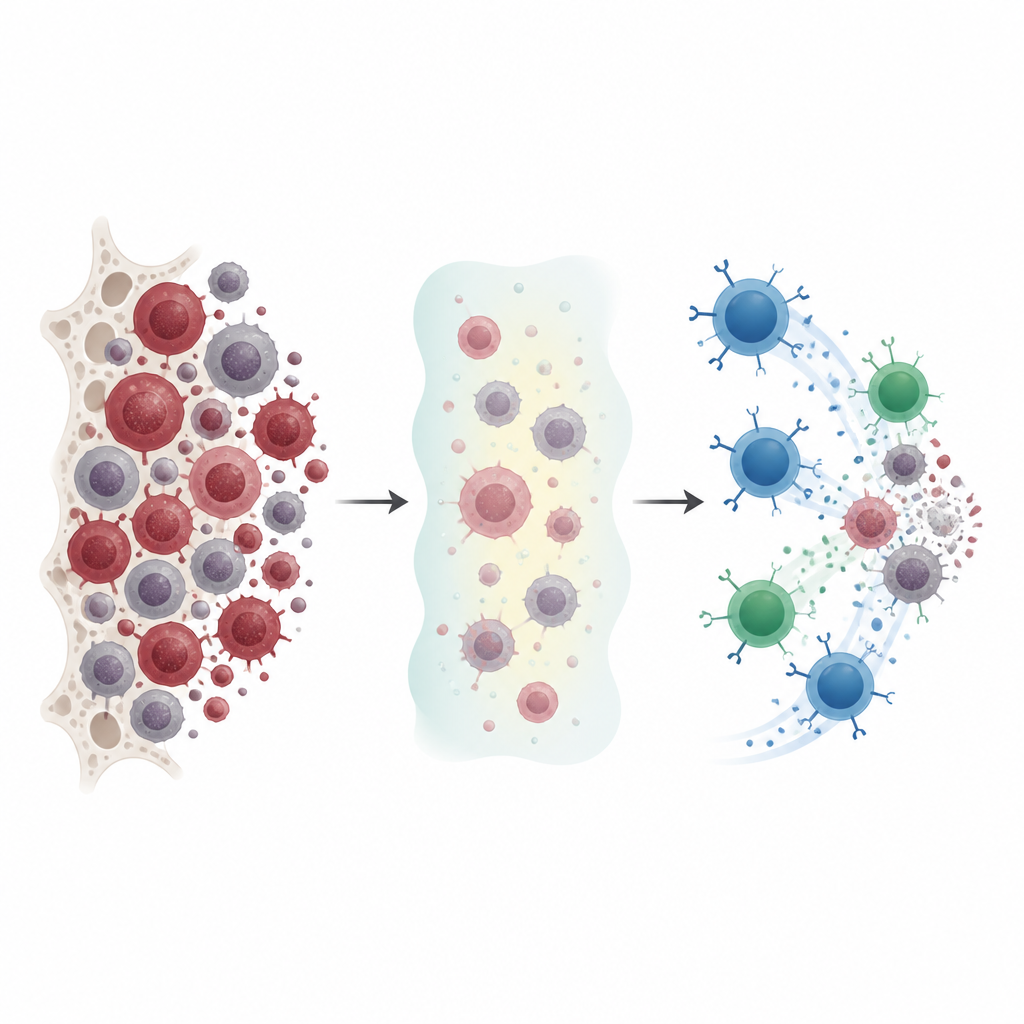
为何现有治疗仍不足
医生常用一类称为低甲基化剂的药物治疗急性髓系白血病,这些药物通过微妙地重编程癌细胞而非直接摧毁它们来发挥作用。这些药物可以减缓病情并帮助免疫系统识别肿瘤细胞,但缓解常不完全且许多患者会复发。作者研究了这些药物如何改变白血病细胞的表面,并探讨能否将这些变化转化为可被定制免疫疗法利用的弱点。
让白血病细胞更易被识别
在培养皿中的白血病细胞系和小鼠模型中,研究者发现长期低剂量的低甲基化剂治疗一贯使肿瘤细胞对免疫系统“更可见”。这些药物提高了CD70和CD1d的表达,以及一组天然杀伤细胞易识别的应激标志物。即便起初CD70表达很低的白血病细胞,经药物处理后也能被诱导出更多CD70。在小鼠体内,相同药物既减缓了白血病生长,又在骨髓、肝脏和肺中增强了这些免疫可见的标志,表明这种处理改变了活体中肿瘤的表型,而不只是实验室条件下的现象。
构建现成的“智能”杀伤细胞
为利用这一新出现的脆弱性,团队工程化了一类称为不变型自然杀伤T细胞的特殊免疫细胞。一种产品AlloCAR70‑NKT由脐带血干细胞在分阶段培养体系中生成,另一种则由成年供者血细胞制备。两者都配备了识别CD70的受体,并被设计为分泌生长因子IL‑15以帮助其持续存活。来自脐带血的细胞达到了很高的纯度,显示出均一的受体表达,且可从单个供者单位大量生产,暗示了向许多患者提供冷冻、即用剂量的可行路径。
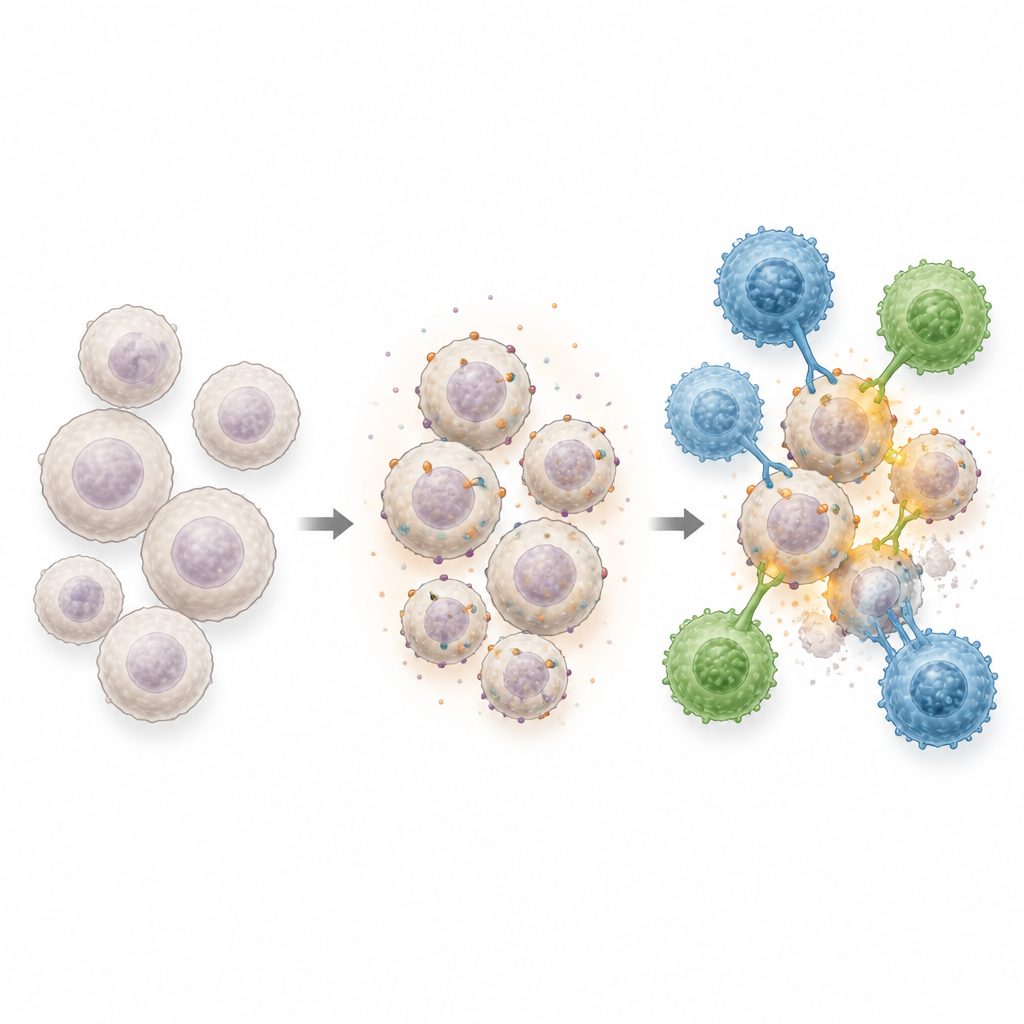
联合疗法如何攻击白血病
在体外实验中,这些工程化细胞能有效杀死表达CD70或CD1d的白血病细胞,且脐带血来源的细胞还能通过天然杀伤受体发起攻击,从而提供三种独立的识别途径。当白血病细胞先用低甲基化药物预处理后,杀伤在各种细胞类型间变得更为高效,尤其是对那些起初CD70含量很低的肿瘤。在带有侵袭性白血病的小鼠模型中,药物处理随后给予AlloCAR70‑NKT细胞的组合能够清除疾病、延长生存并诱导强烈的抗肿瘤免疫反应,即便在单独使用工程化细胞疗法效果较差的情况下亦然。重要的是,这些工程化细胞未引发常限制其他细胞疗法的严重并发症,如移植物抗宿主病或细胞因子风暴。
这对患者可能意味着什么
对非专业读者而言,关键结论是:一类熟悉的白血病药物可用于在癌细胞上描绘更清晰的靶标,而一种新型预制免疫细胞产品可从多个角度锁定这些靶点。在动物实验中,这种两步打击不仅减缓了白血病,在某些情况下还能在不产生传统工程化T细胞所见严重副作用的前提下将其清除。尽管仍需在患者样本和临床试验中做进一步工作,该研究表明将低甲基化药物与现成的工程化自然杀伤T细胞配对,可能为急性髓系白血病患者提供一种更精确且更易耐受的治疗选择。
引用: Li, YR., Shen, X., Chen, Y. et al. Synergizing hypomethylating agents with off-the-shelf CD70-targeted chimeric antigen receptor-engineered natural killer T cells for the treatment of acute myeloid leukemia. Leukemia 40, 880–893 (2026). https://doi.org/10.1038/s41375-026-02930-5
关键词: 急性髓系白血病, CAR‑NKT 细胞, CD70, 低甲基化剂, 免疫疗法