Clear Sky Science · de
Synergie zwischen hypomethylierenden Wirkstoffen und gebrauchsfertigen, auf CD70 gerichteten chimären Antigenrezeptor‑konstruierten natürlichen Killer‑T‑Zellen zur Behandlung der akuten myeloischen Leukämie
Die Abwehrkräfte des Körpers gegen eine Blutkrebserkrankung wenden
Die akute myeloische Leukämie ist ein rasch verlaufender Blutkrebs, der besonders bei älteren Menschen tödlich sein kann; viele Patienten vertragen keine intensive Chemotherapie. Diese Studie untersucht eine zweigleisige Strategie: Zunächst werden Leukämiezellen mit etablierten Medikamenten »weichgeklopft«, anschließend werden sie mit einer neuen Art gebrauchsfertiger Immunzellen therapiert. Das bietet einen Ausblick darauf, wie künftige Behandlungen sowohl wirksamer als auch sicherer werden könnten.
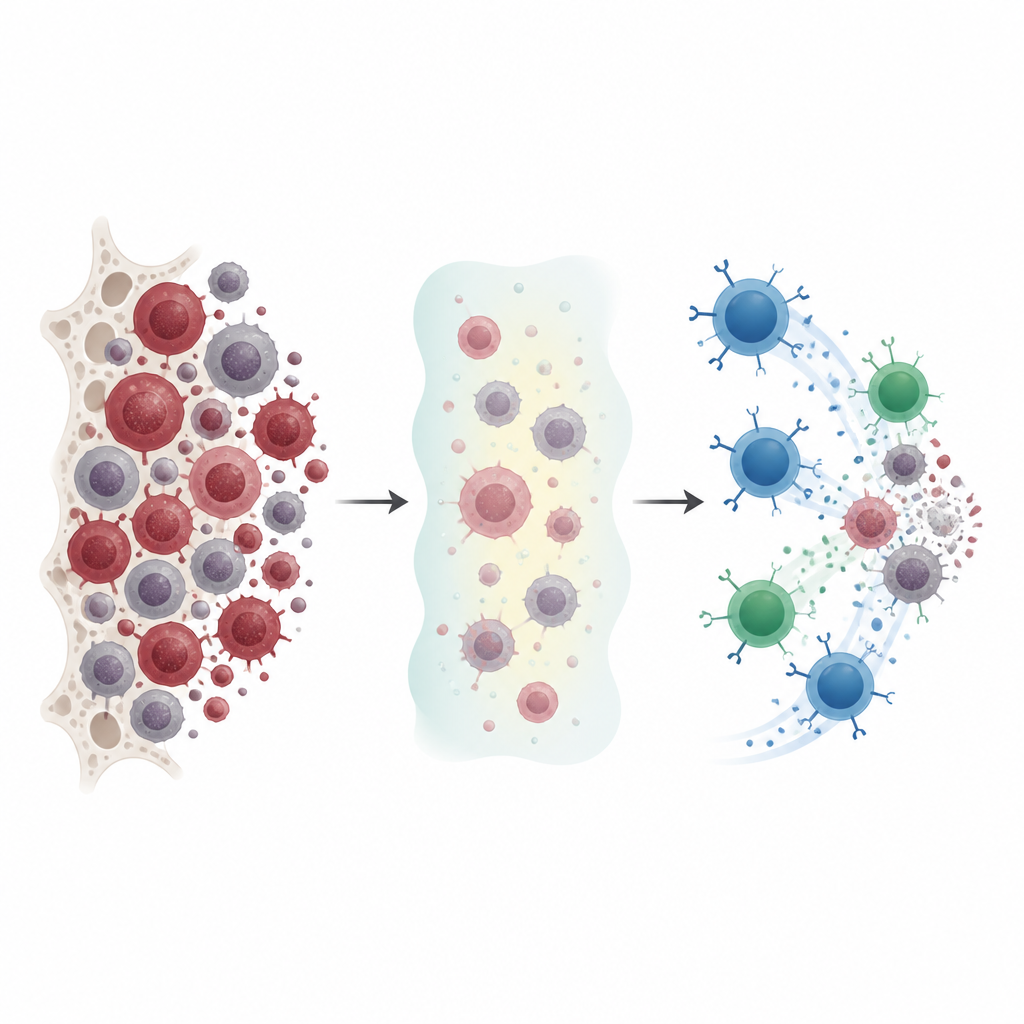
Warum aktuelle Behandlungen nicht ausreichen
Ärzte behandeln die akute myeloische Leukämie oft mit sogenannten hypomethylierenden Wirkstoffen, die Krebszellen eher umprogrammieren als sie radikal zu zerstören. Diese Medikamente können das Fortschreiten verlangsamen und das Immunsystem dabei unterstützen, Tumorzellen zu erkennen, doch die Remissionen sind unvollständig und viele Patienten erleiden ein Rezidiv. Die Autorinnen und Autoren untersuchten, wie diese Wirkstoffe die Oberfläche von Leukämiezellen verändern, und fragten, ob sich diese Veränderungen als Schwachstelle nutzen lassen, die eine gezielte Immuntherapie ausnutzen könnte.
Leukämiezellen leichter erkennbar machen
An Zelllinien und in Mäusen fanden die Forschenden, dass eine langfristige, niedrig dosierte Behandlung mit hypomethylierenden Wirkstoffen die Tumorzellen beständig »sichtbarer« für das Immunsystem machte. Die Medikamente erhöhten die Menge an CD70 und CD1d sowie die Expression mehrerer Stressmarker, die natürliche Killerzellen anlocken. Selbst Leukämiezellen mit zunächst sehr wenig CD70 konnten nach der Arzneimittelexposition deutlich mehr davon zeigen. In Mäusen verlangsamten die gleichen Wirkstoffe das Leukämie‑Wachstum und erhöhten diese immun‑sichtbaren Marker in Knochenmark, Leber und Lunge, was darauf hindeutet, dass die Behandlung die Tumorumgebung im lebenden Organismus und nicht nur im Reagenzglas verändert.
Gebrauchsfertige intelligente Killerzellen entwickeln
Um diese neue Verwundbarkeit auszunutzen, konstruierten die Forscher spezielle Immunzellen, sogenannte invariant natürliche Killer‑T‑Zellen. Ein Produkt, AlloCAR70‑NKT genannt, wurde aus Nabelschnurblutstammzellen in einem mehrstufigen Kultursystem gezüchtet, während ein zweites Produkt aus dem Blut erwachsener Spender hergestellt wurde. Beide wurden mit einem Rezeptor ausgestattet, der CD70 erkennt, und so programmiert, dass sie den Wachstumsfaktor IL‑15 abgeben, um ihr Durchhaltevermögen zu unterstützen. Die aus Nabelschnurblut gewonnenen Zellen erreichten sehr hohe Reinheit, zeigten eine einheitliche Rezeptorexpression und ließen sich in großer Zahl aus einer einzigen Spender‑Einheit herstellen, was einen praktischen Weg zu gefrorenen, sofort einsetzbaren Dosen für viele Patienten andeutet.
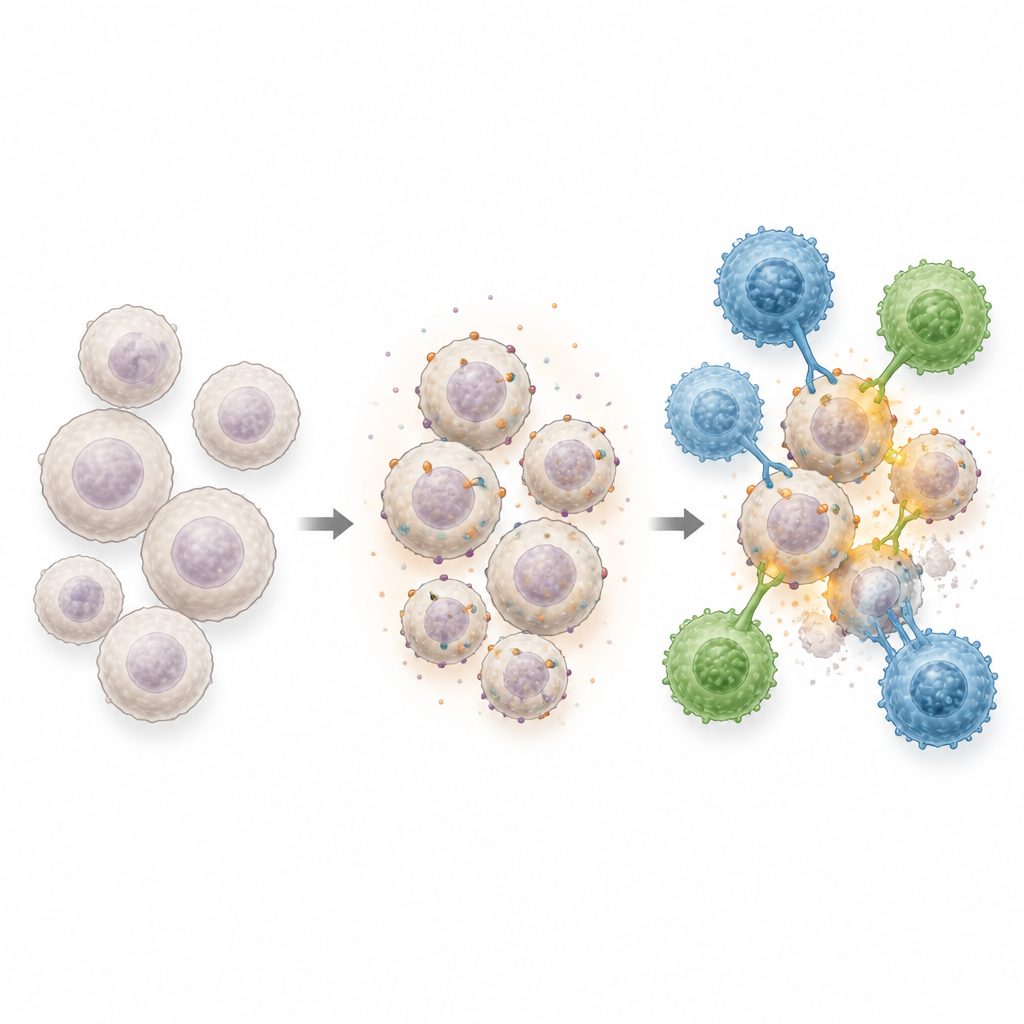
Wie die Kombinationsbehandlung die Leukämie angreift
In Labortests töteten die gentechnisch veränderten Zellen zuverlässig Leukämiezellen, die CD70 oder CD1d zeigten; die aus Nabelschnurblut stammenden Zellen konnten außerdem über natürliche Killerrezeptoren angreifen und verfügten damit über drei verschiedene Erkennungswege. Wenn Leukämiezellen zuvor mit hypomethylierenden Wirkstoffen präpariert wurden, wurde das Abtöten deutlich effizienter, insbesondere bei Tumoren, die anfangs wenig CD70 aufwiesen. In Mausmodellen mit aggressiver Leukämie beseitigte die Kombination aus medikamentöser Vorbehandlung gefolgt von AlloCAR70‑NKT‑Zellen die Erkrankung, verlängerte das Überleben und löste eine starke antitumorale Immunantwort aus – selbst in Fällen, in denen die gentechnisch veränderten Zellen allein weniger wirksam waren. Wichtig ist: Diese konstruierten Zellen lösten keine gefährlichen Komplikationen wie Graft‑versus‑Host‑Erkrankungen oder Zytokinstürme aus, die andere Zelltherapien oft einschränken.
Was das für Patienten bedeuten könnte
Die Kernaussage für Laien ist: Eine vertraute Medikamentenklasse kann gezielt klarere Ziele auf Krebszellen sichtbar machen, während ein neues, vorgefertigtes Immunzellprodukt diese Ziele aus mehreren Richtungen anvisiert. In Tiermodellen verlangsamte dieser Zwei‑Schritte‑Ansatz die Leukämie und beseitigte sie in einigen Fällen, ohne die schweren Nebenwirkungen konventioneller gentechnisch veränderter T‑Zellen. Zwar sind weitere Untersuchungen an Patientenproben und klinische Studien notwendig, doch die Studie legt nahe, dass die Kombination von hypomethylierenden Wirkstoffen mit gebrauchsfertigen, gentechnisch veränderten natürlichen Killer‑T‑Zellen eine präzisere und besser verträgliche Behandlungsoption für Menschen mit akuter myeloischer Leukämie bieten könnte.
Zitation: Li, YR., Shen, X., Chen, Y. et al. Synergizing hypomethylating agents with off-the-shelf CD70-targeted chimeric antigen receptor-engineered natural killer T cells for the treatment of acute myeloid leukemia. Leukemia 40, 880–893 (2026). https://doi.org/10.1038/s41375-026-02930-5
Schlüsselwörter: akute myeloische Leukämie, CAR‑NKT‑Zellen, CD70, hypomethylierende Wirkstoffe, Immuntherapie