Clear Sky Science · ru
Синергия гипометилирующих препаратов с готовыми CD70-нацеленными химерными рецепторами в естественных киллерных T-клетках для лечения острого миелоидного лейкоза
Обращение защитных сил организма против рака крови
Острый миелоидный лейкоз — быстро прогрессирующий рак крови, особенно опасный у пожилых людей; многие пациенты не переносят интенсивную химиoterapiю. В этом исследовании предлагается двухэтапная стратегия: сначала «размягчить» лейкозные клетки с помощью уже известных препаратов, а затем атаковать их новым типом готовой к использованию терапии иммунных клеток, что даёт представление о том, как будущие лечения могут стать одновременно более мощными и безопасными.
Почему текущих методов недостаточно
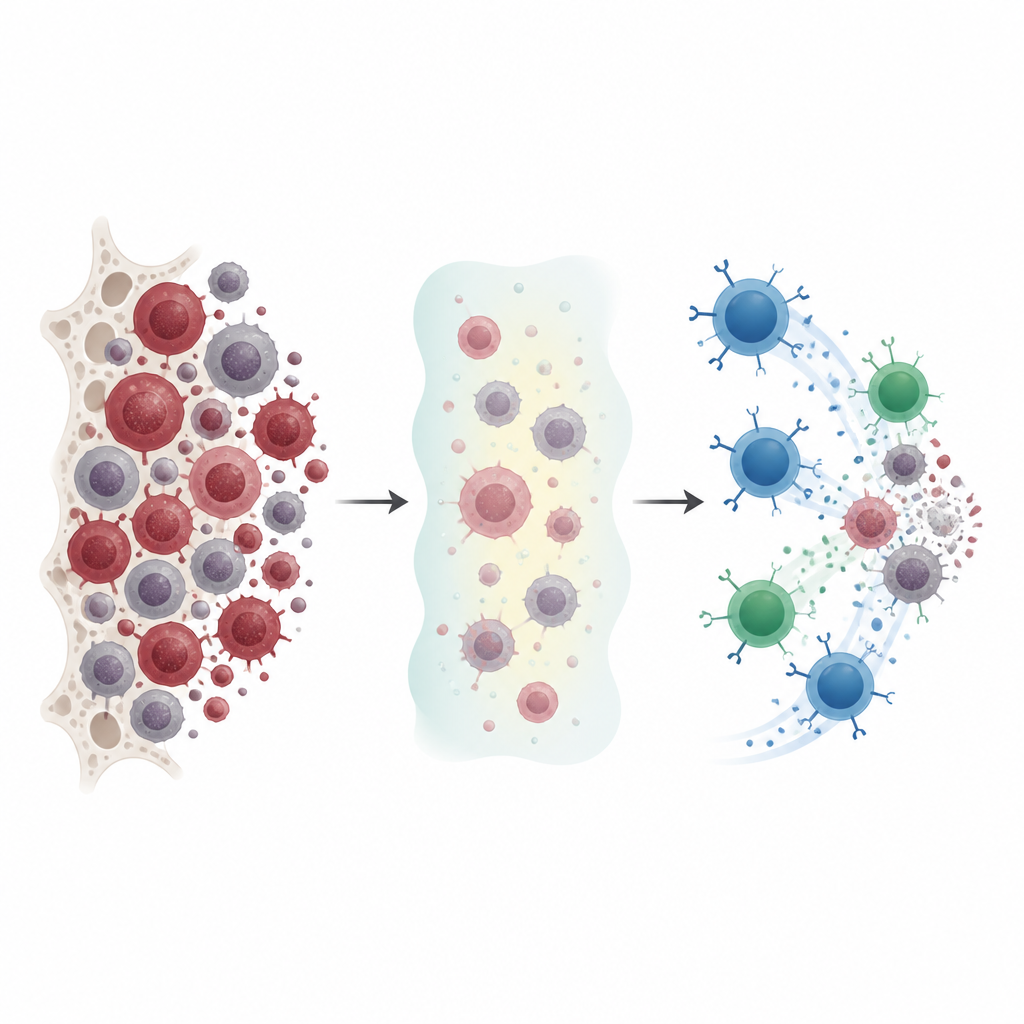
Врачи часто лечат острый миелоидный лейкоз препаратами, называемыми гипометилирующими агентами: они не уничтожают клетки грубо, а тонко перепрограммируют их. Эти лекарства могут замедлять развитие болезни и помогать иммунной системе распознавать опухолевые клетки, но ремиссии остаются неполными, и многие пациенты рецидивируют. Авторы изучили, как эти препараты меняют поверхность лейкозных клеток, и поставили вопрос, можно ли превратить эти изменения в уязвимость, которую целевая иммунотерапия сможет использовать.
Делая лейкозные клетки легче распознаваемыми
При работе с культурами лейкозных клеток и в экспериментах на мышах исследователи обнаружили, что долговременная низкодозная терапия гипометилирующими агентами последовательно делает опухолевые клетки более «видимыми» для иммунной системы. Препараты повышали уровни CD70 и CD1d, а также набор стрессовых маркеров, к которым склонны привлекаться натуральные киллерные клетки. Даже клетки лейкоза с очень малым исходным уровнем CD70 после обработки могли начать выражать его в значительно большем количестве. В моделях на мышах те же препараты замедляли рост лейкоза и усиливали эти иммунно‑видимые метки на раковых клетках в костном мозге, печени и лёгких, что указывает на то, что лечение перестраивает ландшафт опухоли в живом организме, а не только в культурах.
Создание готовых «умных» киллерных клеток
Чтобы воспользоваться этой новой уязвимостью, команда создала специализированные иммунные клетки — инвариантные NKT‑клетки. Один продукт, названный AlloCAR70‑NKT, выращивали из стволовых клеток пуповинной крови в поэтапной системе культивирования, а второй изготовляли из донорской крови взрослых. Обе линии были оснащены рецептором, распознающим CD70, и запрограммированы на выделение фактора роста IL‑15 для повышения выживаемости. Клетки, полученные из пуповинной крови, отличались очень высокой чистотой, равномерным экспрессированием рецептора и могли быть произведены в большом количестве из одной донорской единицы, что указывает на практический путь к замороженным, готовым к применению дозам для множества пациентов.
Как эта комбо‑терапия атакует лейкоз
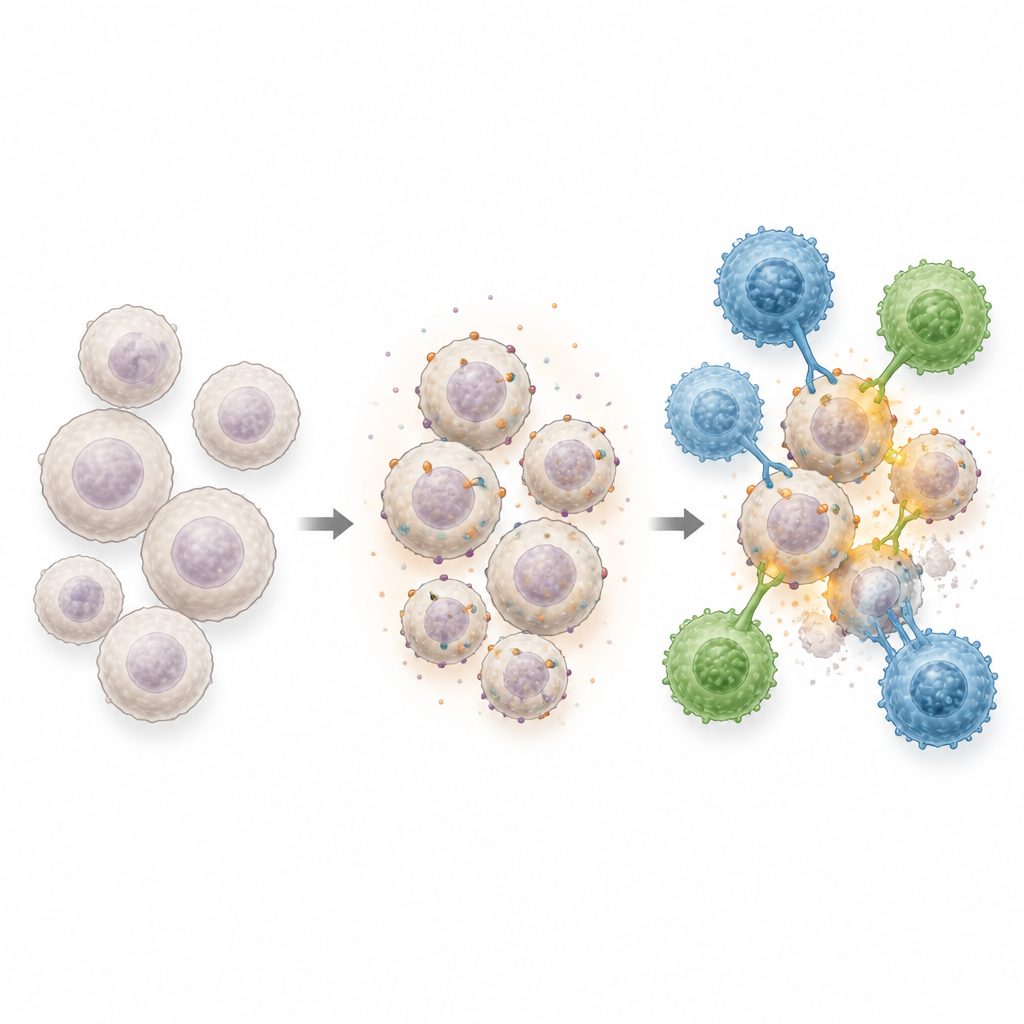
В лабораторных тестах инженерные клетки эффективно убивали лейкозные клетки, экспрессирующие CD70 или CD1d, а клетки из пуповинной крови могли также атаковать через естественные NK‑рецепторы, обеспечивая три отдельные механизма распознавания мишеней. Когда лейкозные клетки предварительно «готовили» гипометилирующими препаратами, эффективность уничтожения существенно возрастала во многих типах клеток, особенно в опухолях с изначально низким уровнем CD70. В моделях на мышах с агрессивным лейкозом сочетание лечения препаратом с последующим введением AlloCAR70‑NKT клеток устраняло болезнь, продлевало выживаемость и вызывало мощную противоопухолевую иммунную активность, даже в случаях, когда одни только инженерные клетки были менее эффективны. Важно, что эти инженерные клетки не вызывали опасных осложнений, таких как болезнь «трансплантат против хозяина» или цитокиновый шторм, которые часто ограничивают применение других клеточных терапий.
Что это может значить для пациентов
Для широкого круга читателей ключевая мысль такова: знакомый класс препаратов против лейкоза может использоваться для «окрашивания» более чётких мишеней на раковых клетках, а новый пред‑изготовленный продукт из иммунных клеток на нескольких уровнях нацеливается на эти мишени. В экспериментах на животных такое сочетание не только замедляло лейкоз, но в некоторых условиях и полностью его устраняло без тяжёлых побочных эффектов, характерных для традиционных инженерных T‑клеток. Хотя необходимы дальнейшие исследования на образцах пациентов и клинические испытания, работа указывает на то, что сочетание гипометилирующих препаратов с готовыми инженерными NKT‑клетками может предложить более точный и переносимый вариант лечения для людей с острым миелоидным лейкозом.
Цитирование: Li, YR., Shen, X., Chen, Y. et al. Synergizing hypomethylating agents with off-the-shelf CD70-targeted chimeric antigen receptor-engineered natural killer T cells for the treatment of acute myeloid leukemia. Leukemia 40, 880–893 (2026). https://doi.org/10.1038/s41375-026-02930-5
Ключевые слова: острый миелоидный лейкоз, CAR‑NKT клетки, CD70, гипометилирующие агенты, иммунотерапия