Clear Sky Science · tr
Rekonstrüktif kemik iskeleleri için çok ölçekli biyomekanik odaklı tasarım akışları
Kırık Kemiklerin Daha İyi İyileşmesine Yardımcı Olmak
Bir kemik kaza, hastalık veya cerrahi nedeniyle ağır hasar gördüğünde, vücut bazen boşluğu kendi başına onaramaz. Cerrahlar artık üç boyutlu “iskeletler” — gözenekli, süngerimsi destekler — implante edebiliyor; bunlar defekti doldurur ve yeni kemik oluşumunu teşvik eder. Bu makale, çoklu ölçeklerde mekanik ilkeleri kullanan yeni bir tasarım yaklaşımının, sadece kemiği bir arada tutmakla kalmayıp aynı zamanda hücrelere besin sağlamak ve kemik onaran hücrelere doğru fiziksel sinyalleri iletmek için nasıl daha akıllı iskeletler yarattığını açıklıyor.
Kemik İskeletlerinin Yapması Gerekenler
Geleneksel kemik greftleri, hastanın kendi kemiğinin parçalarının nakline dayanır; bu, ağrıya neden olabilir ve sınırlı kaynağa sahiptir. Mühendislik ürünü iskeletler bir alternatif sunar: bunlar, defekte yerleştirilen ve geçici olarak kemiğin doğal destek çerçevesi rolünü üstlenen, özel şekillendirilmiş implantlardır. Görevleri zordur. Eklem veya çenenin işlev görebilmesi için yük taşımalı, kan ve besinlerin derinlerdeki hücrelere ulaşmasına izin vermeli ve kök hücrelerin yara izi değil de kemik oluşturan hücrelere dönüşmesini sağlayan ince mekanik ipuçları sunmalıdır. Modern 3B baskı ve gelişmiş malzemeler, gözenek boyutu, şekli ve yöneliminin yüksek hassasiyetle kontrol edilmesine imkan vererek son derece kişiselleştirilmiş implantların önünü açar.
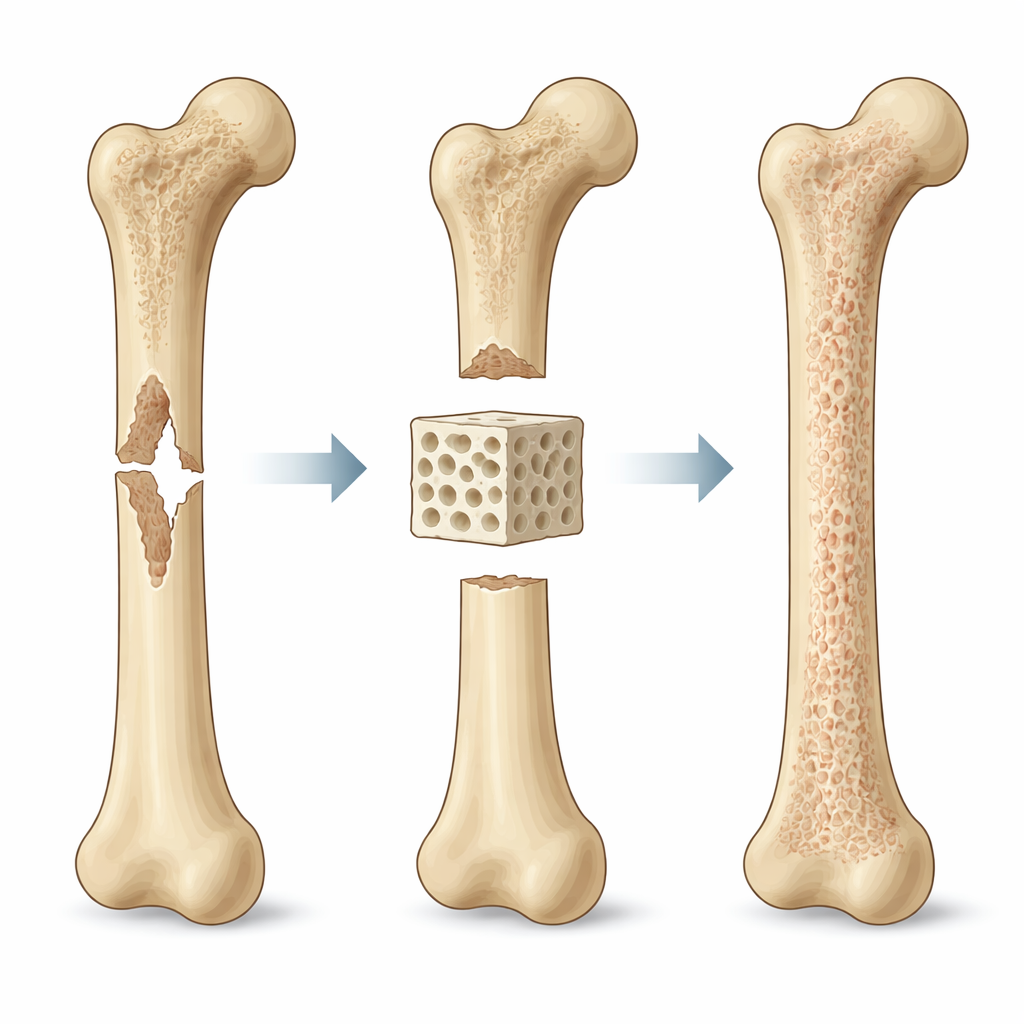
Soruna Büyükten Küçüğe Bakmak
Yazarlar, iskelet tasarımının üç bağlı ölçekte biyomekanik tarafından yönlendirilmesi gerektiğini öne sürüyor. “Makro” ölçekte — tüm kemik segmentinin boyutu — iskelet defekti köprülemeli ve çevreleyen kemikle kuvvetleri paylaşmalıdır. Çok yumuşaksa, küçük hareketler implantı gevşetebilir ve kemiğin yerine yumuşak doku oluşumunu teşvik edebilir. Çok sertse, doğal kemiği stresten koruyarak iyileşmeyi yavaşlatabilir. “Meso” ölçekte — gözenekler ve kanallar düzeyi — mimari, sıvı, oksijen ve hücrelerin yapı içinde ne kadar kolay hareket edebileceğini belirler. Daha büyük ve daha bağlantılı gözenekler taşımayı ve damar büyümesini iyileştirir, ancak aşırıya kaçılırsa iskeleti zayıflatır. “Mikro” ölçekte — bireysel hücrelerin çevresini hissettiği düzeyde — lokal gerilme, yüzey sertliği ve küçük akımlar hücrelerin nasıl tutunduğunu, şekil değiştirdiğini ve hangi doku tipini oluşturacaklarına nasıl karar verdiklerini etkiler.
Kemik Büyümesi İçin Tatlı Noktayı Bulmak
Deneyler ve bilgisayar modelleri, kemik hücrelerinin mekanik sinyaller belirli “pencereler” içinde düştüğünde en iyi yanıt verdiğini; tek bir mükemmel değerde değil, bir aralıkta tepki verdiklerini öne sürüyor. Çok az gerilme veya sıvı hareketi genellikle lifli, yara benzeri doku üretme eğilimindedir; çok fazlası hücrelere zarar verebilir veya erken iyileşmeyi bozabilir. Arada, kemik oluşumunun desteklendiği bir osteojenik pencere bulunur. Kesin aralıklar iyileşme aşamasına, vücut içindeki konuma ve hastanın durumuna bağlı olarak değişir, ancak kavram sağlamdır: iskeletler günlük yükler altında, içlerindeki hücrelerin büyük çoğunluğunu bu elverişli mekanik koşullara maruz bırakırken aynı zamanda yeterli dayanım ve sıvı taşımayı sağlamalıdır.
Adım Adım Bir Tasarım Akışı
Bu fikirleri pratiğe dökmek için makale dört aşamalı bir tasarım akışı özetliyor. Birinci olarak, klinisyenler ve mühendisler hasta taramalarını, defekt şekillerini ve beklenen yükleri iskelet için hedefler ve sınırlar — örneğin hedef sertlik, izin verilen porozite ve istenen kemik ve damar büyümesi — olarak çevirir. İkinci olarak, bilgisayarlar malzeme, gözenek boyutu ve iç desenleri değiştirerek birçok sanal iskelet tasarımı üretir ve ardından her birinin kuvvetleri nasıl taşıdığını, sıvıyı nasıl hareket ettirdiğini ve hücre ölçeğindeki ortamı nasıl şekillendirdiğini simüle eder. Üçüncü olarak, en umut verici adaylar laboratuvarda ve hayvan modellerinde üretilip test edilir; gerçek davranışın öngörülerle uyuşup uyuşmadığı ve hücrelerin gerçekten kemik oluşturup oluşturmadığı kontrol edilir. Son olarak, çok amaçlı optimizasyon teknikleri, güç ile geçirgenlik gibi çelişen ihtiyaçlar arasında en iyi dengeyi sağlayan tasarımları belirlemeye yardımcı olur ve bunlar belirli klinik durumlar için seçilir.
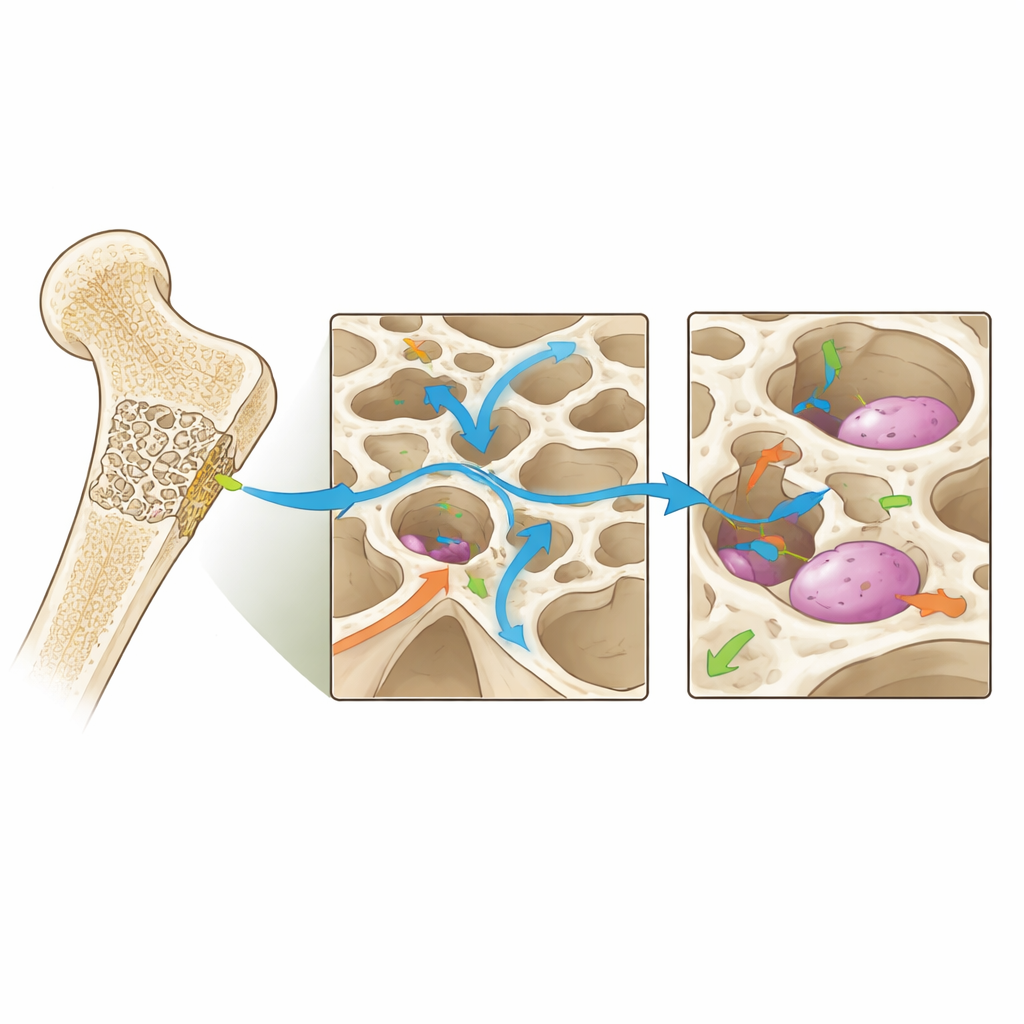
Daha Akıllı İmplantlara Bakış
Derleme ayrıca yapay zekâyı geniş tasarım alanlarında arama yapmak için kullanma, kullanım koşullarına yanıt olarak sertliği değiştiren veya faktörler salan “akıllı” malzemeler ve belirli bir hastada implante edilen iskelet ile çevreleyen kemiğin zaman içinde birlikte nasıl evrildiğini izleyen dijital ikiz modelleri gibi gelecekteki yönleri inceliyor. Bu ilerlemeler birlikte, sadece dolgu malzemeleri olmayan, iyileşmede aktif ortaklar olan; kemik defekti içindeki mekanik ortamı güçlü, kalıcı rejenerasyonu teşvik eden tatlı noktada tutacak şekilde ayarlanmış iskeletlere doğru işaret ediyor.
Atıf: Hou, B., Yang, X., Li, Y. et al. Multiscale biomechanics-driven design pipelines for reconstructive bone scaffolds. npj Biol. Phys. Mech. 3, 5 (2026). https://doi.org/10.1038/s44341-026-00035-9
Anahtar kelimeler: kemik iskeleti tasarımı, biyomekanik, doku rejenerasyonu, 3B baskılı implantlar, mekanobiyoloji