Clear Sky Science · nl
Meervoudige schaal biomechanica-gestuurde ontwerppijplijnen voor reconstructieve botscaffolds
Helpen dat gebroken botten beter genezen
Wanneer een bot ernstig beschadigd is door een ongeluk, ziekte of operatie, kan het lichaam de kloof soms niet zelfstandig herstellen. Chirurgen kunnen nu driedimensionale "scaffolds" implanteren — poreuze, sponsachtige structuren die het defect opvullen en de groei van nieuw bot stimuleren. Dit artikel legt uit hoe een nieuwe ontwerpmethode principes van mechanica op meerdere schalen gebruikt om slimmere scaffolds te maken die niet alleen het bot bij elkaar houden, maar ook voedingsstoffen leveren en de juiste fysieke signalen afgeven aan de cellen die bot herbouwen.
Wat botscaffolds moeten doen
Traditionele bottransplantaten zijn gebaseerd op het verplaatsen van stukken van het eigen bot van de patiënt, wat pijnlijk kan zijn en beperkt in beschikbaarheid. Gefabriceerde scaffolds bieden een alternatief: het zijn op maat gemaakte implantaten die in het defect worden geplaatst en tijdelijk de rol van het natuurlijke dragende raamwerk van het bot overnemen. Hun taak is veeleisend. Ze moeten belastingen dragen zodat het lidmaat of de kaak kan functioneren, bloed en voedingsstoffen toelaten zodat cellen diep binnenin kunnen overleven, en subtiele mechanische signalen geven die stamcellen aanzetten om botvormende cellen te worden in plaats van littekenweefsel. Moderne 3D-printtechnieken en geavanceerde materialen maken het mogelijk om poriegrootte, vorm en oriëntatie met grote precisie te beheersen, wat de deur opent naar sterk gepersonaliseerde implantaten.
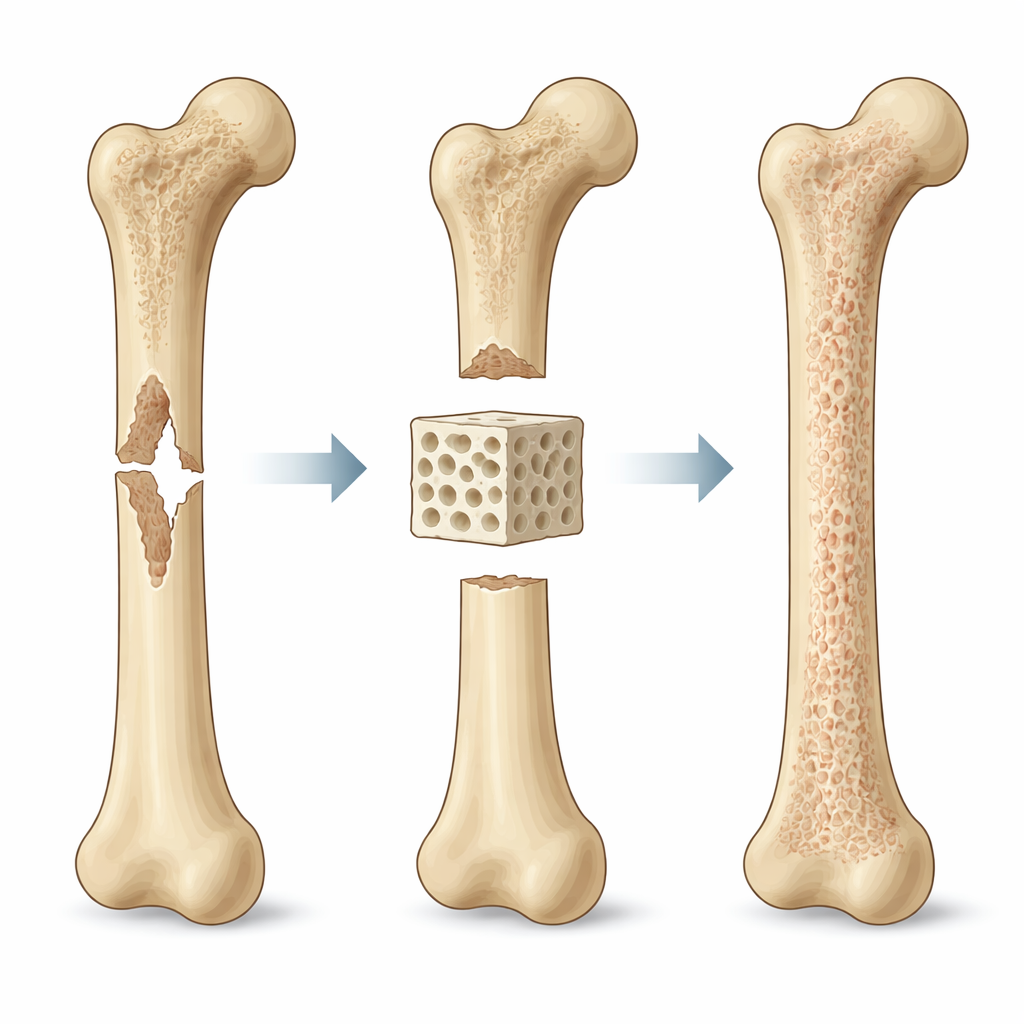
Het probleem vanuit groot naar klein bekijken
De auteurs stellen voor dat het ontwerp van scaffolds gestuurd moet worden door biomechanica op drie onderling gekoppelde schalen. Op de "macro"-schaal — de omvang van het hele botsegment — moet de scaffold het defect overbruggen en krachten delen met het omringende bot. Als hij te zacht is, kunnen kleine bewegingen het implantaat losmaken en zachtere weefsels stimuleren in plaats van bot. Als hij te stijf is, kan hij het natuurlijke bot van belasting afschermen en zo de genezing vertragen. Op de "meso"-schaal — het niveau van poriën en kanalen — bepaalt de architectuur hoe gemakkelijk vloeistof, zuurstof en cellen door de structuur kunnen bewegen. Grotere en beter verbonden poriën verbeteren transport en bloedvatgroei, maar verzwakken de scaffold ook als dat te ver wordt doorgevoerd. Op de "micro"-schaal — waar individuele cellen hun omgeving voelen — beïnvloeden lokale rek, oppervlaktedikte en kleine stromingen hoe cellen zich hechten, van vorm veranderen en beslissen welk weefseltype ze vormen.
Het vinden van de optimale zone voor botvorming
Experimenten en computermodellen suggereren dat botcellen het beste reageren wanneer mechanische signalen binnen bepaalde "vensters" vallen, in plaats van op één perfecte waarde. Te weinig rek of vloeibeweging leidt vaak tot vezelig, littekenachtig weefsel; te veel kan cellen beschadigen of de vroege genezing verstoren. Daartussen ligt een osteogeen venster waarin botvorming wordt bevorderd. De exacte grenzen hangen af van de genezingsfase, de locatie in het lichaam en de conditie van de patiënt, maar het concept is robuust: scaffolds moeten zo worden ontworpen dat, onder dagelijkse belastingen, het grootste deel van hun interieur cellen aan deze gunstige mechanische condities blootstelt terwijl ze nog steeds voldoende sterkte en doorlaatbaarheid bieden.
Een stapsgewijze ontwerppijplijn
Om deze ideeën in de praktijk te brengen, beschrijft het artikel een ontwerppijplijn in vier fasen. Eerst vertalen clinici en ingenieurs patiëntscans, de vorm van het defect en verwachte belastingen naar heldere doelen en grenzen voor de scaffold — zoals gewenste stijfheid, toelaatbare porositeit en beoogde bot- en vaargroei. Ten tweede genereren computers vele virtuele scaffoldontwerpen door materiaal, poriegrootte en interne patronen te variëren, en simuleren vervolgens hoe elk ontwerp krachten draagt, vloeistof verplaatst en de celschaal-omgeving vormt. Ten derde worden de veelbelovende kandidaten gebouwd en in het laboratorium en in diermodellen getest om te controleren of het echte gedrag overeenkomt met de voorspellingen en of cellen daadwerkelijk bot vormen. Tot slot helpen multi-objectif optimalisatietechnieken bij het kiezen van ontwerpen die conflicterende eisen — zoals sterkte versus permeabiliteit — het beste in balans brengen voor specifieke klinische situaties.
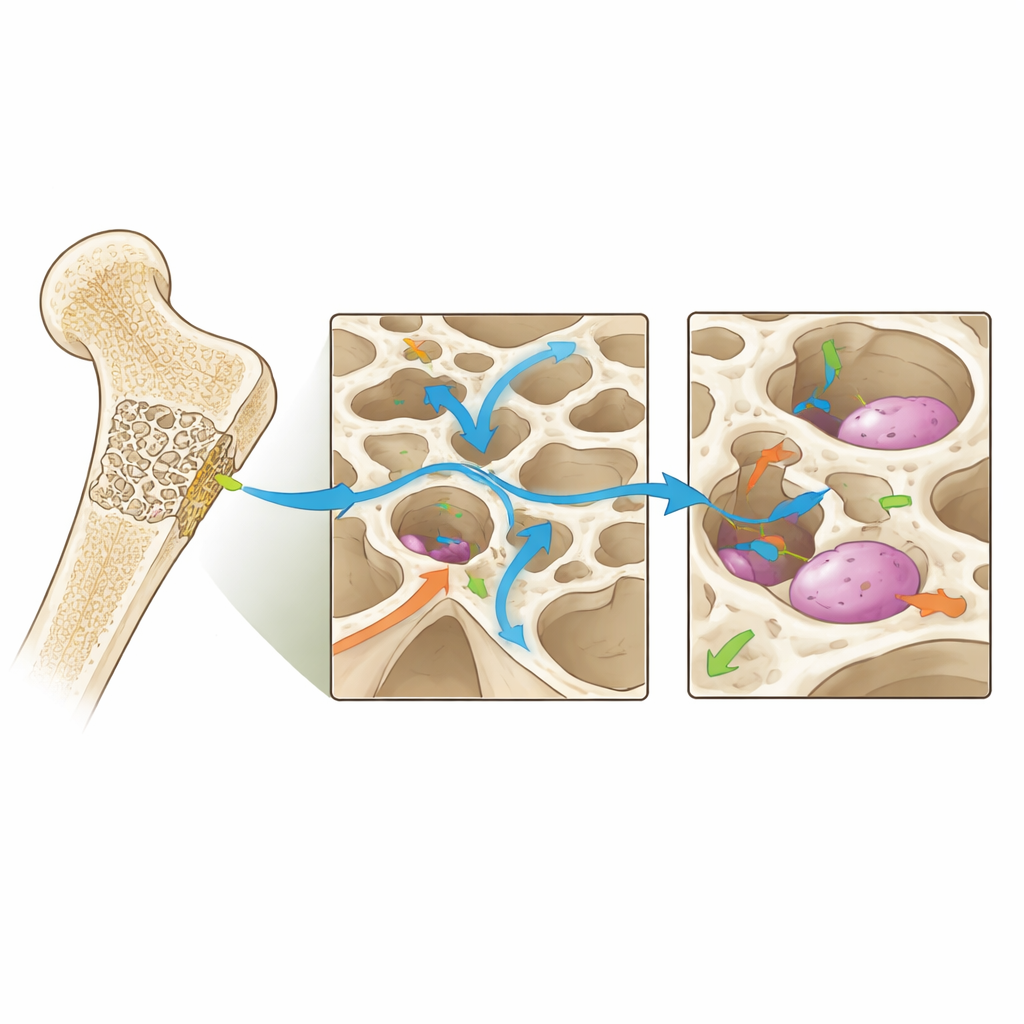
Vooruitkijken naar slimere implantaten
De review verkent ook toekomstige richtingen, waaronder het gebruik van kunstmatige intelligentie om enorme ontwerp‑ruimten te doorzoeken, "slimme" materialen die stijfheid veranderen of factoren afgeven als reactie op gebruik, en digitale tweelingen die bijhouden hoe een geïmplanteerde scaffold en het omliggende bot zich in de loop van de tijd bij een bepaalde patiënt samen ontwikkelen. Gezamenlijk wijzen deze vooruitgangen op scaffolds die niet louter vullers zijn maar actieve partners in genezing — structuren afgestemd om de mechanische omgeving binnen een botdefect in de optimale zone te houden die robuuste, langdurige regeneratie bevordert.
Bronvermelding: Hou, B., Yang, X., Li, Y. et al. Multiscale biomechanics-driven design pipelines for reconstructive bone scaffolds. npj Biol. Phys. Mech. 3, 5 (2026). https://doi.org/10.1038/s44341-026-00035-9
Trefwoorden: ontwerp van botscaffold, biomechanica, weefselregeneratie, 3D-geprinte implantaten, mechanobiologie