Clear Sky Science · de
Multiskalige, biomechanikgesteuerte Entwurfs‑Pipelines für rekonstruktive Knochengerüste
Wie gebrochene Knochen besser heilen können
Wenn ein Knochen durch einen Unfall, eine Erkrankung oder eine Operation schwer beschädigt ist, kann der Körper die Lücke manchmal nicht allein verschließen. Chirurgen können heute dreidimensionale „Gerüste“ implantieren — poröse, schwammartige Stützen, die den Defekt ausfüllen und neues Knochenwachstum fördern. Dieser Artikel erklärt, wie ein neuer Entwurfsansatz Prinzipien der Mechanik auf mehreren Skalen nutzt, um intelligentere Gerüste zu schaffen, die nicht nur den Knochen zusammenhalten, sondern auch Nährstoffe liefern und den Zellen die richtigen physikalischen Signale geben, die Knochen aufbauen.
Was Knochengerüste leisten sollen
Traditionelle Knochentransplantate beruhen darauf, Stücke des körpereigenen Knochens zu verpflanzen, was Schmerzen verursachen kann und nur begrenzt verfügbar ist. Ingenieurmäßig hergestellte Gerüste bieten eine Alternative: Sie sind individuell geformte Implantate, die in den Defekt eingesetzt werden und dort vorübergehend die Rolle des natürlichen Stützgerüsts übernehmen. Ihre Aufgabe ist anspruchsvoll. Sie müssen Lasten tragen, damit Gliedmaßen oder der Kiefer funktionieren, Blut und Nährstoffe tief ins Innere lassen und subtile mechanische Hinweise liefern, die Stammzellen dazu bringen, sich in knochenbildende Zellen statt in Narbengewebe zu verwandeln. Moderne 3D-Druckverfahren und fortschrittliche Materialien erlauben es, Porengröße, -form und -orientierung mit großer Präzision zu steuern und so hochgradig maßgeschneiderte Implantate zu ermöglichen.
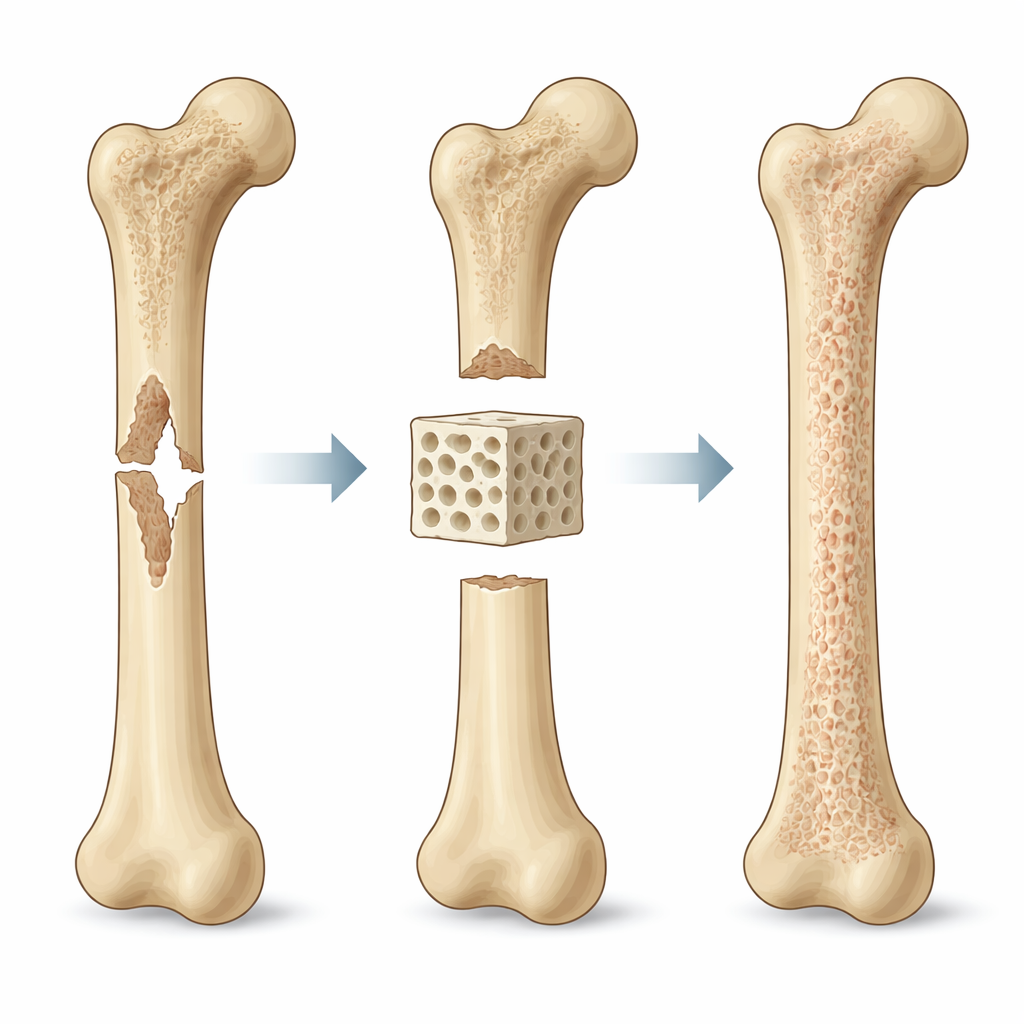
Das Problem von groß bis klein betrachten
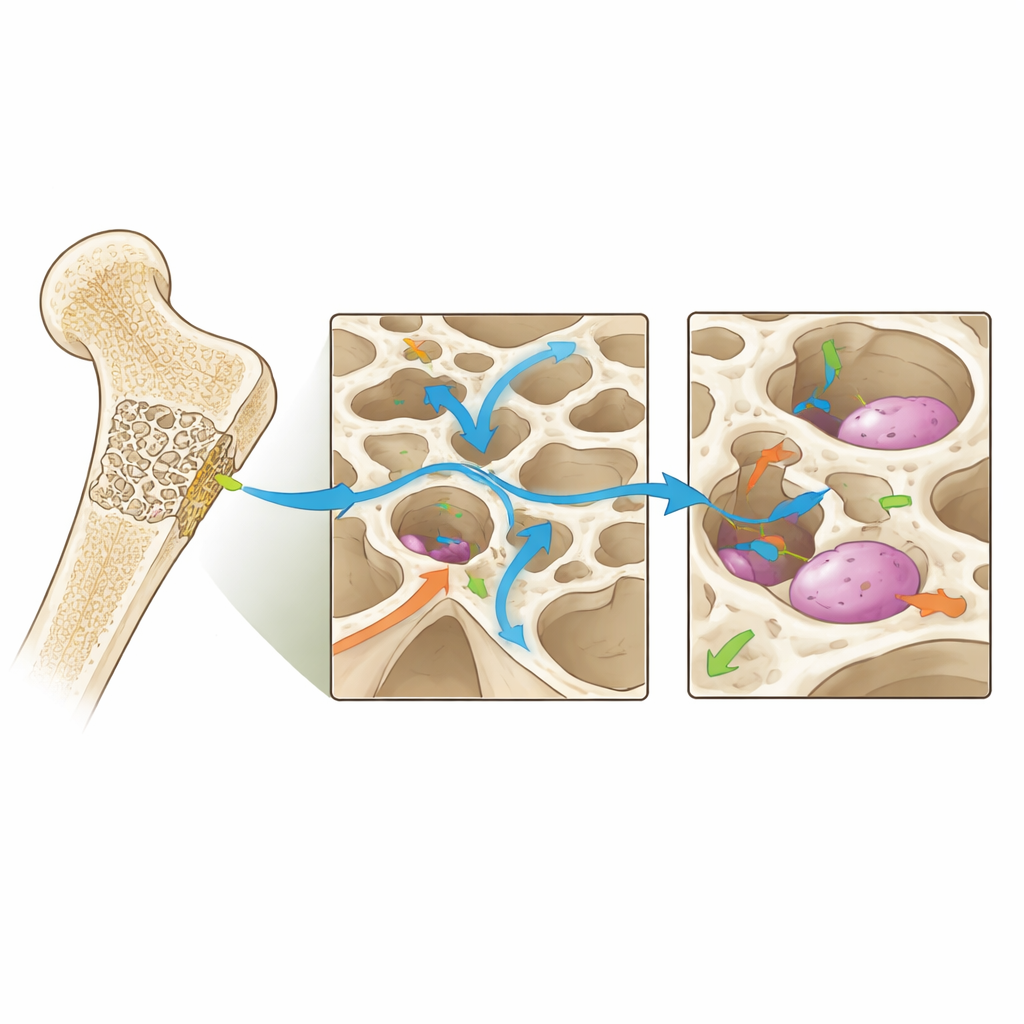
Die Autoren schlagen vor, dass die Gestaltung von Gerüsten durch Biomechanik auf drei miteinander verknüpften Skalen geleitet werden muss. Auf der „Makro“-Skala — der Größe des gesamten Knochenabschnitts — muss das Gerüst den Defekt überbrücken und Kräfte mit dem umgebenden Knochen teilen. Ist es zu weich, können kleinste Bewegungen das Implantat lockern und weiches Gewebe statt Knochen begünstigen. Ist es zu steif, kann es den natürlichen Knochen von Belastung abschirmen und die Heilung verlangsamen. Auf der „Meso“-Skala — der Ebene von Poren und Kanälen — bestimmt die Architektur, wie leicht Flüssigkeiten, Sauerstoff und Zellen durch die Struktur gelangen. Größere und besser vernetzte Poren verbessern den Transport und das Gefäßwachstum, schwächen das Gerüst aber auch, wenn sie übertrieben werden. Auf der „Mikro“-Skala — wo einzelne Zellen ihre Umgebung wahrnehmen — beeinflussen lokale Dehnung, Oberflächensteifigkeit und winzige Strömungen, wie Zellen anhaften, ihre Form ändern und entscheiden, welchen Gewebetyp sie bilden.
Den optimalen Bereich für Knochenwachstum finden
Experimente und Computermodelle legen nahe, dass Knochenzellen am besten reagieren, wenn mechanische Signale innerhalb bestimmter „Fenster“ liegen, statt bei einem einzigen perfekten Wert. Zu geringe Dehnung oder Flüssigkeitsbewegung führt tendenziell zu faserigem, narbenähnlichem Gewebe; zu starke Beanspruchung kann Zellen schädigen oder die frühe Heilung stören. Dazwischen liegt ein osteogenes Fenster, in dem Knochenbildung begünstigt wird. Die genauen Bereiche hängen vom Heilungsstadium, der Körperstelle und dem Zustand des Patienten ab, doch das Konzept ist robust: Gerüste sollten so entworfen werden, dass unter alltäglicher Belastung ein Großteil ihres Inneren Zellen diesen günstigen mechanischen Bedingungen aussetzt und gleichzeitig ausreichende Festigkeit und Fluiddurchlässigkeit gewährleistet bleibt.
Eine schrittweise Entwurfs‑Pipeline
Um diese Ideen in die Praxis zu überführen, skizziert der Artikel eine vierstufige Entwurfs‑Pipeline. Zunächst übersetzen Kliniker und Ingenieure Patienten-Scans, Defektgeometrie und erwartete Belastungen in klare Ziele und Grenzen für das Gerüst — wie Zielsteifigkeit, zulässige Porosität und gewünschtes Knochen- sowie Gefäßwachstum. Zweitens erzeugen Computer viele virtuelle Gerüstentwürfe durch Variation von Material, Porengröße und inneren Mustern und simulieren dann, wie jeder Entwurf Kräfte trägt, Flüssigkeit bewegt und die zellskalige Umgebung gestaltet. Drittens werden die vielversprechendsten Kandidaten gebaut und im Labor sowie in Tiermodellen getestet, um zu prüfen, ob das reale Verhalten den Vorhersagen entspricht und ob Zellen tatsächlich Knochen bilden. Schließlich helfen Multi‑Objective‑Optimierungstechniken, Entwürfe zu wählen, die widersprüchliche Anforderungen, etwa Festigkeit versus Permeabilität, bestmöglich für spezifische klinische Situationen ausbalancieren.
Blick nach vorn: intelligentere Implantate
Die Übersicht beleuchtet auch künftige Richtungen, darunter den Einsatz künstlicher Intelligenz zur Durchsuchung großer Entwurfsräume, „intelligente“ Materialien, die Steifigkeit ändern oder Faktoren freisetzen als Reaktion auf Belastung, und digitale Zwillinge, die nachverfolgen, wie ein implantiertes Gerüst und der umgebende Knochen bei einem bestimmten Patienten gemeinsam über die Zeit ko‑evolvieren. Zusammen deuten diese Fortschritte auf Gerüste hin, die nicht nur Füllstoffe sind, sondern aktive Partner der Heilung — Strukturen, die so abgestimmt sind, dass sie die mechanische Umgebung in einer Knochenlücke im optimalen Bereich halten und damit eine robuste, langlebige Regeneration fördern.
Zitation: Hou, B., Yang, X., Li, Y. et al. Multiscale biomechanics-driven design pipelines for reconstructive bone scaffolds. npj Biol. Phys. Mech. 3, 5 (2026). https://doi.org/10.1038/s44341-026-00035-9
Schlüsselwörter: Design von Knochengerüsten, Biomechanik, Geweberegeneration, 3D-gedruckte Implantate, Mechanobiologie