Clear Sky Science · es
Canales de diseño impulsados por la biomecánica multiescala para andamios óseos reconstructivos
Ayudar a que los huesos rotos sanen mejor
Cuando un hueso queda gravemente dañado por un accidente, una enfermedad o una cirugía, el cuerpo a veces no puede reparar el hueco por sí solo. Hoy los cirujanos pueden implantar «andamios» tridimensionales —soportes porosos, tipo esponja— que rellenan el defecto y fomentan el crecimiento de nuevo hueso. Este artículo explica cómo un nuevo enfoque de diseño utiliza principios de la mecánica a múltiples escalas para crear andamios más inteligentes que no solo mantienen el hueso unido, sino que también suministran nutrientes y envían las señales físicas adecuadas a las células que reconstruyen el hueso.
Para qué sirven los andamios óseos
Los injertos óseos tradicionales se basan en trasplantar fragmentos del propio hueso del paciente, lo que puede causar dolor y tiene suministro limitado. Los andamios diseñados ofrecen una alternativa: son implantes con forma personalizada colocados en el defecto, donde desempeñan temporalmente el papel del armazón de soporte natural del hueso. Su trabajo es exigente. Deben soportar cargas para que la extremidad o la mandíbula funcionen, permitir que la sangre y los nutrientes alcancen células profundamente situadas y proporcionar señales mecánicas sutiles que indiquen a las células madre que se conviertan en células formadoras de hueso en lugar de tejido cicatricial. La impresión 3D moderna y los materiales avanzados permiten controlar con gran precisión el tamaño, la forma y la orientación de los poros, abriendo la puerta a implantes altamente personalizados.
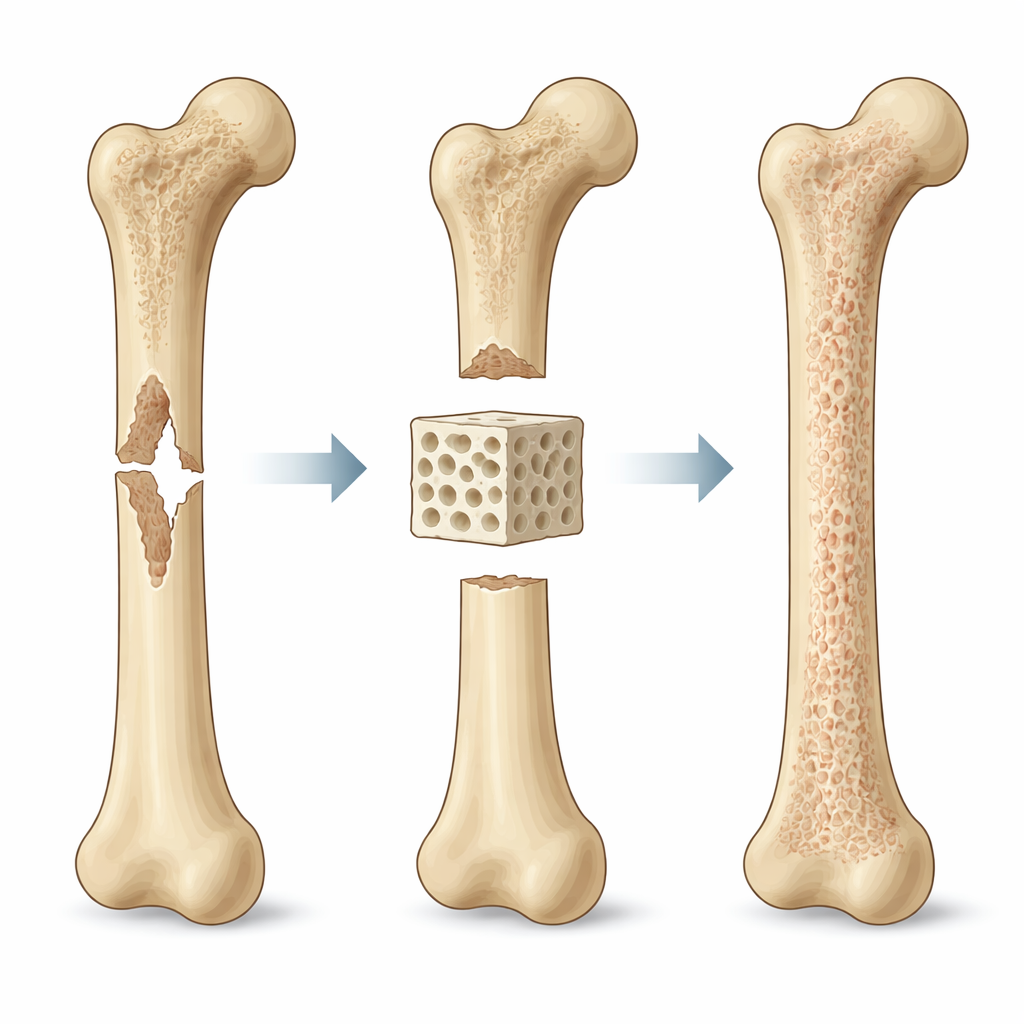
Mirar el problema de lo grande a lo pequeño
Los autores proponen que el diseño del andamio debe guiarse por la biomecánica en tres escalas vinculadas. A escala «macro» —el tamaño del segmento óseo completo— el andamio debe salvar el defecto y compartir fuerzas con el hueso circundante. Si es demasiado blando, pequeños movimientos pueden aflojar el implante y fomentar tejido blando en lugar de hueso. Si es demasiado rígido, puede proteger en exceso al hueso natural del esfuerzo, ralentizando la curación. A escala «meso» —el nivel de poros y canales— su arquitectura gobierna la facilidad con que el fluido, el oxígeno y las células pueden desplazarse por la estructura. Poros más grandes y mejor conectados mejoran el transporte y el crecimiento vascular, pero también debilitan el andamio si se exagera. A escala «micro» —donde las células individuales perciben su entorno— la deformación local, la rigidez superficial y los pequeños flujos influyen en cómo las células se adhieren, cambian de forma y deciden qué tipo de tejido formar.
Encontrar el punto óptimo para el crecimiento óseo
Experimentos y modelos por ordenador sugieren que las células óseas responden mejor cuando las señales mecánicas se sitúan dentro de ciertas «ventanas», más que en un único valor perfecto. Muy poca deformación o movimiento de fluidos tiende a producir tejido fibroso, similar a cicatriz; demasiado puede dañar las células o perturbar la curación temprana. En el intervalo intermedio existe una ventana osteogénica donde se favorece la formación de hueso. Los rangos exactos dependen de la fase de la curación, la localización en el cuerpo y la condición del paciente, pero el concepto es sólido: los andamios deben diseñarse para que, bajo cargas cotidianas, la mayor parte de su interior exponga a las células a estas condiciones mecánicas favorables garantizando al mismo tiempo resistencia y transporte de fluidos adecuados.
Un proceso de diseño paso a paso
Para convertir estas ideas en práctica, el artículo describe una canalización de diseño en cuatro fases. Primero, clínicos e ingenieros traducen las exploraciones del paciente, la forma del defecto y las cargas esperadas en objetivos y límites claros para el andamio —como rigidez objetivo, porosidad admisible y crecimiento deseado de hueso y vasos—. Segundo, los ordenadores generan muchos diseños virtuales variando material, tamaño de poro y patrones internos, y simulan cómo cada uno soporta fuerzas, mueve fluidos y configura el entorno a escala celular. Tercero, los candidatos más prometedores se fabrican y prueban en el laboratorio y en modelos animales para verificar que el comportamiento real coincide con las predicciones y que las células efectivamente forman hueso. Finalmente, técnicas de optimización multiobjetivo ayudan a elegir diseños que mejor equilibran necesidades en conflicto, como resistencia frente a permeabilidad, para situaciones clínicas específicas.
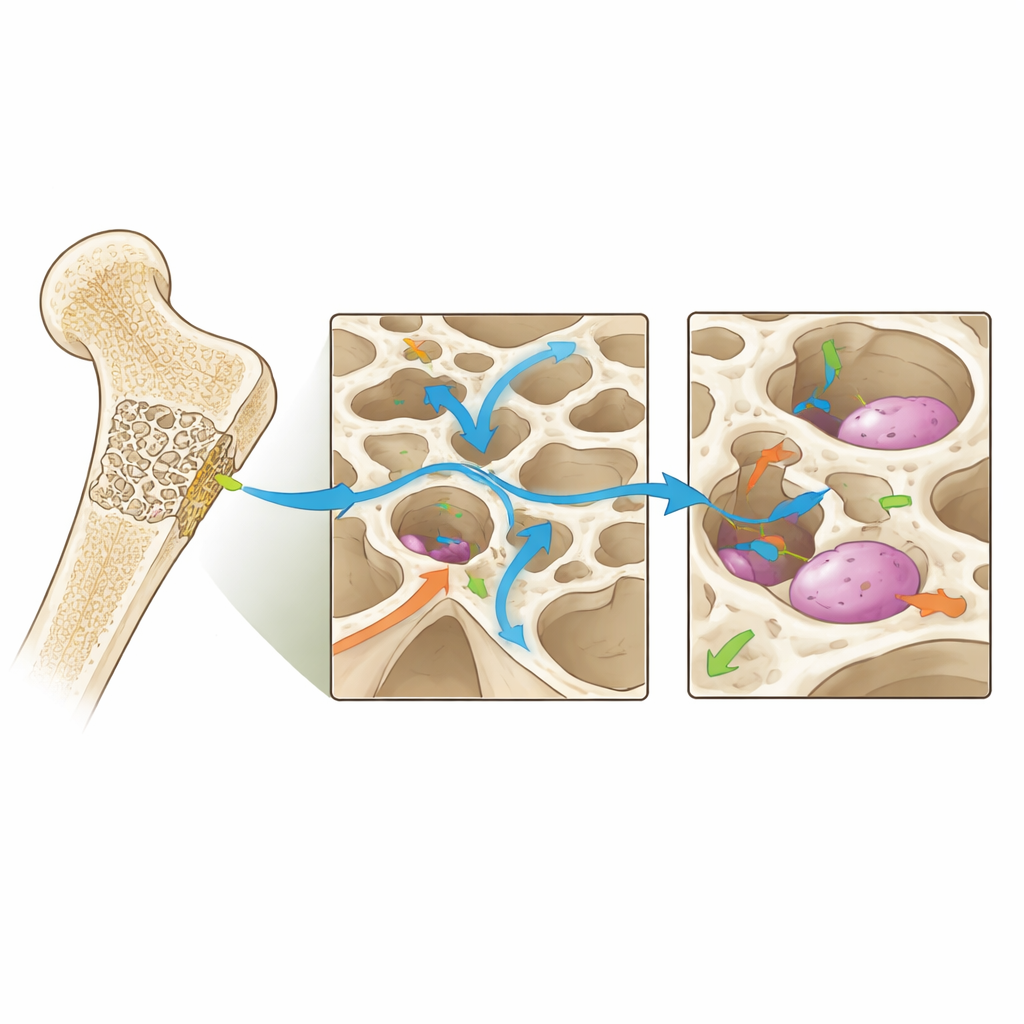
Mirando hacia implantes más inteligentes
La revisión también explora direcciones futuras, incluyendo el uso de inteligencia artificial para explorar vastos espacios de diseño, materiales «inteligentes» que cambian la rigidez o liberan factores en respuesta al uso, y modelos de gemelo digital que siguen cómo coevoluciona con el tiempo un andamio implantado y el hueso circundante en un paciente concreto. En conjunto, estos avances apuntan a andamios que no son meros rellenos sino socios activos en la curación: estructuras afinadas para mantener el entorno mecánico dentro de un defecto óseo en el punto óptimo que fomenta una regeneración robusta y duradera.
Cita: Hou, B., Yang, X., Li, Y. et al. Multiscale biomechanics-driven design pipelines for reconstructive bone scaffolds. npj Biol. Phys. Mech. 3, 5 (2026). https://doi.org/10.1038/s44341-026-00035-9
Palabras clave: diseño de andamios óseos, biomecánica, regeneración tisular, implantes impresos en 3D, mecanobiología