Clear Sky Science · tr
Radyomik, derin öğrenme, transkriptomik ve metabolomik entegrasyonu, kolorektal kanserde prognostik risk sınıflandırması ve alttaki biyolojik mekanizmaları ortaya koyuyor
Bu araştırma hastalar ve aileleri için neden önemli
Kolorektal kanser, dünya çapında en yaygın ve ölümcül kanserlerden biridir; yine de cerrahi sonrası hangi hastaların iyi sonuç alacağını ve hangi hastaların hastalıktan ölme riski daha yüksek olduğunu tahmin etmek hekimler için zordur. Bu çalışma, sıradan tıbbi taramaların ileri bilgisayar analizleri ve moleküler testlerle birleştirildiğinde hastaları net risk gruplarına ayırabildiğini ve tümörlerinin içindeki gizli biyolojiyi ortaya çıkarabildiğini gösteriyor. Gelecekte bu tür bir yaklaşım, yüksek riskli hastaların daha sık izlenmesi ve daha güçlü tedaviler alması, düşük riskli hastaların ise gereksiz yan etkilere maruz kalmaması için tedavi ve takipleri kişiselleştirmeye yardımcı olabilir.
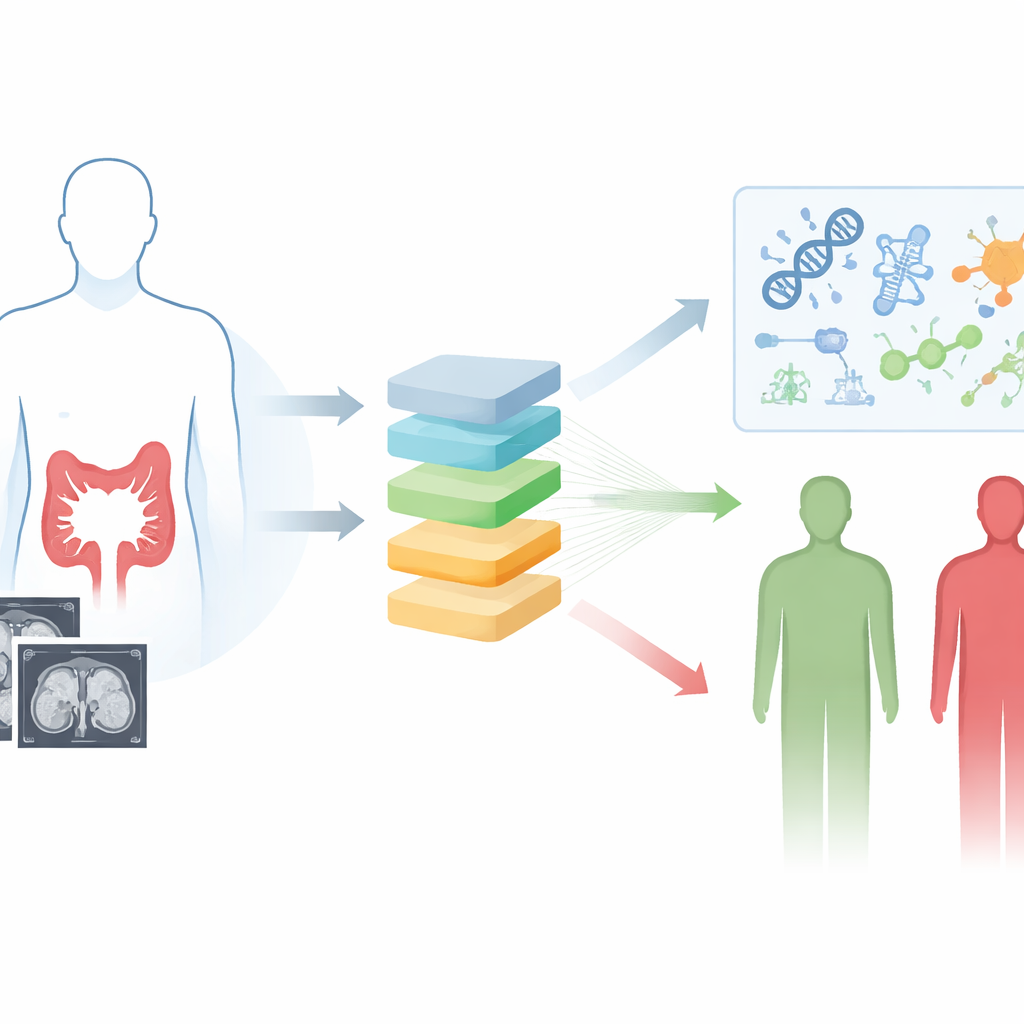
Skalpeli kullanmadan tümörlerin içine bakmak
Araştırmacılar, kolorektal kanseri değerlendirmede rutin olarak kullanılan kontrastlı BT taramalarına odaklandı. İnsan gözünün görebildiğine dayanmaktansa, görüntülerden yaklaşık 2.000 küçük nicel detayı çıkarmak için radyomik ve derin öğrenmeyi kullandılar; bu, tümör heterojenliğini yansıtan şekil ve dokuya ait ince desenleri yakalıyor. Ardından bu görüntü özelliklerini hastaların ne kadar süre yaşadığıyla ilişkilendirmek için on makine öğrenmesi algoritmasının 117 kombinasyonunu sistematik olarak test ettiler. Lasso ve gradient boosting adı verilen iki tekniği harmanlayan kazanan model, tamamen preoperatif BT taramasına dayanarak her kişi için tek bir risk skoru üretti.
Düşük riskli ve yüksek riskli hastaları ayırmak
Takım, dört hastanede tedavi edilen 1.183 hastanın BT görüntülerini kullanarak derin öğrenme tabanlı radyomik modelini eğitti ve titizlikle test etti. Görüntüye dayalı skorda hastaları düşük riskli ve yüksek riskli gruplara ayıran bir eşik belirlediler. Eğitim setinde, dahili doğrulama setinde ve iki bağımsız hastanede yüksek riskli hastaların düşük riskli gruptakilere göre tutarlı şekilde daha kısa yaşadığı görüldü. Modelin sonuçları ayırt etme yeteneği, daha genç ve daha yaşlı hastalar, kadın ve erkekler, farklı tümör evreleri ve kemoterapi alıp almadıklarına göre gibi birçok alt grupta korundu. Araştırmacılar görüntü tabanlı skoru iki standart klinik gösterge—kandaki CEA düzeyi ve lenf nodu evresi—ile birleştirip nomogram adlı basit bir grafik araç oluşturduklarında, üç ve beş yıllık sağkalım tahminleri daha da isabetli ve klinik olarak yararlı hale geldi.
Bir tümörü diğerinden daha tehlikeli kılan nedir?
Tahminin ötesine geçip bazı tümörlerin neden daha agresif davrandığını anlamak için ekip, görüntüye dayalı risk gruplarını kansere ait moleküler değişikliklerle ilişkilendirdi. Bir hasta alt kümesinde, tümör dokusundaki küçük molekülleri nükleer manyetik rezonans spektroskopisiyle analiz edip tümörleri yakınındaki normal doku ile karşılaştırdılar. Yüksek riskli ve düşük riskli tümörlerin, aminoasitleri ve kısa zincirli yağ asitlerini işleyen yolları içeren farklı metabolik parmak izlerine sahip olduğunu buldular. Paralel olarak, ekip halka açık bir görüntüleme veritabanındaki tümörlerin gen aktivitesini inceledi. Yüksek riskli tümörler, hücrelerin çevresindeki destek iskeleti olan ekstrasellüler matriks ile ilişkili yolların güçlü sinyallerini gösterdi; bu yapıların kanser hücrelerinin yayılmasına ve tedaviye direnç göstermesine yardımcı olduğu biliniyor. Düşük riskli tümörler ise immünle ilişkili yollar açısından zengindi ve daha yüksek düzeyde kanser öldürücü CD8 T hücreleri içeriyordu; bu da daha aktif bir anti-tümör immün ortamına işaret ediyor.
Daha iyi sağkalımla ilişkili koruyucu metabolik yollar
Çarpıcı biçimde, hem metabolit verileri hem de gen aktivite verileri aynı iki metabolik rotaya—butanoat metabolizması ve azot metabolizması—işaret etti ve bunların düşük riskli tümörlerde daha aktif olduğunu gösterdi. Bu yollar, bağırsak bakterilerinin ürünleriyle ve hücrelerin azotu nasıl işlediğiyle bağlantılıdır; bu da enerji dengesini ve immün fonksiyonu etkiler. Araştırmacılar The Cancer Genome Atlas’tan 417 kolorektal kanser hastasını içeren büyük, bağımsız bir veri setini kontrol ettiklerinde, bu iki yolun daha düşük aktivitesinin daha kötü genel sağkalımla açıkça ilişkili olduğunu buldular. Bu, bu metabolik süreçlerin sürdürülmesinin tümör büyümesini sınırlamaya veya daha güçlü bir immün yanıta destek olmaya yardımcı olabileceğini ve bir gün biyobelirteç veya tedavi hedefi olarak araştırılabileceklerini düşündürüyor.
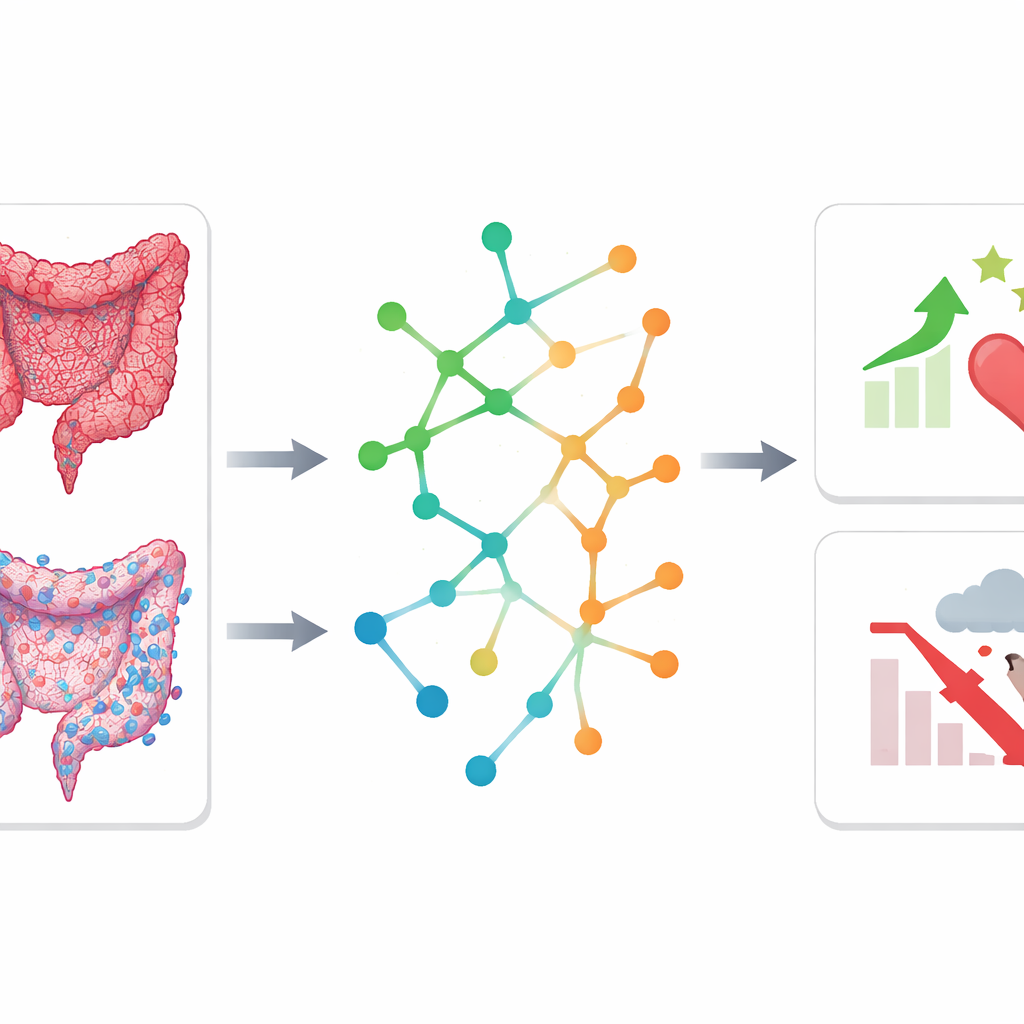
Gelecekteki kanser bakımına ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma akıllı görüntü analizini moleküler profilleme ile birleştirmenin hem prognostik araçları keskinleştirebileceğini hem de kolorektal tümörlerin içinde neler olduğunu ortaya çıkarabileceğini gösteriyor. Standart BT taramalarından türetilen bir risk skoru, özellikle rutin klinik ölçümlerle eşleştirildiğinde, doktorların cerrahi sonrası hangi hastaların daha yoğun tedavi veya takip gerektirdiğini belirlemesine yardımcı olabilir. Aynı zamanda, belirli immün desenler ve metabolik yolların daha iyi sonuçlarla ilişkilendirilmesi, vücudun savunmasını desteklemenin ve hedefe yönelik tedaviler tasarlamanın yeni yollarına işaret ediyor. Bu bulguların doğrulanması için daha büyük, prospektif çalışmalara ihtiyaç olsa da, bu bütünleştirici yaklaşım kolorektal kanser hastaları için daha kişiselleştirilmiş, biyolojiyle bilgilendirilmiş bakıma doğru atılmış bir adımı temsil ediyor.
Atıf: Li, Z., Cai, R., Qin, Y. et al. Integration of radiomics, deep learning, transcriptomics, and metabolomics reveals prognostic risk stratification and underlying biological mechanisms in colorectal cancer. npj Precis. Onc. 10, 155 (2026). https://doi.org/10.1038/s41698-026-01331-2
Anahtar kelimeler: kolorektal kanser, radyomik, derin öğrenme, tümör metabolizması, immün mikroçevre