Clear Sky Science · ar
دمج الرِّئوميكس، التعلّم العميق، النسخوميات، والتمثيل الغذائي يكشف تصنيف المخاطر التنبؤي والآليات البيولوجية الكامنة في سرطان القولون والمستقيم
لماذا يهم هذا البحث المرضى وعائلاتهم
يعد سرطان القولون والمستقيم من أكثر السرطانات شيوعًا وسُببًا للوفاة في العالم، ومع ذلك لا يزال الأطباء يجدون صعوبة في التنبؤ بمن سيفيْق وضعه جيدًا بعد الجراحة ومن هم المعرضون لخطر أكبر للوفاة بسبب المرض. تُظهر هذه الدراسة أن الفحوصات الطبية الروتينية، عند دمجها مع تحليل حاسوبي متقدّم وفحوصات جزيئية، يمكنها تصنيف المرضى إلى مجموعات مخاطِر واضحة وكشف البيولوجيا الخفية داخل أورامهم. في المستقبل، قد يساعد هذا النوع من النهج على تخصيص العلاج والمتابعة بحيث يحظى المرضى ذوو المخاطر العالية بمراقبة أقرب وعلاجات أقوى، بينما يتجنّب المرضى ذوو المخاطر المنخفضة آثارًا جانبيّة غير ضرورية.
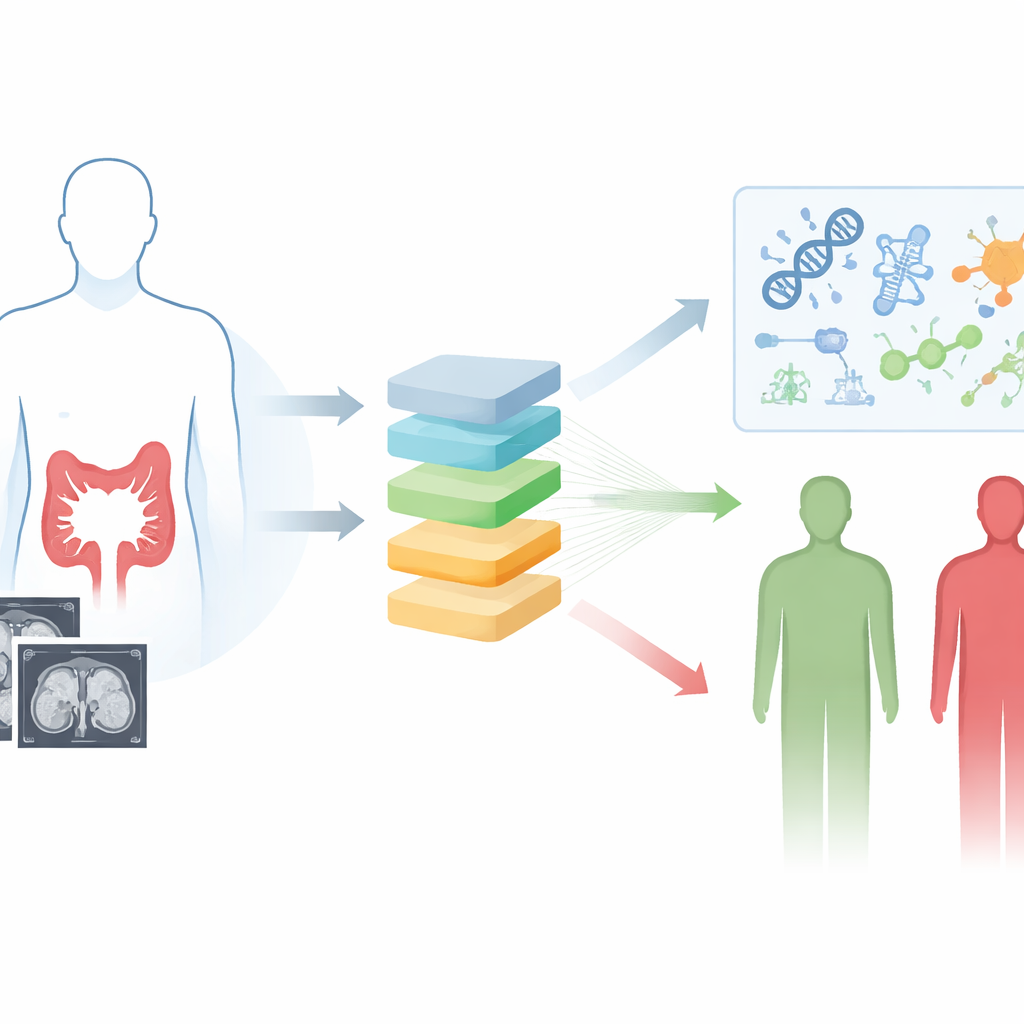
نظرة داخل الأورام من دون مشرط
ركّز الباحثون على فحوص الأشعة المقطعية المحسنة بالصبغة، وهو اختبار تصوير روتيني يُستخدم بالفعل في تقييم سرطان القولون والمستقيم. بدلًا من الاعتماد على ما تراه العين البشرية، استخدموا الرِّئوميكس والتعلّم العميق لاستخراج ما يقرب من 2000 ميزة كمية دقيقة من الصور، تلتقط أنماطًا دقيقة في الشكل والملمس تعكس تعدّدية خلايا الورم. بعد ذلك اختبروا بشكل منهجي 117 تركيبة من عشرة خوارزميات تعلّم آلي لإيجاد الطريقة الأكثر موثوقية لربط هذه ميزات الصورة بمدى بقاء المرضى. أعطى النموذج الفائز، الذي مزج بين تقنيتين تُدعيان لاسو والتدرّج المعزّز، درجة مخاطرة واحدة لكل شخص اعتمادًا فقط على صور الأشعة المقطعية قبل الجراحة.
فصل المرضى منخفضي الخطر عن عاليي الخطر
باستخدام صور الأشعة المقطعية لـ 1183 مريضًا عُولجوا في أربعة مستشفيات، درّب الفريق نموذج الرِّئوميكس القائم على التعلّم العميق واختبره بدقّة. حدّدوا عتبة في الدرجة المبنية على الصورة قسمت المرضى إلى مجموعتي خطر منخفض وخطر مرتفع. عبر مجموعة التدريب ومجموعة التحقق الداخلي ومستشفيين مستقلين، عاش المرضى ذوو الخطر العالي فترة أقصر باستمرار من أولئك في مجموعة الخطر المنخفض. بقيت قدرة النموذج على تمييز النتائج ثابتة عبر العديد من الفِرَق الفرعية، بما في ذلك المرضى صغارًا وكبارًا، والرجال والنساء، ومراحل الورم المختلفة، وما إذا كان المرضى قد تلقّوا الكيميائيّات أم لا. عندما جمع الباحثون الدرجة المبنية على الصورة مع مؤشرين سريريين قياسيين—مستويات الدم من CEA ومرحلة العقد اللمفاوية—في أداة رسومية بسيطة تُدعى اسميًا (نوموجرام)، أصبحت توقعات البقاء لثلاث وخمس سنوات أكثر دقة وفائدة سريرية.
ما الذي يجعل ورمًا أكثر خطورة من آخر؟
للتجاوز عن حدود التنبؤ وفهم لماذا تتصرّف بعض الأورام بشكل أكثر عدوانية، ربط الفريق مجموعات المخاطر المبنية على الصور بالتغيرات الجزيئية في السرطان. في مجموعة فرعية من المرضى، حلّلوا الجزيئات الصغيرة في نسيج الورم باستخدام مطيافية الرنين المغناطيسي النووي وقارنوا الأورام بالنسيج الطبيعي المجاور. وجدوا أن الأورام عالية المخاطر ومنخفضة المخاطر لها بصمات أيضية مميزة، تشمل مسارات تتعامل مع الأحماض الأمينية والأحماض الدهنية قصيرة السلسلة. بالتوازي، فحصوا نشاط الجينات في الأورام من قاعدة بيانات صور عامة. أظهرت الأورام عالية المخاطر إشارات قوية من مسارات متعلّقة بالمصفوفة خارج الخلوية—الهيكل الداعم حول الخلايا—الذي يُعرف بأنه يساعد خلايا السرطان على الانتشار ومقاومة العلاج. أما الأورام منخفضة المخاطر فكانت غنية بمسارات متعلقة بالمناعة واحتوت على مستويات أعلى من خلايا CD8 التائية القاتلة للسرطان، مما يشير إلى بيئة مناعية مضادّة للورم أكثر نشاطًا.
مسارات أيضية حمائية مرتبطة ببقاء أفضل
من اللافت أن بيانات المستقلبات وبيانات نشاط الجينات أشارتا إلى نفس مسارين أيضيين اثنين—تمثيل البيوتانات (butanoate) وتمثيل النيتروجين—بأنهما أكثر نشاطًا في الأورام منخفضة المخاطر. ترتبط هذه المسارات بمنتجات بكتيريا الأمعاء وبكيفية معالجة الخلايا للنيتروجين، ما يؤثر على توازن الطاقة ووظيفة المناعة. عندما تحقق الباحثون في مجموعة بيانات مستقلة كبيرة مكونة من 417 مريضًا بسرطان القولون والمستقيم من مشروع أطلس الجينوم للسرطان (The Cancer Genome Atlas)، وجدوا أن انخفاض نشاط هذين المسارين كان مرتبطًا بوضوح ببقاء عام أسوأ. يقترح هذا أن الحفاظ على هذه العمليات الأيضية قد يساعد في كبح نمو الورم أو دعم استجابة مناعية أقوى، وأنه قد يُستَكشَف يومًا ما كعلامات حيوية أو أهداف علاجية.
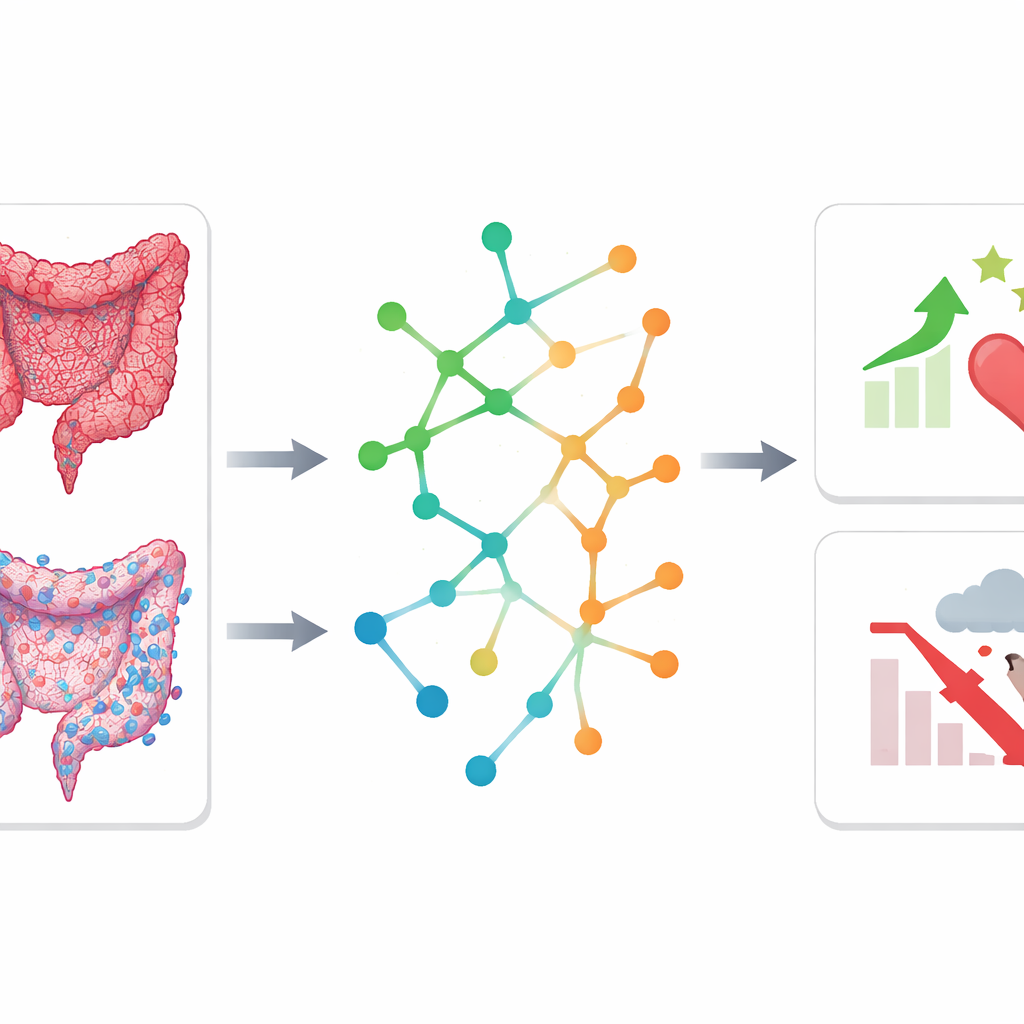
ماذا يعني هذا لرعاية السرطان المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن دمج تحليل الصور الذكي مع التصنيف الجزيئي يمكنه تحسين أدوات التنبؤ وكشف ما يجري داخل أورام القولون والمستقيم. يمكن أن تساعد درجة المخاطرة المستنبطة من صور الأشعة المقطعية القياسية، خاصة عند اقترانها بالقياسات السريرية الروتينية، الأطباء على تحديد المرضى الذين يحتاجون إلى علاج أو متابعة مكثّفة بعد الجراحة. في الوقت نفسه، توحي الاكتشافات بأن أنماطًا مناعية ومسارات أيضية معينة مرتبطة بنتائج أفضل بسبل جديدة لدعم دفاعات الجسم وتصميم علاجات موجهة. ومع حاجة دراسات مستقبلية أكبر واستباقية لتأكيد هذه النتائج، يمثل هذا النهج التكاملِي خطوة نحو رعاية أكثر تخصيصًا ومستنيرة بالبيولوجيا للأشخاص المصابين بسرطان القولون والمستقيم.
الاستشهاد: Li, Z., Cai, R., Qin, Y. et al. Integration of radiomics, deep learning, transcriptomics, and metabolomics reveals prognostic risk stratification and underlying biological mechanisms in colorectal cancer. npj Precis. Onc. 10, 155 (2026). https://doi.org/10.1038/s41698-026-01331-2
الكلمات المفتاحية: سرطان القولون والمستقيم, الرِّئوميكس, التعلّم العميق, تمثيل الورم الغذائي, البيئة المناعية الدقيقة