Clear Sky Science · ru
Интеграция радиомики, глубокого обучения, транскриптомики и метаболомики выявляет прогностическую стратификацию риска и лежащие в основе биологические механизмы при колоректальном раке
Почему это исследование важно для пациентов и их семей
Колоректальный рак — один из самых распространённых и смертельных видов рака в мире, и врачи по‑прежнему затрудняются предсказать, кто будет хорошо себя чувствовать после операции, а у кого риск смерти от болезни выше. В этом исследовании показано, что обычные медицинские сканы в сочетании с продвинутым компьютерным анализом и молекулярными тестами позволяют разделить пациентов на чёткие группы риска и выявить скрытую биологию внутри их опухолей. В будущем такой подход может помочь индивидуализировать лечение и наблюдение: пациентам высокого риска обеспечить более тщательный контроль и более агрессивную терапию, а пациентам низкого риска — избежать ненужных побочных эффектов.
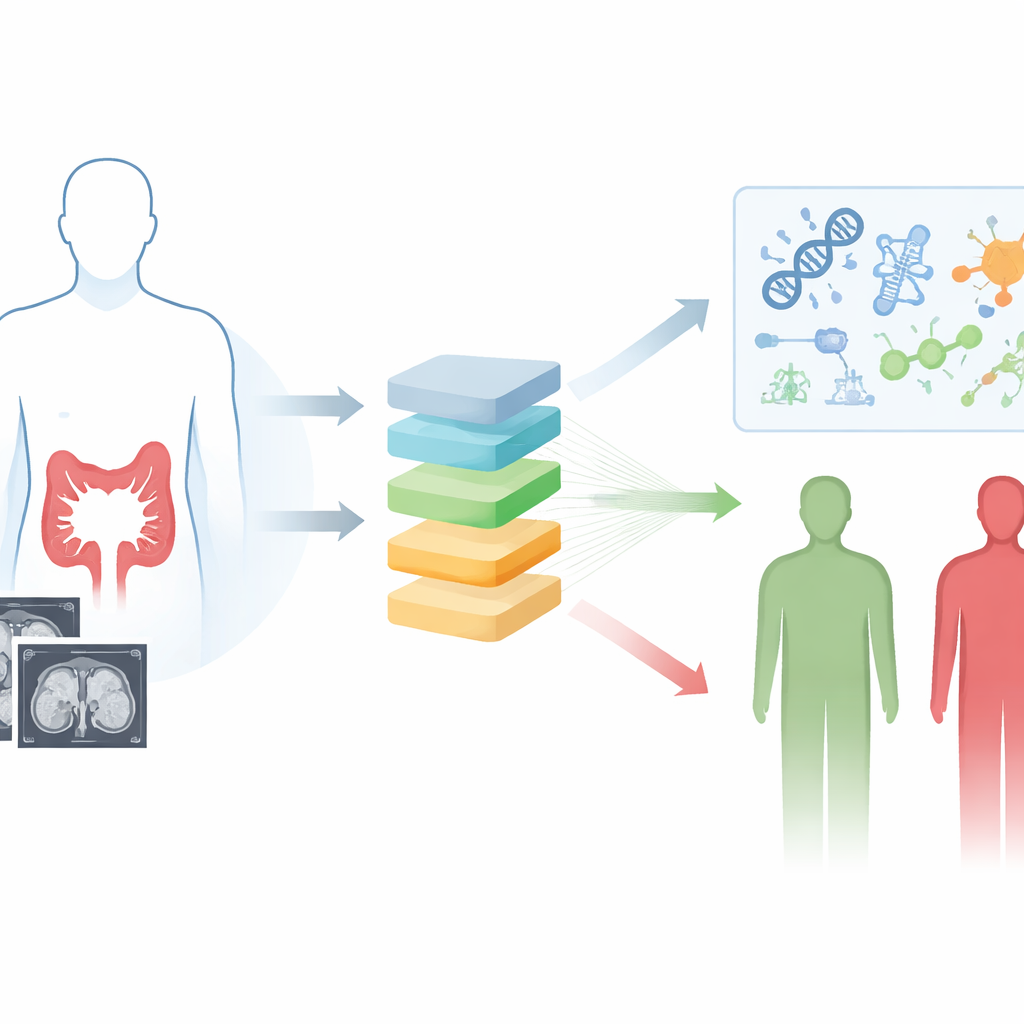
Заглянуть в опухоль без скальпеля
Исследователи сосредоточились на контрастно‑усиленных КТ‑сканах, рутинном методе визуализации, уже используемом при оценке колоректального рака. Вместо того чтобы полагаться на то, что видит человеческий глаз, они применили радиомику и глубокое обучение, чтобы извлечь почти 2000 мелких количественных признаков из изображений, фиксирующих тонкие паттерны формы и текстуры, отражающие гетерогенность опухоли. Затем они систематически протестировали 117 комбинаций десяти алгоритмов машинного обучения, чтобы найти наиболее надёжный способ связать эти признаки изображения с длительностью выживания пациентов. Победившая модель, сочетавшая два метода — Lasso и градиентный бустинг, — выдавала единый риск‑скор для каждого человека, основанный исключительно на предоперационной КТ.
Отделение пациентов низкого и высокого риска
Используя КТ‑сканы 1183 пациентов из четырёх больниц, команда обучила и тщательно протестировала свою глубокую радиомическую модель. Они определили порог в скоре, полученном из изображений, который разделил пациентов на группы низкого и высокого риска. В обучающей выборке, во внутренней валидационной выборке и в двух независимых больницах пациенты высокого риска последовательно жили меньше, чем пациенты низкого риска. Способность модели различать исходы сохранялась во многих подгруппах, включая молодых и пожилых пациентов, мужчин и женщин, разные стадии опухоли и в зависимости от того, получали ли пациенты химиотерапию. Когда исследователи объединили изображенческий скор с двумя стандартными клиническими индикаторами — уровнем CEA в крови и стадией лимфоузлов — в простое графическое средство (номограмму), прогнозы на три и пять лет стали ещё более точными и клинически полезными.
Почему одна опухоль опаснее другой?
Чтобы выйти за рамки простого предсказания и понять, почему некоторые опухоли ведут себя агрессивнее, команда связала группы риска по изображениям с молекулярными изменениями в раке. В подгруппе пациентов они проанализировали малые молекулы в опухолевой ткани с помощью ядерно‑магнитного резонанса и сравнили опухоли с соседней нормальной тканью. Они обнаружили, что опухоли высокого и низкого риска имеют разные метаболические отпечатки, затрагивающие пути, связанные с аминокислотами и короткоцепочечными жирными кислотами. Параллельно была исследована активность генов в опухолях из публичной базы изображений. У опухолей высокого риска наблюдались выраженные сигналы путей, связанных с внеклеточным матриксом — опорной структурой вокруг клеток, которая способствует распространению раковых клеток и устойчивости к терапии. В опухолях низкого риска, напротив, преобладали иммунные пути и был выявлен более высокий уровень CD8+ Т‑клеток, убийц раковых клеток, что указывает на более активную противоопухолевую иммунную среду.
Защитные метаболические пути, связанные с лучшей выживаемостью
Удивительно, но и данные о метаболитах, и данные об активности генов указывали на одни и те же два метаболических маршрута — метаболизм бутирата (бутаноата) и азотный метаболизм — как более активные в опухолях низкого риска. Эти пути связаны с продуктами кишечных бактерий и с тем, как клетки обрабатывают азот, что влияет на энергетический баланс и функцию иммунной системы. При проверке на большой независимой выборке из 417 пациентов с колоректальным раком из The Cancer Genome Atlas оказалось, что пониженная активность этих двух путей явно ассоциируется с худшей общей выживаемостью. Это позволяет предположить, что поддержание этих метаболических процессов может помочь сдерживать рост опухоли или поддерживать более сильную иммунную реакцию, и что впоследствии они могут быть изучены как биомаркеры или терапевтические мишени.
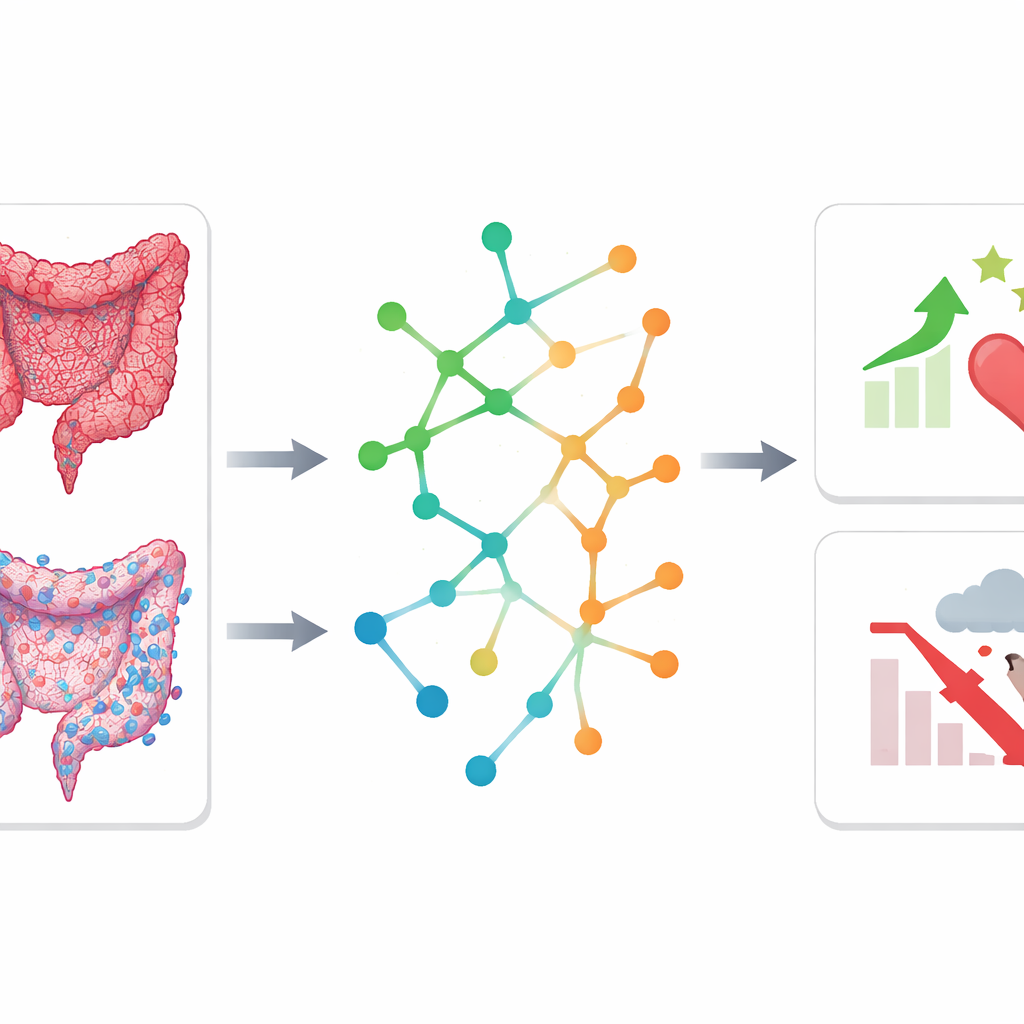
Что это значит для будущей онкологической помощи
Проще говоря, это исследование показывает, что комбинирование интеллектуального анализа изображений с молекулярным профилированием может как улучшить прогностические инструменты, так и раскрыть процессы, происходящие внутри колоректальных опухолей. Риск‑скор, полученный из стандартных КТ‑сканов, особенно в сочетании с рутинными клиническими измерениями, может помочь врачам выявлять пациентов, которым после операции потребуется более интенсивное лечение или наблюдение. Одновременно открытие, что определённые иммунные паттерны и метаболические пути связаны с лучшими исходами, намекает на новые пути поддержки иммунной защиты организма и разработки таргетной терапии. Хотя для подтверждения этих результатов нужны более масштабные проспективные исследования, такой интегративный подход — шаг к более персонализированной, биологически информированной помощи людям с колоректальным раком.
Цитирование: Li, Z., Cai, R., Qin, Y. et al. Integration of radiomics, deep learning, transcriptomics, and metabolomics reveals prognostic risk stratification and underlying biological mechanisms in colorectal cancer. npj Precis. Onc. 10, 155 (2026). https://doi.org/10.1038/s41698-026-01331-2
Ключевые слова: колоректальный рак, радиомика, глубокое обучение, метаболизм опухоли, иммунная микроокружение