Clear Sky Science · fr
Intégration de la radiomique, de l’apprentissage profond, de la transcriptomique et de la métabolomique révèle une stratification pronostique du risque et les mécanismes biologiques sous-jacents dans le cancer colorectal
Pourquoi cette recherche est importante pour les patients et leurs proches
Le cancer colorectal est l’un des cancers les plus fréquents et les plus mortels dans le monde, et les médecins peinent encore à prédire quels patients se porteront bien après une chirurgie et lesquels courent un risque plus élevé de mourir de la maladie. Cette étude montre que des examens médicaux ordinaires, combinés à des analyses informatiques avancées et à des tests moléculaires, peuvent classer les patients en groupes de risque distincts et révéler la biologie cachée de leurs tumeurs. À l’avenir, ce type d’approche pourrait aider à personnaliser les traitements et le suivi afin que les patients à haut risque bénéficient d’une surveillance plus étroite et de thérapies plus fortes, tandis que les patients à faible risque évitent des effets indésirables inutiles.
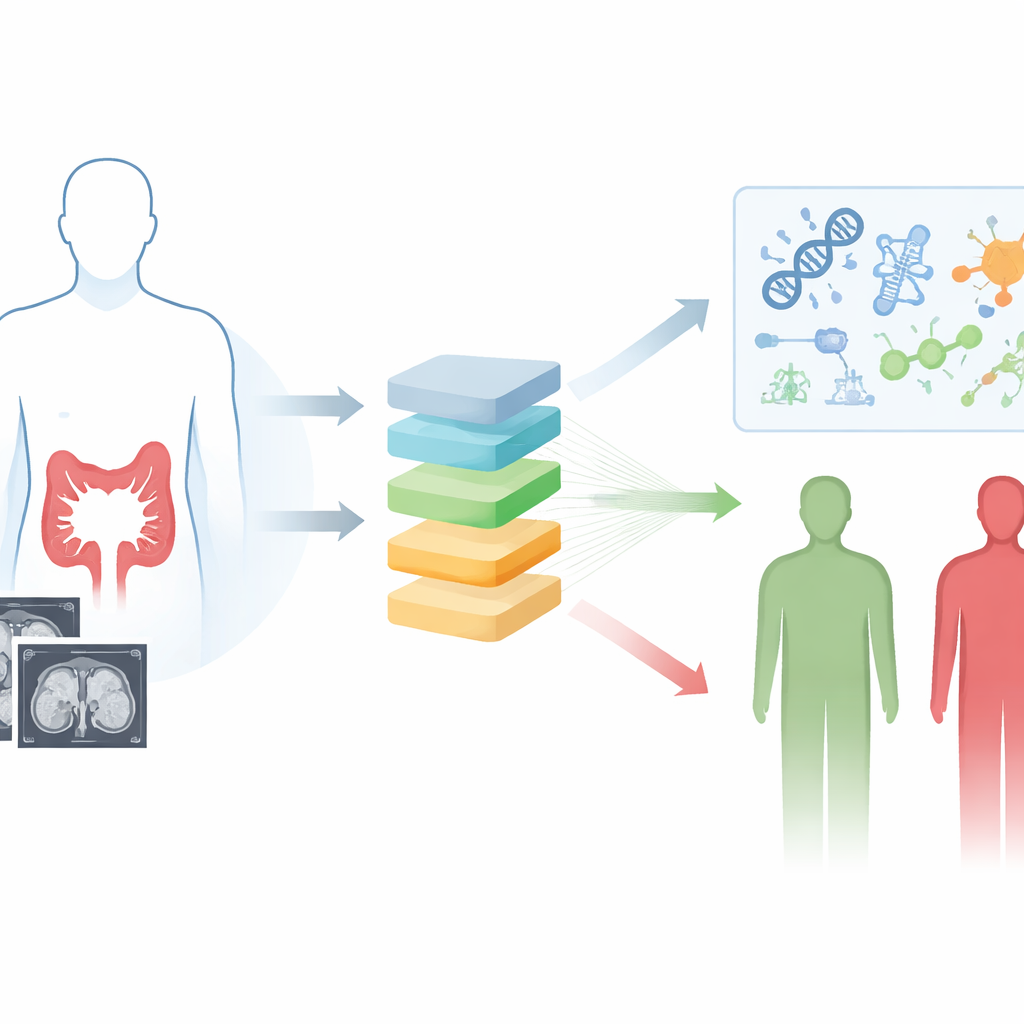
Explorer les tumeurs sans scalpel
Les chercheurs se sont concentrés sur les scans CT avec produit de contraste, un examen d’imagerie de routine déjà utilisé pour évaluer le cancer colorectal. Plutôt que de s’en remettre à ce que l’œil humain peut voir, ils ont utilisé la radiomique et l’apprentissage profond pour extraire près de 2 000 détails quantitatifs minuscules à partir des images, capturant des motifs subtils de forme et de texture reflétant l’hétérogénéité tumorale. Ils ont ensuite testé systématiquement 117 combinaisons de dix algorithmes d’apprentissage automatique pour trouver la manière la plus fiable de relier ces caractéristiques d’image à la durée de survie des patients. Le modèle retenu, qui combinait deux techniques appelées Lasso et gradient boosting, a produit un score de risque unique pour chaque personne basé uniquement sur son scanner préopératoire.
Séparer les patients à faible risque et à haut risque
En utilisant les scanners CT de 1 183 patients traités dans quatre hôpitaux, l’équipe a entraîné et testé de manière rigoureuse son modèle de radiomique par apprentissage profond. Ils ont identifié un seuil dans le score basé sur l’image qui a divisé les patients en groupes à faible risque et à haut risque. Dans l’ensemble de l’ensemble d’entraînement, un jeu de validation interne et deux hôpitaux indépendants, les patients à haut risque ont systématiquement vécu moins longtemps que ceux du groupe à faible risque. La capacité du modèle à distinguer les issues est restée robuste dans de nombreux sous-groupes, y compris chez les patients plus jeunes et plus âgés, les hommes et les femmes, les différents stades tumoraux et selon que les patients aient reçu ou non une chimiothérapie. Lorsque les chercheurs ont combiné le score issu des images avec deux indicateurs cliniques standards — le taux sérique d’ACE et le stade ganglionnaire — dans un outil graphique simple appelé nomogramme, les prédictions de survie à trois et cinq ans sont devenues encore plus précises et utiles en pratique clinique.
Qu’est-ce qui rend une tumeur plus dangereuse qu’une autre ?
Pour aller au-delà de la prédiction et comprendre pourquoi certaines tumeurs se comportent de façon plus agressive, l’équipe a relié les groupes de risque basés sur l’imagerie aux altérations moléculaires du cancer. Dans un sous‑groupe de patients, ils ont analysé de petites molécules dans le tissu tumoral par spectroscopie par résonance magnétique nucléaire et ont comparé les tumeurs aux tissus normaux adjacents. Ils ont trouvé que les tumeurs à haut risque et à faible risque présentaient des empreintes métaboliques distinctes, impliquant des voies liées aux acides aminés et aux acides gras à chaîne courte. Parallèlement, ils ont examiné l’activité génétique des tumeurs à partir d’une base de données d’imagerie publique. Les tumeurs à haut risque montraient des signaux marqués provenant de voies liées à la matrice extracellulaire — l’armature de soutien autour des cellules —, connue pour favoriser la dissémination des cellules cancéreuses et la résistance aux traitements. Les tumeurs à faible risque, en revanche, étaient enrichies en voies liées au système immunitaire et présentaient des niveaux plus élevés de cellules T CD8 cytotoxiques, ce qui suggère un microenvironnement anti-tumoral plus actif.
Voies métaboliques protectrices associées à une meilleure survie
Fait remarquable, les données métabolitiques et les données d’expression génique convergent vers les mêmes deux voies métaboliques — le métabolisme du butanoate et le métabolisme de l’azote — comme étant plus actives dans les tumeurs à faible risque. Ces voies sont liées à des produits de bactéries intestinales et à la manière dont les cellules traitent l’azote, ce qui influence l’équilibre énergétique et la fonction immunitaire. Lorsque les chercheurs ont vérifié un grand jeu de données indépendant de 417 patients atteints de cancer colorectal issu du Cancer Genome Atlas, ils ont constaté qu’une activité réduite de ces deux voies était clairement associée à une survie globale plus mauvaise. Cela suggère que le maintien de ces processus métaboliques pourrait contribuer à freiner la croissance tumorale ou à soutenir une réponse immunitaire plus efficace, et qu’ils pourraient un jour être explorés comme biomarqueurs ou cibles thérapeutiques.
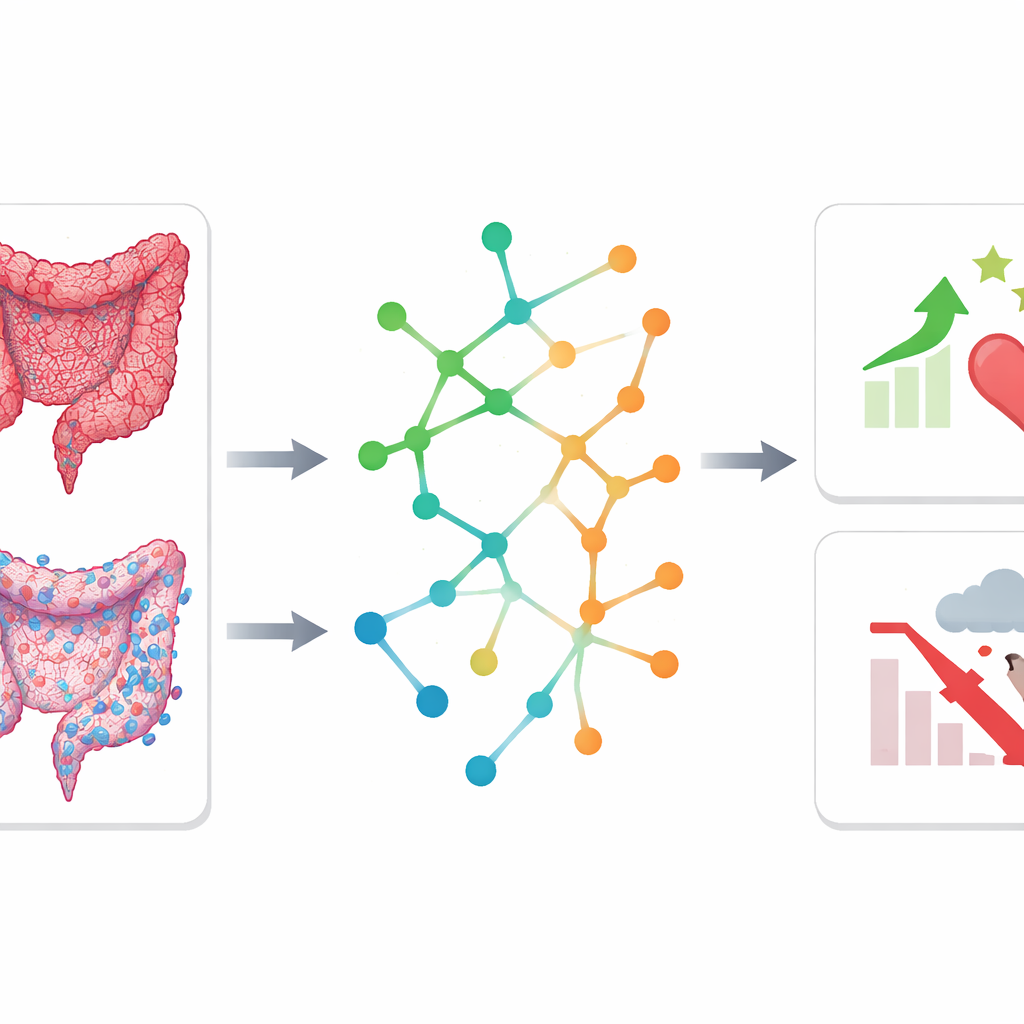
Ce que cela signifie pour les soins du cancer à l’avenir
En termes simples, cette étude montre que combiner une analyse intelligente des images avec un profilage moléculaire peut à la fois affiner les outils pronostiques et révéler ce qui se passe à l’intérieur des tumeurs colorectales. Un score de risque dérivé de scanners CT standards, surtout lorsqu’il est associé à des mesures cliniques de routine, pourrait aider les médecins à identifier quels patients nécessitent un traitement ou un suivi plus intensif après la chirurgie. Parallèlement, la découverte que certains profils immunitaires et voies métaboliques sont liés à de meilleurs résultats ouvre la voie à de nouvelles stratégies pour soutenir les défenses de l’organisme et concevoir des thérapies ciblées. Bien que des études prospectives plus larges soient nécessaires pour confirmer ces résultats, cette approche intégrative marque un pas vers des soins plus personnalisés et informés par la biologie pour les personnes atteintes d’un cancer colorectal.
Citation: Li, Z., Cai, R., Qin, Y. et al. Integration of radiomics, deep learning, transcriptomics, and metabolomics reveals prognostic risk stratification and underlying biological mechanisms in colorectal cancer. npj Precis. Onc. 10, 155 (2026). https://doi.org/10.1038/s41698-026-01331-2
Mots-clés: cancer colorectal, radiomique, apprentissage profond, métabolisme tumoral, microenvironnement immunitaire