Clear Sky Science · tr
Yeni fenotiazin-kromen hibrit bileşiklerin sentezi, antimikrobiyal değerlendirmesi, moleküler yerleştirme ve ilaç-benzeri özellik değerlendirmesi
Neden Yeni Mikroba Karşı Moleküller Önemli?
Antibiyotiğe dirençli enfeksiyonlar, bir zamanlar rutin olan hastalıkları ciddi tıbbi tehditlere dönüştürüyor. Bu çalışma, laboratuvarda üretilen ve üç tanınmış ilaç-benzeri yapı taşını tek bir iskelette birleştiren yeni bir molekül ailesini sunuyor. Araştırmacıların amacı, mevcut birçok ilacı etkisizleştirmeyi öğrenmiş bakteriler ve mantarları alt etmek. Çalışma, bu hibritlerin mikropları ne kadar iyi öldürdüğünü test etmekle kalmıyor; aynı zamanda ağızdan alınabilecek kadar “ilaç-benzeri” olup olmadıklarını ve mikropların içindeki ana direnç enziminin üzerine tutunup tutunmadıklarını da inceliyor.
Daha Akıllı Bir Molekül İnşa Etmek
Araştırma ekibi, mikropların hücre zarlarını bozduğu ve savunmalarını etkilediği bilinen bir kimyasal çekirdek olan fenotiazinden yola çıktı. Buna, kromen adı verilen halka biçimli birimler ve ilgili yapılar ile tiazoller, tiofenler ve pirazoller gibi ek halkalar oluşturabilen küçük parçalar eklendi. Aşamalı reaksiyonlarla bu parçalar kontrollü koşullar altında birleştirildi ve her ürün, istenen yapının oluştuğunu doğrulamak için atomik titreşimleri ve manyetik özellikleri okuyan standart tekniklerle kontrol edildi. Sonuçta, her biri halkaların ve yan grupların biraz farklı düzenine sahip küçük bir bileşik kütüphanesi elde edildi.
Mikroplara Karşı Ne Kadar Etkili Olduklarını Test Etmek
Yeni bileşikler daha sonra hastalık yapan mikroplardan oluşan bir panele karşı sınandı: E. coli gibi yaygın Gram-negatif bakteriler, Staphylococcus aureus ve Bacillus subtilis gibi Gram-pozitif türler ve iki sorunlu mantar, Candida albicans ile Fusarium oxysporum. Ekip, sıvı kültürde büyümeyi durdurmak için her bileşiğin gerekli olan en düşük miktarını ölçtü. Birkaç hibrit öne çıktı. 4 ve 7 etiketli iki aday, özellikle E. coliye karşı etkiliydi; büyümeyi durdurmak için yalnızca miligramın onda biri mertebesinde mikrogram/mL düzeylerinde miktar gerektirdiler—bazı testlerde referans bir antibiyotiğe denk veya ondan daha iyi sonuçlar verdiler. Başka bir bileşik olan 10, bitki ve fırsatçı insan patojeni olan Fusarium'a karşı en güçlü aktiviteyi gösterdi. Buna karşılık, sentezdeki daha basit bazı ara ürünler neredeyse etkisizdi; bu da sonundaki halka açısından zengin çerçevelerin etkinlik için kritik olduğunu vurguluyor.
Deney Tüpünden Olası Bir Hap Formuna
Uygun aktiviteye sahip olmak işin yalnızca yarısıdır; faydalı bir ilacın ayrıca vücutta doğru şekilde hareket etmesi gerekir. Bu nedenle araştırmacılar, her molekülü ağız yoluyla alımdan sonra emilme olasılığını tahmin eden yaygın “beş kuralı” (rule-of-five) yönergelerine karşı kontrol ettiler. Hibritlerin çoğu bu filtreleri geçti; moleküler ağırlıkları tercihen belirlenen sınırın yakınında veya biraz üzerindeydi ve hücre zarlarını aşmalarına izin verecek, ne çok yapışkan ne de çok hantal olmayan yağlılık ve suyla uyumlu özelliklerin bir dengesi vardı. Molekülün su ile etkileşimini gösteren bir ölçüm olan polar yüzey alanı hesapları, özellikle 5, 6, 8a, 8b ve 11 numaralı bazı adayların bağırsakta iyi emileceğini gösterdi.
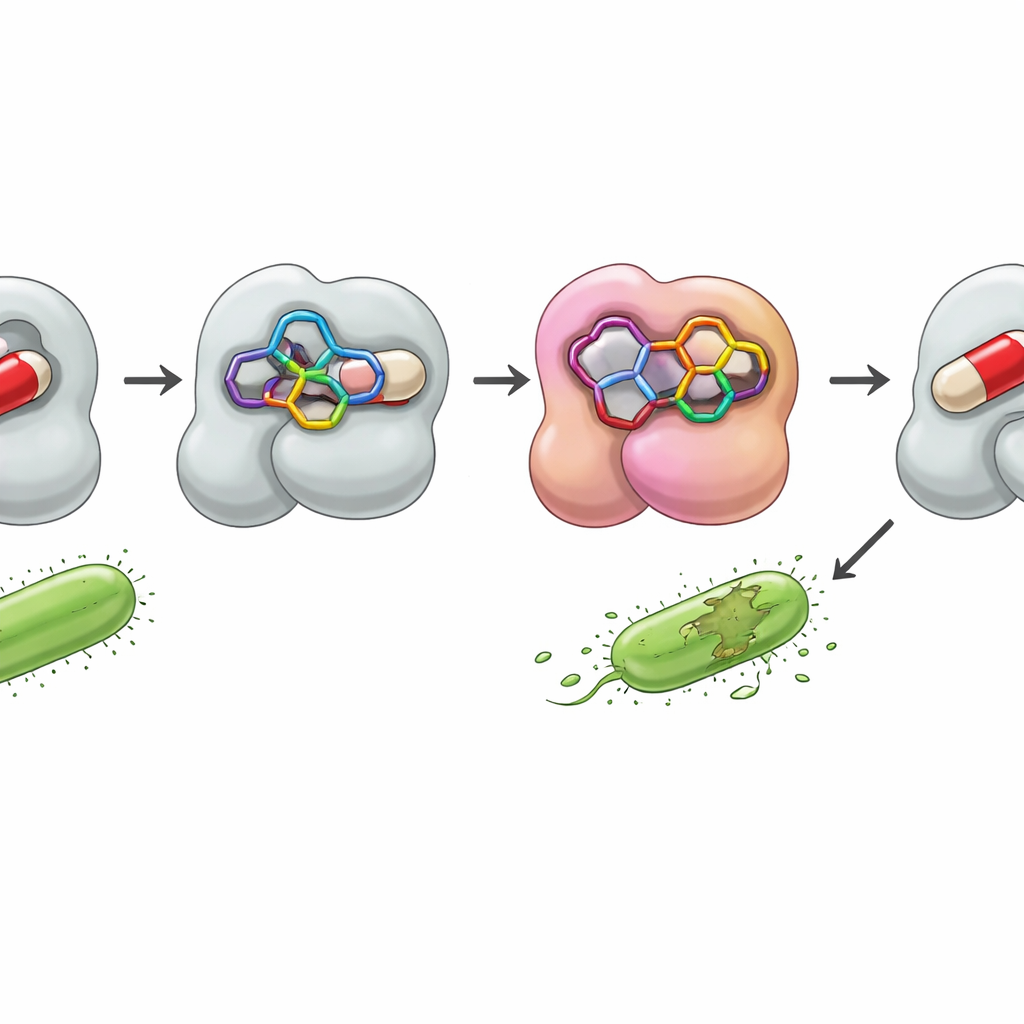
Bakteriyel Kalkanın İçine Bir Bakış
Bu hibritlerin direnci nasıl yenebileceğini keşfetmek için ekip, β-laktamaz adlı bir bakteriyel enzimle bilgisayar destekli yerleştirme (docking) çalışmalarına yöneldi. Birçok bakteri bu proteini bir kalkan olarak kullanıyor; β-laktam antibiyotikleri zarar vermeden önce parçalıyor. Yeni moleküllerin enzimin aktif cebinde nasıl konumlandığını modelleyerek bağlanma gücünü tahmin edebildiler ve önemli temas noktalarını haritalandırdılar. 7 numaralı bir bileşik, sitede özellikle iyi oturdu; birkaç aminoasitle stabilize edici etkileşimler kurdu ve hesaplanan bağlanma enerjisi, bilgisayar modellerinde referans ilaçlar ampisilin ve klotrimazolunkinden bile daha iyi çıktı. Diğer etkin molekül 4 de elverişli etkileşimler gösterdi. Biyolojik verilerin istatistiksel analizleri de bu eğilimleri destekledi ve 4, 7 ve 10 numaralı bileşikleri test edilen mikroplar arasında en tutarlı şekilde güçlü olanlar olarak gruplayıp öne çıkardı.
Gelecekteki Tedaviler İçin Anlamı Ne Olabilir?
Günlük ifadeyle bu çalışma, çok sayıda ilaç-dostu parçayı dikkatle tek bir düz, halka açısından zengin molekülde “birleştirmenin””, dirençli mikroplara güçlü darbeler indirebilen ve hap formu geliştirme için uygun görünen yeni adaylar üretebileceğini gösteriyor. En başarılı hibritler yalnızca çeşitli bakteri ve mantarların büyümesini yavaşlatmakla kalmadı, bilgisayar modellerinde mevcut ilaçlardan daha sıkı şekilde ana bir direnç enziminin içine sıkışıyor gibi göründü. Bu moleküller hâlâ laboratuvar aşamasında olup hayvan ve insan çalışmalarıyla güvenlik ve etkinlik açısından test edilmeleri gerekir; yine de hızla evrilen, çoklu ilaç direncine sahip patojenlerle başa çıkacak yeni nesil antibiyotikler için umut verici bir plan sunuyorlar.
Atıf: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Synthesis, antimicrobial evaluation, molecular docking, and drug-likeness assessment of novel phenothiazine chromene hybrid compounds. Sci Rep 16, 10592 (2026). https://doi.org/10.1038/s41598-026-43195-3
Anahtar kelimeler: antibiyotik direnci, antimikrobiyal ajanlar, fenotiazin hibritleri, moleküler yerleştirme, ilaç tasarımı