Clear Sky Science · he
סינתזה, הערכה אנטימיקרוביאלית, דוקינג מולקולרי והערכת דמוּת‑תרופה של תרכובות היברידיות חדשות של פנוטיאזין‑כרופן
מדוע מולקולות חדשות להלחם בזיהומים חשובות
זיהומים עמידים לאנטיביוטיקה הופכים מחלות שבעבר היו שגרתיות לאיומי בריאות משמעותיים. מחקר זה מדווח על משפחה חדשה של מולקולות מיוצרות במעבדה המשלבות שלושה כנויים מוכרים בעלי תכונות תרופתיות למבנה אחד. באמצעות מיזוג זה שואפים החוקרים לעלות על החיידקים והפטריות שלמדו להתגבר על תרופות רבות קיימות. העבודה לא רק בוחנת עד כמה ההיברידים האלה הורגים מיקרובים, אלא גם בודקת האם הם נראים דמוּת‑תרופה מספיק לספיגה דרך הפה והאם הם נקשרים לאנזים מרכזי המעורב בעמידות בתוך המיקרובים.
בניית מולקולה חכמה יותר
צוות המחקר התחיל מליבה כימית הנקראת פנוטיאזין, הידועה בהשבחת קרומי התא של מיקרובים ובהתערבות בהגנותיהם. אליה צירפו יחידות טבעתיות הנקראות כרופנים ומבנים קרובים, וכן קטעים קטנים המסוגלים ליצור טבעות נוספות כמו תיאזולים, תיופנים ופיראזולים. תגובות מדורגות קישרו בין החלקים האלה בתנאים מבוקרים, וכל תוצר נבדק בטכניקות סטנדרטיות שקוראות תנודות אטומיות והתנהגות מגנטית כדי לאשר שהמבנים הרצויים נוצרו. התוצאה הסופית היא ספרייה קטנה של מולקולות קרובות זו לזו, כל אחת עם סידור קל שונה של טבעות וקבוצות צדדיות.
בדיקה של יכולת ההלחמה בזיהומים
התרכובות החדשות נבדקו מול פאנל של מיקרובים גורמי מחלה: חיידקים גרם‑שליליים נפוצים כגון E. coli, מינים גרם‑חיוביים כמו Staphylococcus aureus ו‑Bacillus subtilis, ושתי פטריות מטרידות, Candida albicans ו‑Fusarium oxysporum. הצוות מדד את הכמות המזערית של כל תרכובת הנדרשת כדי לעכב גדילה בתרבית נוזלית. כמה היברידים בלטו. שני מועמדים, המסומנים 4 ו‑7, היו יעילים במיוחד נגד E. coli, ונזקקו לכמה עשרות מיקרוגרמים למיליליטר בלבד כדי לעצור גדילה — בקנה אחד עם או טובים יותר מאנטיביוטיקה התייחסותית בחלק מהבדיקות. תרכובת אחרת, 10, הראתה את הפעילות החזקה ביותר נגד Fusarium, פתוגן של צמחים וגם אופורטוניסטי לאדם. לעומת זאת, כמה מתווכים פשוטים יותר בסינתזה כמעט שלא הפעילו, מה שמדגיש שהמערכות הסופיות העשירות בטבעות הן קריטיות לעוצמה.
מבחנה אל לכדור אפשרי
פעילות מבטיחה היא רק חצי מהמאבק; תרופה שימושית גם צריכה לנוע בגוף בצורה נכונה. לכן החוקרים בדקו כל מולקולה ביחס להנחיות ה"כלל‑חמש" הנפוצות, המעריכות האם תרכובת צפויה להיספג לאחר מתן דרך הפה. רוב ההיברידים עברו סינון זה, עם משקלי מולקולריים קרובים או מעט מעל להגבלה המועדפת ואיזון של תכונות שומניות ומימיות שיאפשרו להם לעבור קרומי תאים מבלי להיות דביקים מדי או מגושמים מדי. חישובי שטח פני פולרי — מידה הקשורה למידת האינטראקציה של מולקולה עם מים — הצביעו על כך שכמה מועמדים, ובמיוחד התרכובות 5, 6, 8a, 8b ו‑11, צפויים להיספג היטב במעי.
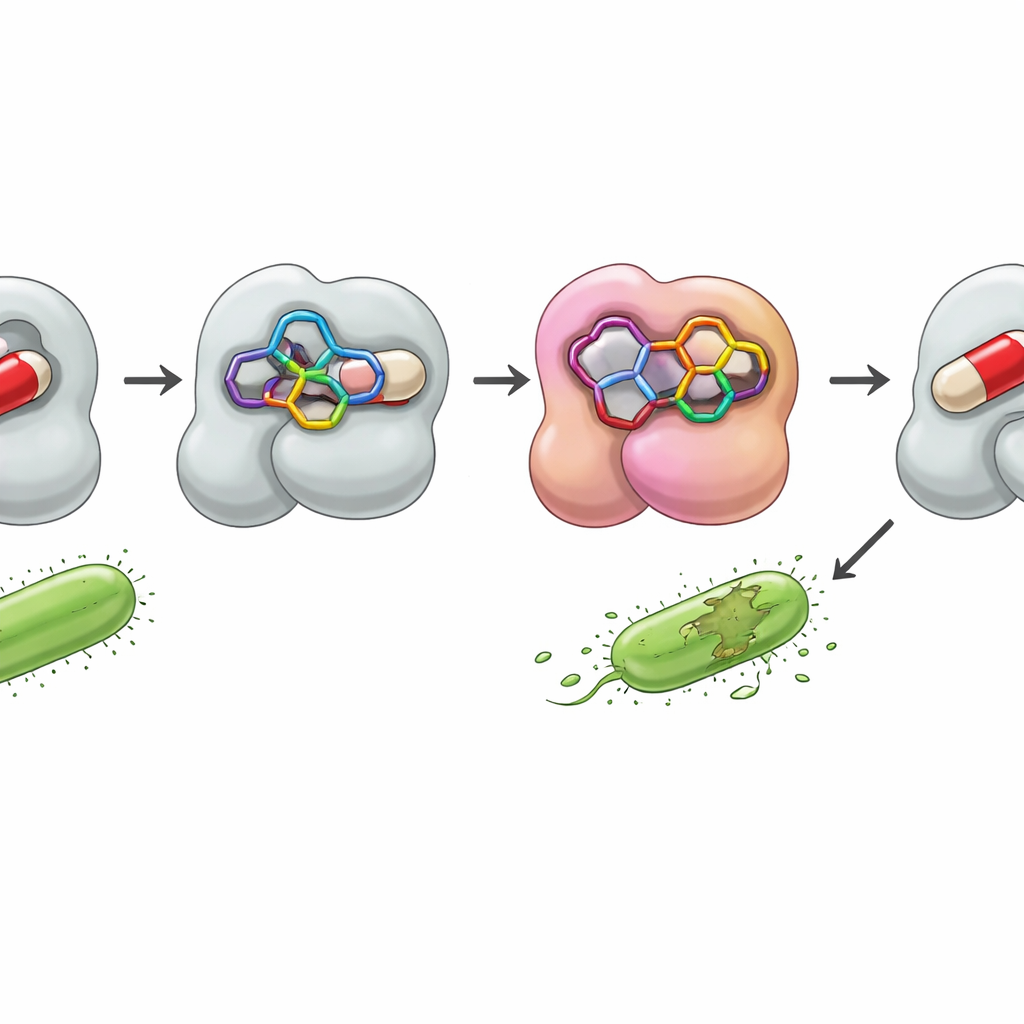
מציצים בתוך מגן החיידק
כדי לחקור כיצד היברידים האלה עשויים להתגבר על עמידות, פנה הצוות ללימודי דוקינג ממוחשבים עם אנזים חיידקי הנקרא β‑לקטמאז. חיידקים רבים משתמשים בחלבון זה כמגן, חותכים אנטיביוטיקות β‑לקטאם לפני שהן יכולות להזיק. על ידי דימוי איך המולקולות החדשות יושבות בכיס הפעיל של האנזים, יכלו החוקרים לאמוד עוצמת קשירה ולמפות קשרים מרכזיים. תרכובת אחת, 7, התמקמה במיוחד בנוחות באתר, יצרה אינטראקציות מייצבות עם מספר חומצות אמינו והגיעה לאנרגיית קשירה מחושבת אף טובה יותר מאשר של תרופות ההתייחסות אמפיצילין וקלו-טרימזול. תרכובת פעילה נוספת, 4, גם הראתה אינטראקציות מועילות. ניתוחים סטטיסטיים של הנתונים הביולוגיים החזיקו במגמות אלה, וקיבצו את התרכובות 4, 7 ו‑10 יחד כעוצמתיות התרכובות העקביות ביותר לאורך המיקרובים שנבדקו.
מה זה עשוי להשפיע על טיפולים עתידיים
באופן יומיומי, מחקר זה מראה כי חיבור מבוקר של מספר קטעים ידידותיים‑תרופה לתוך מולקולה שטוחה ועשירה בטבעות יכול להניב מועמדים חדשים שפוגעים חזק במיקרובים עמידים ונראים מתאימים לפיתוח ככדורים. ההיברידים המוצלחים לא רק האטו את גדילתם של מגוון חיידקים ופטריות, אלא גם נדמה שנתקעו בחוזקה בכיס של אנזים עמידות מרכזי במודלים ממוחשבים יותר מתרופות קיימות. למרות שהמולקולות הללו נמצאות עדיין בשלב מעבדתי מוקדם וצריך לבדוק את בטיחותן וביצועיהן בבעלי חיים ובאדם, הן מציעות תבנית מבטיחה לאנטיביוטיקות הדור הבא שמטרתן לתת קצב להתפתחות המהירה של פתוגנים רב‑עוקרים.
ציטוט: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Synthesis, antimicrobial evaluation, molecular docking, and drug-likeness assessment of novel phenothiazine chromene hybrid compounds. Sci Rep 16, 10592 (2026). https://doi.org/10.1038/s41598-026-43195-3
מילות מפתח: עמידות לאנטיביוטיקה, חומרי אנטימיקרוביאליים, היברידי פנוטיאזין, דוקינג מולקולרי, עיצוב תרופות