Clear Sky Science · ru
Синтез, оценка антимикробной активности, молекулярный докинг и оценка пригодности к лекарственным препаратам новых гибридных соединений фенотиазина и хромена
Почему важны новые противомикробные молекулы
Инфекции, устойчивые к антибиотикам, превращают когда‑то рутинные заболевания в серьёзные медицинские угрозы. В этом исследовании описывается новая семья лабораторно синтезированных молекул, которые объединяют три известных «лекарственных» фрагмента в единую структуру. Тем самым исследователи стремятся перехитрить бактерии и грибы, научившиеся игнорировать многие существующие препараты. Работа не только проверяет, насколько эффективно эти гибриды убивают микроорганизмы, но и изучает, насколько они соответствуют критериям «лекарственности» при приёме внутрь и способны ли они связываться с ключевым ферментом резистентности внутри микроорганизмов.
Создание более «умной» молекулы
Команда начала с химического ядра фенотиазина, уже известного тем, что нарушает мембраны микробных клеток и вмешивается в их защитные механизмы. К нему они прицепили кольцевые фрагменты — хромены и родственные структуры, а также более мелкие фрагменты, способные образовывать дополнительные кольца, такие как тиазолы, тиофены и пиразолы. Пошаговые реакции объединяли эти части в контролируемых условиях, и каждый продукт проверяли стандартными методами, считывающими колебания атомов и магнитные характеристики, чтобы подтвердить образование желаемых структур. В результате получилась небольшая библиотека родственных молекул, каждая с немного отличающимся расположением колец и боковых групп.
Проверка против микробов
Новые соединения подвергли испытаниям против панели патогенных микроорганизмов: обычных грамотрицательных бактерий, таких как E. coli, грамотрицательных видов вроде Staphylococcus aureus и Bacillus subtilis, а также двух проблемных грибов — Candida albicans и Fusarium oxysporum. Команда измеряла минимальную концентрацию каждого соединения, необходимую для остановки роста в жидкой культуре. Несколько гибридов выделялись. Два кандидата, обозначенные как 4 и 7, оказались особенно эффективны против E. coli, требуя лишь десятки микрограммов на миллилитр для подавления роста — сопоставимо или лучше референтного антибиотика в некоторых тестах. Другое соединение, 10, продемонстрировало наибольшую активность против Fusarium, патогена растений и оппортунистического человека. Напротив, некоторые более простые промежуточные продукты синтеза были почти неактивны, что подчёркивает важность окончательных насыщенных кольцевых каркасов для силы действия.
От пробирки к потенциальной таблетке
Многообещающая активность — лишь половина дела; полезное лекарство также должно правильно перемещаться по организму. Поэтому исследователи проверили каждую молекулу по широко применяемым рекомендациям «правила пяти», которые оценивают вероятность всасывания при пероральном приёме. Большинство гибридов прошли эти фильтры, имея массы молекул близкие к или чуть выше предпочтительного предела, а также баланс липофильных и гидрофильных свойств, что должно позволять им пересекать клеточные мембраны, не становясь слишком «липкими» или громоздкими. Расчёты полярной поверхностной площади — показателя, связанного со взаимодействием молекулы с водой — показали, что несколько кандидатов, в частности соединения 5, 6, 8a, 8b и 11, вероятно, будут хорошо всасываться в кишечнике.
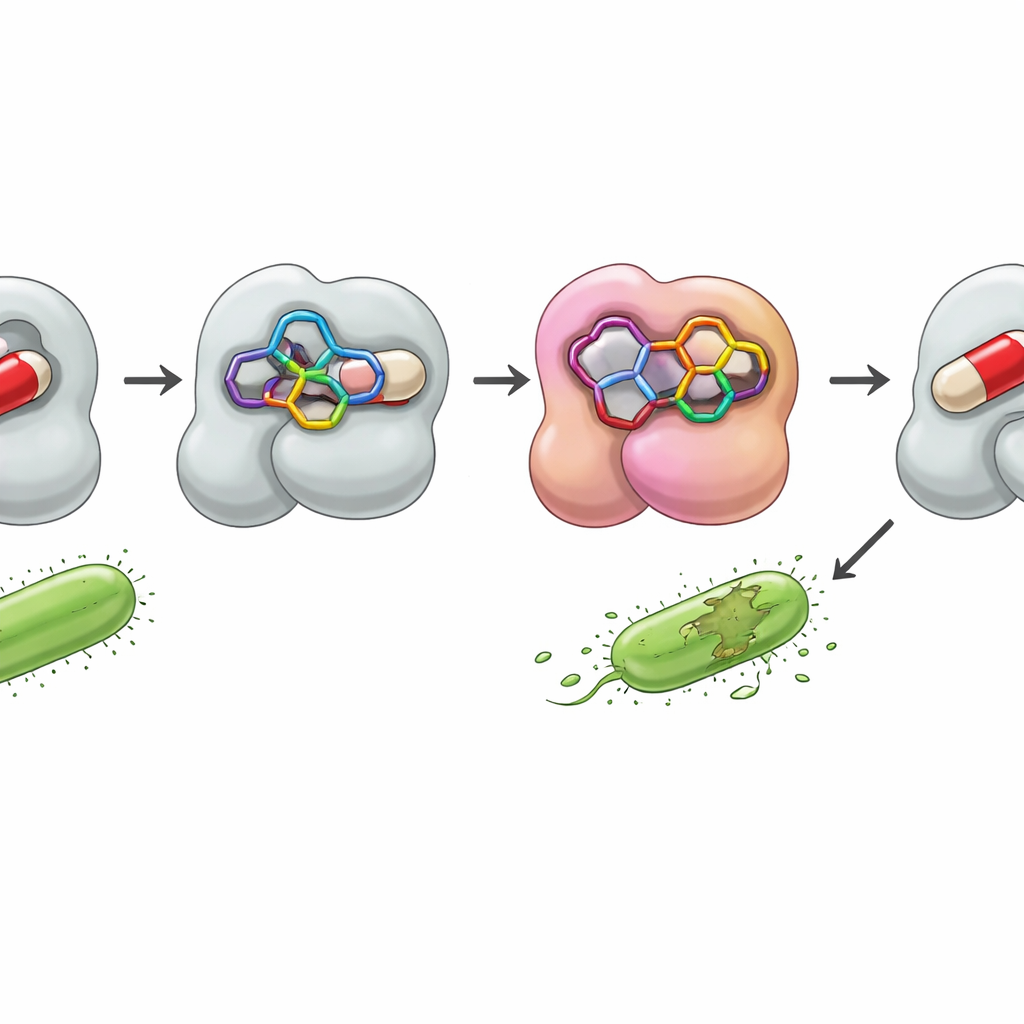
Заглядывая внутрь бактериального щита
Чтобы понять, как эти гибриды могут преодолевать резистентность, команда провела компьютерные докинг‑исследования с бактериальным ферментом β‑лактамазой. Многие бактерии используют этот белок как щит, разрезая β‑лактамные антибиотики прежде, чем те успеют нанести вред. Моделируя, как новые молекулы располагаются в активном кармане фермента, исследователи оценивали силу связывания и картировали ключевые контакты. Одно соединение, 7, расположилось особенно плотно в сайте, образуя стабилизирующие взаимодействия с несколькими аминокислотами и достигая рассчитанной энергии связывания даже лучше, чем у референтных препаратов ампициллина и клотримазола. Ещё одно активное соединение, 4, также показало благоприятные взаимодействия. Статистический анализ биологических данных подтвердил эти тенденции, объединив соединения 4, 7 и 10 в группу наиболее постоянно мощных в тестируемой панели микроорганизмов.
Что это может значить для будущих лечений
Проще говоря, это исследование демонстрирует, что аккуратное «сращивание» нескольких лекарственно благоприятных фрагментов в единую плоскую, насыщенную кольцами молекулу может породить новые кандидаты, которые одновременно эффективно действуют на устойчивые микроорганизмы и выглядят перспективно для разработки пероральных препаратов. Наиболее успешные гибриды не только замедляли рост ряда бактерий и грибов, но и в компьютерных моделях, по-видимому, надежнее встраивались в ключевой фермент резистентности, чем существующие лекарства. Хотя эти молекулы всё ещё находятся на ранней лабораторной стадии и должны быть проверены на безопасность и эффективности в животных и людях, они предлагают обнадёживающую схему для разработки антибиотиков следующего поколения, способных поспевать за быстро эволюционирующими многорезистентными патогенами.
Цитирование: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Synthesis, antimicrobial evaluation, molecular docking, and drug-likeness assessment of novel phenothiazine chromene hybrid compounds. Sci Rep 16, 10592 (2026). https://doi.org/10.1038/s41598-026-43195-3
Ключевые слова: антибиотикорезистентность, антимикробные агенты, гибриды фенотиазина, молекулярный докинг, дизайн лекарств