Clear Sky Science · pl
Synteza, ocena przeciwbakteryjna, dokowanie molekularne i ocena właściwości lekopodobnych nowych hybryd fenotiazyny i chromenu
Dlaczego nowe molekuły przeciwko zarazkom są ważne
Infekcje odporne na antybiotyki przekształcają kiedyś rutynowe schorzenia w poważne zagrożenia medyczne. W tym badaniu opisano nową rodzinę związków syntetycznych, które łączą trzy znane budulce o charakterze lekowym w jedną strukturę. Celem badaczy jest przechytrzenie bakterii i grzybów, które nauczyły się ignorować wiele istniejących leków. Praca nie tylko sprawdza, jak skuteczne są te hybrydy w zabijaniu drobnoustrojów, lecz także bada, czy mają właściwości „lekopodobne” umożliwiające podanie doustne oraz czy wiążą się z kluczowym enzymem oporności wewnątrz mikroorganizmów.
Budowanie mądrzejszej molekuły
Zespół badawczy zaczynał od rdzenia chemicznego nazwanego fenotiazyną, już znanego z zaburzania błon komórkowych drobnoustrojów i osłabiania ich mechanizmów obronnych. Do tego przyłączono jednostki pierścieniowe zwane chromenami oraz pokrewne struktury, a także mniejsze fragmenty zdolne do tworzenia dodatkowych pierścieni, takie jak tiazole, tiofeny i pyrazole. Krokowe reakcje łączyły te elementy w kontrolowanych warunkach, a każdy produkt weryfikowano standardowymi technikami odczytującymi drgania atomów i zachowanie magnetyczne, by potwierdzić powstanie oczekiwanych struktur. Efektem końcowym była niewielka biblioteka spokrewnionych związków, z nieco różnymi układami pierścieni i grup bocznych.
Badanie, jak dobrze zwalczają zarazki
Nowe związki poddano następnie próbom przeciwko panelowi patogennych drobnoustrojów: powszechnym bakteriom Gram‑ujemnym, takim jak E. coli, gatunkom Gram‑dodatnim, jak Staphylococcus aureus i Bacillus subtilis, oraz dwóm problematycznym grzybom, Candida albicans i Fusarium oxysporum. Zespół mierzył minimalne stężenie każdego związku zdolne zatrzymać wzrost w kulturze płynnej. Kilka hybryd wyróżniało się skutecznością. Dwa kandydaty, oznaczone jako 4 i 7, były szczególnie efektywne przeciwko E. coli, wymagając jedynie kilkudziesięciu mikrogramów na mililitr, by zahamować wzrost — na poziomie porównywalnym lub lepszym niż antybiotyk odniesienia w niektórych testach. Inny związek, 10, wykazał najsilniejsze działanie przeciwko Fusarium, patogenowi roślinnemu i oportunistycznemu dla ludzi. W przeciwieństwie do tego, niektóre prostsze pośrednie produkty syntezy były prawie nieaktywne, co podkreśla, że końcowe, bogate w pierścienie ramy są kluczowe dla mocy działania.
Z probówki do potencjalnej tabletki
Obiecująca aktywność to tylko połowa problemu; użyteczny lek musi także właściwie przemieszczać się w organizmie. Badacze sprawdzili więc każdy związek względem powszechnie stosowanych zasad „rule‑of‑five”, które szacują, czy związek prawdopodobnie zostanie wchłonięty po podaniu doustnym. Większość hybryd przeszła te filtry, z masami molowymi bliskimi lub nieco powyżej preferowanego limitu oraz balansem cech lipofilnych i hydrofilnych, który powinien pozwolić im przekraczać błony komórkowe bez nadmiernego „zlepiania się” czy zajmowania zbyt dużej objętości. Obliczenia policarbonowej (pola powierzchni polarnej) — miary związanej z siłą interakcji z wodą — sugerowały, że kilka kandydatów, w szczególności związki 5, 6, 8a, 8b i 11, powinno być dobrze wchłanialnych w jelitach.
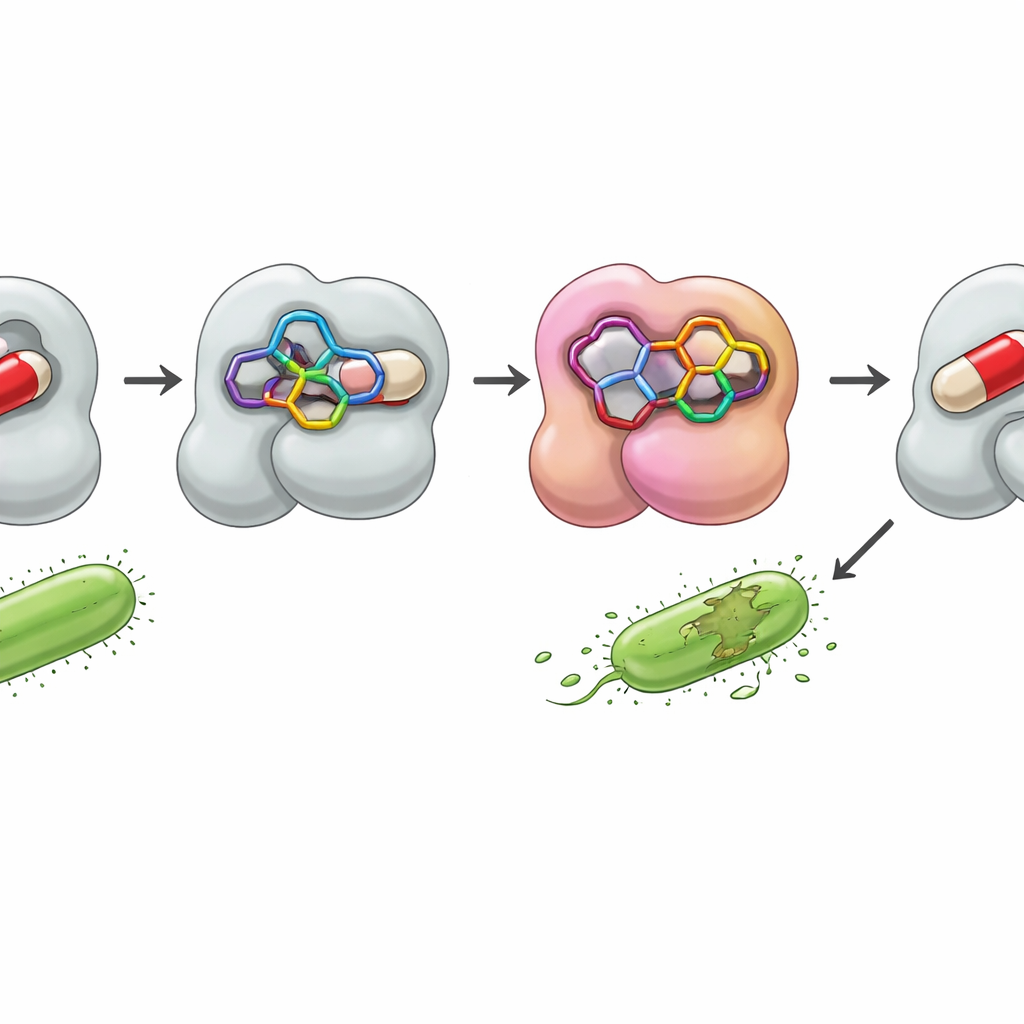
Wgląd w bakteryczną tarczę
Aby zbadać, jak te hybrydy mogłyby przełamać oporność, zespół przeprowadził komputerowe studia dokowania z bakteryjnym enzymem zwanym β‑laktamazą. Wiele bakterii używa tego białka jako tarczy, rozkładając antybiotyki β‑laktamowe, zanim zdążą wyrządzić szkody. Poprzez modelowanie, jak nowe molekuły mieszczą się w aktywnym leju enzymu, badacze mogli oszacować siłę wiązania i mapować kluczowe kontakty. Jeden związek, 7, ułożył się w miejscu szczególnie szczelnie, tworząc stabilizujące interakcje z kilkoma aminokwasami i osiągając obliczoną energię wiązania nawet lepszą niż w przypadku leków odniesienia, ampicyliny i klotrymazolu. Inny aktywny związek, 4, również wykazał korzystne interakcje. Analizy statystyczne danych biologicznych potwierdziły te trendy, grupując związki 4, 7 i 10 jako najsystematyczniej silne w badanym panelu drobnoustrojów.
Co to może znaczyć dla przyszłych terapii
Mówiąc prościej, badanie pokazuje, że staranne „połączenie” wielu fragmentów przyjaznych dla leków w jedną, płaską, bogatą w pierścienie molekułę może dać nowe kandydaty, które zarówno silnie atakują oporne drobnoustroje, jak i wyglądają na obiecujące do rozwoju jako doustne leki. Najbardziej udane hybrydy nie tylko spowolniły wzrost szeregu bakterii i grzybów, lecz także wydawały się klinować w kluczowym enzymie oporności mocniej niż istniejące leki w modelach komputerowych. Choć te molekuły są nadal na wczesnym, laboratoryjnym etapie i muszą zostać przebadane pod kątem bezpieczeństwa i skuteczności w modelach zwierzęcych i u ludzi, oferują obiecujący plan dla kolejnej generacji antybiotyków zaprojektowanych tak, by nadążyć za szybko ewoluującymi, wielolekowo opornymi patogenami.
Cytowanie: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Synthesis, antimicrobial evaluation, molecular docking, and drug-likeness assessment of novel phenothiazine chromene hybrid compounds. Sci Rep 16, 10592 (2026). https://doi.org/10.1038/s41598-026-43195-3
Słowa kluczowe: oporność na antybiotyki, środki przeciwdrobnoustrojowe, hybrydy fenotiazynowe, dokowanie molekularne, projektowanie leków