Clear Sky Science · tr
Bakterilerde nano‑mühendislikli RNA organellerinin ekspresyonu
Basit hücrelerin içindeki küçük fabrikalar
En mütevazı bakteriler bile şaşırtıcı sayıda kimyasal reaksiyon gerçekleştirir. Bilim insanları şimdi bu hücrelerin içine yeni, insan yapımı “iş istasyonları” eklemeyi öğreniyor — seçilmiş molekülleri yoğunlaştırabilen küçük damla‑benzeri bölmeler. Bu makale, bu tür bölmeleri normalde genetik mesajları taşıyan RNA’dan nasıl inşa edeceğini ve canlı bakteriler içinde bunları komutla görünür, kaybolur ve proteinleri yakalar hale getirmenin yollarını gösteriyor.
Duvardan yoksun damlalar
Birçok hücre, kimyasını membransız organeller kullanarak düzenler — proteinler ve nükleik asitlerden oluşan, faz ayrışmasıyla meydana gelen damlalar; su içindeki yağ damlalarına benzerler. Bakteriler eskiden içsel yapı için çok basit sanılıyordu, ama onlar da DNA kopyalanması, stres yanıtları ve daha fazlasını kontrol etmek için benzer damlalar kullanır. Araştırmacılar, metabolizmayı yönlendirmek, yararlı ürünleri bir araya getirmek veya doğal damlaların nasıl çalıştığını incelemek için yapay sürümler tasarlamayı umuyor. Mevcut sentetik sistemlerin çoğu öngörülmesi ve tasarlanması zor olan düzensiz proteinlere dayanır.
Programlanabilir RNA şekilleriyle inşa etmek
Yazarlar bunun yerine nükleik asitlerin öngörülebilir baz‑eşleşme kurallarını kullanan RNA nanoteknolojisine yöneliyor. Dört kollu, uçlarında kısa döngüler taşıyan “nano‑yıldızlar” tasarladılar; bu döngüler birbirine uyumlu döngülerle eşleşebiliyor. A ve B adlı iki tasarımın her biri kendi içinde tamamlayıcı döngülere sahip, böylece aynı tür nano‑yıldızlar birbirini çekip yoğunlaşarak damlalar oluşturuyor. Karışık (scrambled) versiyonlar bu tamamlayıcılıktan yoksun olup çözünmüş halde kalmalıydı. Ekip, bu nano‑yıldızların genetik şablonlarını E. coli'ye yerleştirdi ve yapıları mikroskop altında görülebilir kılmak için floresan RNA etiketleri kullandı.
Canlı bakteriler içinde tasarımcı damlalar
Nano‑yıldız A veya B ifade edildiğinde, bakteriyel hücrelerin içinde parlak damlalar belirdi; çoğunlukla kutuplarda oluşuyordu. Floresans desenlerinin ve zaman atlamalı filmlerin analizi, çoğu hücrede iki veya üç damla bulunduğunu, bunların birleşip yeniden büyüyebildiğini ve küçük sıvılar gibi davrandığını gösterdi. Buna karşılık, karışık tasarımlar yalnızca aralıklı zayıf kümelenme ile difüz bir parlaklık üretti; bu da damla oluşumunun özgül baz‑eşleşme ile tetiklendiğini doğruladı. Doğal RNA kesici enzimler bazı nano‑yıldız kollarını kırmasına rağmen, dört ve üç kollu yeterli yapı yoğunlaşmayı sürdürecek kadar kaldı; bu durum tasarımın dayanıklılığını vurguluyor.
Birden çok damla türü ve protein yakalama
A ve B nano‑yıldızları yalnızca kendi türlerini tanıdığı için, her ikisini de üreten hücreler aynı bakteride karışmayan iki damla türü üretti. Bu damlalar genellikle hücrenin zıt uçlarında olmak üzere büyük ölçüde ayrı kaldı. Yazarlar sonra yeni bir özellik ekledi: nanoyıldız A içinde yeşil floresan protein (GFP) bağlayan kısa bir RNA aptameri. Bakteriler hem modifiye nano‑yıldızları hem de GFP’yi ürettiğinde, protein damlaların içinde güçlü şekilde yoğunlaştı; aptameri olmayan kontrol hücrelerinde ise eşit şekilde dağılmış halde kaldı. Fotoblekleme sonrası floresansın toparlanması ölçümleri, GFP ve nano‑yıldızların her ikisinin de çevre sitoplazma ile alışverişi sürdürdüğünü gösterdi; bu da yine sıvı‑benzeri bir duruma işaret etti.
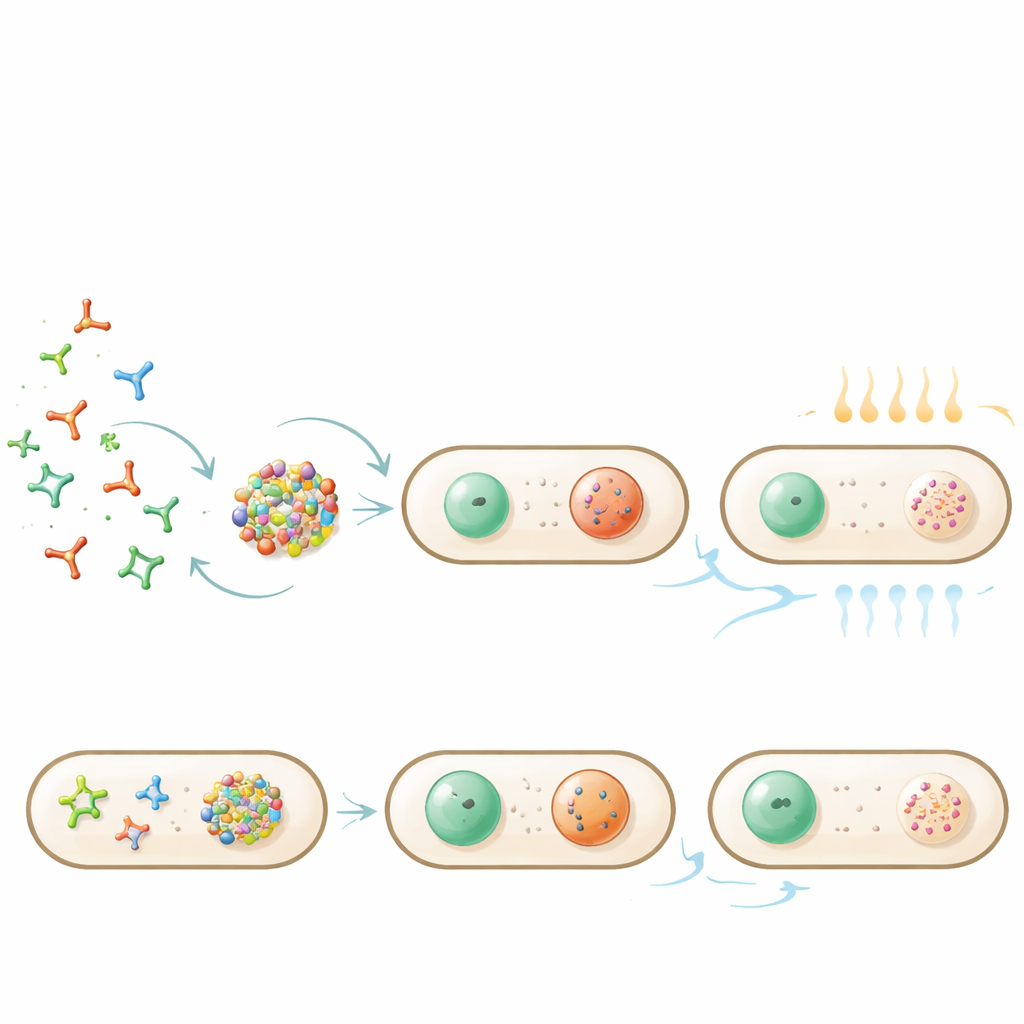
Damlaları ısıyla açıp kapamak
Nano‑yıldızlar baz‑eşleşmesiyle bir arada tuttuğundan, sıcaklık basit bir kontrol düğmesi sağlar. Bakterilerin hafifçe ısıtılması, baz eşleşmeleri erirken damlaların çözünmesine neden oldu; soğutma bunların kutupsal pozisyonlarında yeniden ortaya çıkmasını sağladı. Kesin “erime” sıcaklığı nano‑yıldız tasarımına ve ne kadar enzimatik kırılma olduğuna bağlıydı, ama süreç birçok hücre için geri döndürülebilir şekilde devam etti. Yakalanmış GFP içeren damlalar daha güçlü ısıtıldığında hem RNA hem de protein hücre boyunca dağıldı; soğutma sonrası damlalar yeniden oluştu ve proteini tekrar yoğunlaştırdı — bu, yükün basit bir termal döngüyle serbest bırakılabileceği ve tekrar tutulabileceğini gösterdi.
Gelecekte hücre mühendisliği için anlamı
Günlük ifadeyle, araştırmacılar bakteriler içinde programlanabilir, RNA‑temelli “açılır‑kapanır odacıklar” inşa ettiler — çoğaltılabilen, ayrı tutulabilen, seçilmiş araçlarla doldurulabilen ve istenince katlanıp saklanabilen odacıklar. Temel etkileşimler basit ve tasarlanabilir olduğundan, bu sentetik organeller metabolik yolları yönlendirmek, toksik ara ürünleri izole etmek veya doğal damlaların yaşamın kimyasını nasıl kontrol ettiğini incelemek için esnek bir yol sunuyor. Çalışma, nano‑mühendislikli RNA yoğunlaşmalarının gelecek nesil mikrobiyal fabrikaların temel bileşenleri ve hücresel davranışı yeniden şekillendirmek için güçlü araçlar haline gelebileceğini öne sürüyor.
Atıf: Ng, B., Fan, C., Dordevic, M. et al. Expression of nano-engineered RNA organelles in bacteria. Nat Commun 17, 2752 (2026). https://doi.org/10.1038/s41467-026-69336-w
Anahtar kelimeler: sentetik organeller, RNA nanoteknolojisi, biyomoleküler yoğunlaşmalar, bakteriyel hücre mühendisliği, metabolik mühendislik