Clear Sky Science · fr
Expression d’organelles en ARN nano‑ingénierées dans des bactéries
Petites usines à l’intérieur de cellules simples
Même les bactéries les plus humbles réalisent un nombre stupéfiant de réactions chimiques. Les scientifiques apprennent désormais à ajouter de nouvelles « stations de travail » artificielles à l’intérieur de ces cellules : de minuscules compartiments en forme de goutte qui peuvent concentrer des molécules choisies. Cet article montre comment construire de tels compartiments à partir d’ARN, le même type de molécule qui porte normalement les messages génétiques, et comment les faire apparaître, disparaître et capturer des protéines sur commande à l’intérieur de bactéries vivantes.
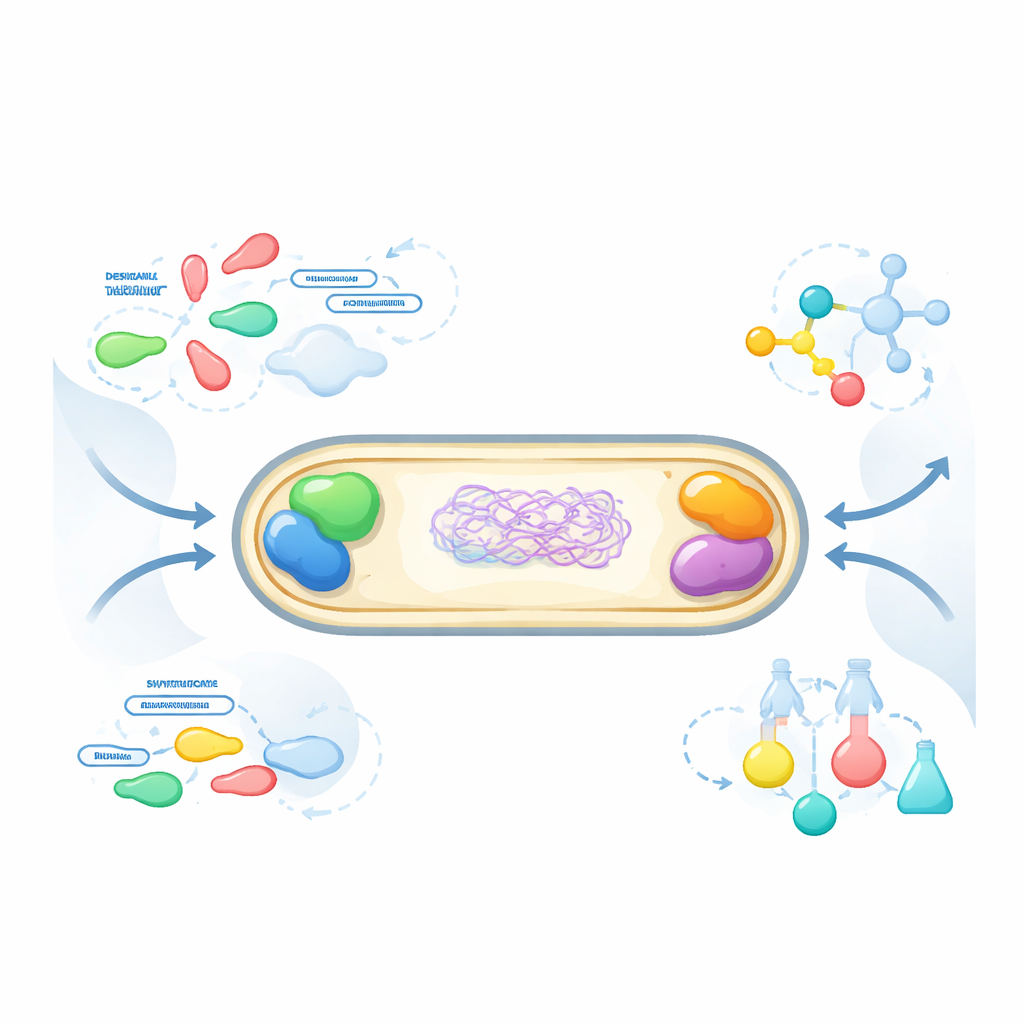
Des gouttes sans parois
De nombreuses cellules organisent leur chimie en utilisant des organelles sans membrane — des gouttes de protéines et d’acides nucléiques qui se forment par séparation de phase, un peu comme des gouttes d’huile dans l’eau. On pensait autrefois que les bactéries étaient trop simples pour ce type de structure interne, mais elles utilisent aussi des gouttes similaires pour contrôler la réplication de l’ADN, les réponses au stress, et plus encore. Les chercheurs espèrent concevoir des versions artificielles de ces compartiments pour orienter le métabolisme, assembler des produits utiles ou étudier le fonctionnement des gouttes naturelles. Les systèmes synthétiques existants reposent souvent sur des protéines désordonnées, dont les interactions adhésives sont difficiles à prédire et à maîtriser.
Construire avec des formes d’ARN programmables
Les auteurs se tournent plutôt vers la nanotechnologie ARN, qui exploite les règles prévisibles d’appariement des bases des acides nucléiques. Ils ont conçu des « nanostars » : des jonctions ARN à quatre bras dont les extrémités portent de courtes boucles capables de s’apparier avec des boucles complémentaires sur d’autres nanostars. Deux conceptions, appelées A et B, ont chacune des boucles auto‑complémentaires, de sorte que les nanostars du même type s’attirent et se condensent en gouttes. Des versions mélangées (scrambled) n’ont pas cette complémentarité et devraient rester dissoutes. L’équipe a inséré des plans génétiques pour ces nanostars dans E. coli, en utilisant des marqueurs fluorescents sur l’ARN pour pouvoir observer les structures au microscope.
Gouttes conçues à l’intérieur de bactéries vivantes
Lorsque les nanostars A ou B étaient exprimés, des gouttes lumineuses apparaissaient à l’intérieur des cellules bactériennes, principalement aux pôles. L’analyse des motifs de fluorescence et des films en temps‑réel a montré que la plupart des cellules contenaient deux ou trois gouttes pouvant fusionner et repousser, se comportant comme de petits liquides. En revanche, les modèles mélangés produisaient une lueur diffuse avec seulement des agrégats faibles et rares, confirmant que l’appariement spécifique des bases pilote la formation des gouttes. Malgré le fait que des enzymes naturelles coupent certains bras des nanostars, suffisamment de structures à quatre et trois bras restaient pour maintenir une condensation robuste, soulignant la résilience du design.
Plusieurs types de gouttes et capture de protéines
Parce que les nanostars A et B ne reconnaissent que leur propre type, les cellules conçues pour produire les deux ont généré deux types de gouttes non miscibles dans la même bactérie. Celles‑ci restaient majoritairement séparées dans l’espace, souvent aux extrémités opposées de la cellule. Les auteurs ont ensuite ajouté une nouvelle fonctionnalité : un court aptamère ARN dans le nanostar A qui se lie à la protéine fluorescente verte (GFP). Lorsque les bactéries produisaient à la fois les nanostars modifiés et la GFP, la protéine s’est fortement concentrée à l’intérieur des gouttes, tandis que dans les cellules témoins sans l’aptamère elle restait uniformément répartie. Les mesures de récupération de fluorescence après photoblanchiment ont révélé que la GFP et les nanostars continuaient d’échanger avec le cytoplasme environnant, ce qui correspond encore à un état de type liquide.
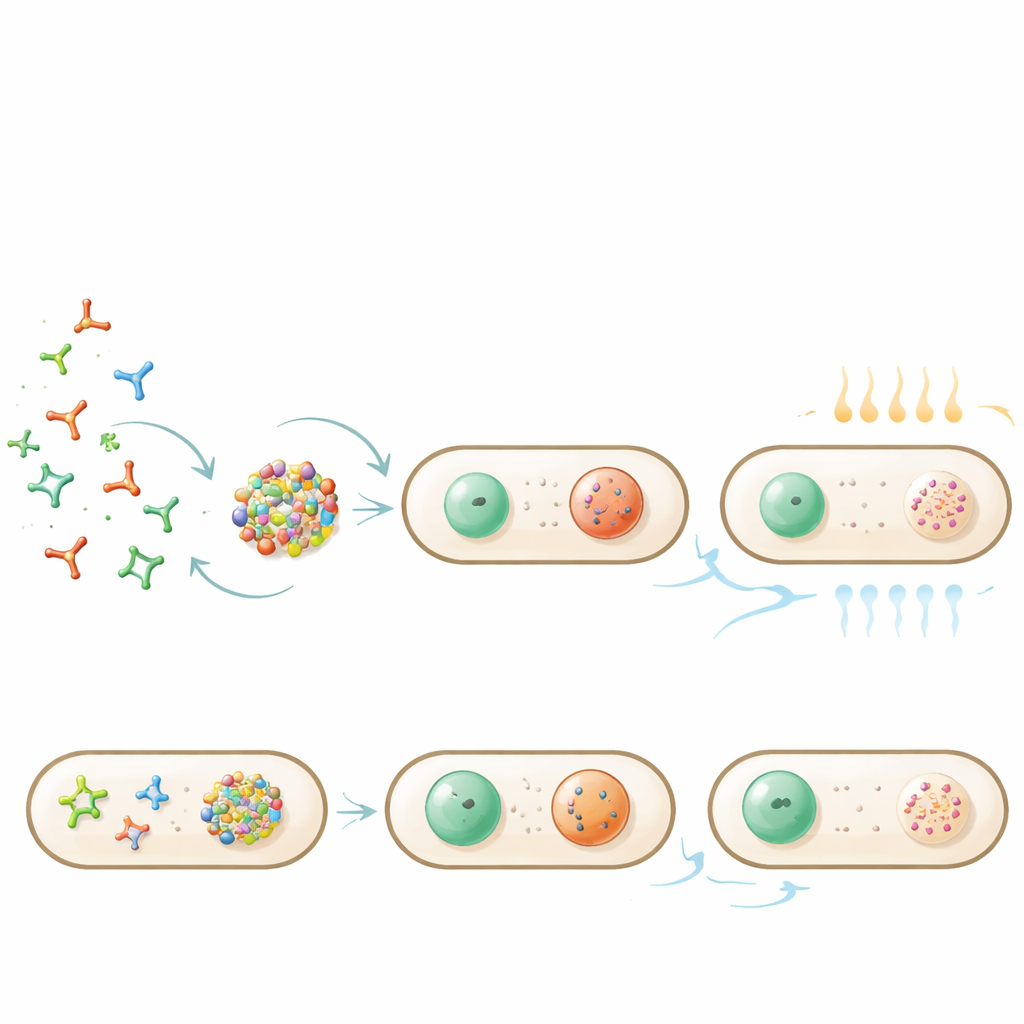
Allumer et éteindre les gouttes par la chaleur
Comme les nanostars s’assemblent par appariement des bases, la température offre un moyen de contrôle simple. Un léger chauffage des bactéries provoquait la dissolution des gouttes lorsque les appariements fondaient ; le refroidissement les faisait réapparaître à leurs positions polaires habituelles. La température de « fusion » précise dépendait du design du nanostar et du degré de rognage enzymatique subi, mais le processus restait réversible pour de nombreuses cellules. Lorsque des gouttes contenant la GFP capturée étaient chauffées plus fortement, à la fois l’ARN et la protéine se dispersaient dans toute la cellule ; après refroidissement, les gouttes se reformaient et concentraient à nouveau la protéine, montrant que la cargaison peut être relâchée puis re‑séquestrée par un simple cycle thermique.
Ce que cela signifie pour l’ingénierie cellulaire future
Concrètement, les chercheurs ont construit des « pièces pop‑up » programmables à base d’ARN à l’intérieur des bactéries — des pièces qui peuvent être dupliquées, maintenues séparées, remplies d’outils sélectionnés et repliées à la demande. Parce que les interactions sous‑jacentes sont simples et concevables, ces organelles synthétiques offrent un moyen flexible de diriger des voies métaboliques, d’isoler des intermédiaires toxiques ou d’explorer comment les gouttes naturelles contrôlent la chimie du vivant. Ce travail suggère que des condensats ARN nano‑ingénierés pourraient devenir des composants centraux des usines microbiennes de nouvelle génération et des outils puissants pour remodeler le comportement cellulaire.
Citation: Ng, B., Fan, C., Dordevic, M. et al. Expression of nano-engineered RNA organelles in bacteria. Nat Commun 17, 2752 (2026). https://doi.org/10.1038/s41467-026-69336-w
Mots-clés: organelles synthétiques, nanotechnologie ARN, condensats biomoléculaires, ingénierie des cellules bactériennes, ingénierie métabolique