Clear Sky Science · de
Expression nano‑konstruktierter RNA‑Organelle in Bakterien
Kleine Fabriken in einfachen Zellen
Sogar die unscheinbarsten Bakterien führen eine beeindruckende Vielzahl chemischer Reaktionen durch. Wissenschaftler lernen nun, neue, von Menschen gemachte „Arbeitsstationen“ in diesen Zellen einzubauen — winzige, tropfenartige Kompartimente, die ausgewählte Moleküle konzentrieren können. Diese Arbeit zeigt, wie man solche Kompartimente aus RNA baut, jener Molekülart, die normalerweise genetische Botschaften trägt, und wie man sie in lebenden Bakterien auf Befehl erscheinen, verschwinden und Proteine binden lassen kann.
Tropfen ohne Membran
Viele Zellen organisieren ihre Chemie mit membranlosen Organellen — Tröpfchen aus Proteinen und Nukleinsäuren, die durch Phasentrennung entstehen, ähnlich wie Öltröpfchen in Wasser. Man hielt Bakterien einst für zu einfach für solche interne Strukturen, doch auch sie nutzen ähnliche Tröpfchen, um DNA‑Replikation, Stressantworten und mehr zu steuern. Forscher hoffen, künstliche Versionen dieser Kompartimente zu entwerfen, um Stoffwechselwege zu lenken, nützliche Produkte zu assemblieren oder zu untersuchen, wie natürliche Tröpfchen funktionieren. Bestehende synthetische Systeme beruhen oft auf ungeordneten Proteinen, deren klebrige Wechselwirkungen schwer vorherzusagen und zu entwerfen sind.
Bauen mit programmierbaren RNA‑Formen
Die Autorinnen und Autoren wenden sich stattdessen der RNA‑Nanotechnologie zu, die die vorhersagbaren Basenpaarungsregeln der Nukleinsäuren ausnutzt. Sie entwarfen „Nanostars“: vierarmige RNA‑Junctions, deren Spitzen kurze Schleifen tragen, die mit passenden Schleifen anderer Nanostars paaren können. Zwei Designs, genannt A und B, besitzen jeweils selbstkomplementäre Schleifen, sodass Nanostars desselben Typs sich anziehen und zu Tröpfchen kondensieren. Gezinkte Versionen fehlen diese Komplementarität und sollten gelöst bleiben. Das Team fügte genetische Baupläne für diese Nanostars in E. coli ein und verwendete fluoreszierende RNA‑Tags, damit die Strukturen im Mikroskop sichtbar wurden.
Designer‑Tröpfchen in lebenden Bakterien
Wenn Nanostars A oder B exprimiert wurden, erschienen helle Tröpfchen in den Bakterienzellen, meist an den Polen. Analysen der Fluoreszenzmuster und Zeitrafferaufnahmen zeigten, dass die meisten Zellen zwei oder drei Tröpfchen enthielten, die verschmelzen und wieder nachwachsen konnten und sich wie kleine Flüssigkeiten verhielten. Im Gegensatz dazu erzeugten die gezinkten Designs ein diffus leuchtendes Signal mit nur gelegentlicher schwacher Clusterbildung, was bestätigt, dass spezifische Basenpaarung die Tröpfchenbildung antreibt. Trotz natürlicher RNA‑schneidender Enzyme, die einige Nanostar‑Arme abschneiden, blieben genügend vier‑ und dreiflügelige Strukturen erhalten, um eine robuste Kondensation zu ermöglichen — ein Hinweis auf die Belastbarkeit des Designs.
Mehrere Tröpfchentypen und Proteinaufnahme
Da A‑ und B‑Nanostars nur ihren eigenen Typ erkennen, produzierten Zellen, die beide herstellten, zwei nicht mischbare Tröpfchentypen in derselben Bakterie. Diese blieben weitgehend räumlich getrennt, häufig an gegenüberliegenden Zellenden. Die Autoren fügten dann eine neue Funktion hinzu: ein kurzes RNA‑Aptamer in Nanostar A, das an grünes fluoreszierendes Protein (GFP) bindet. Wenn Bakterien sowohl die modifizierten Nanostars als auch GFP produzierten, konzentrierte sich das Protein stark in den Tröpfchen, während es in Kontrollzellen ohne Aptamer gleichmäßig verteilt blieb. Messungen der Fluoreszenzwiederherstellung nach Photobleichung zeigten, dass GFP und Nanostars weiterhin mit dem umgebenden Zytoplasma ausgetauscht wurden, was erneut für einen flüssigkeitsähnlichen Zustand spricht.
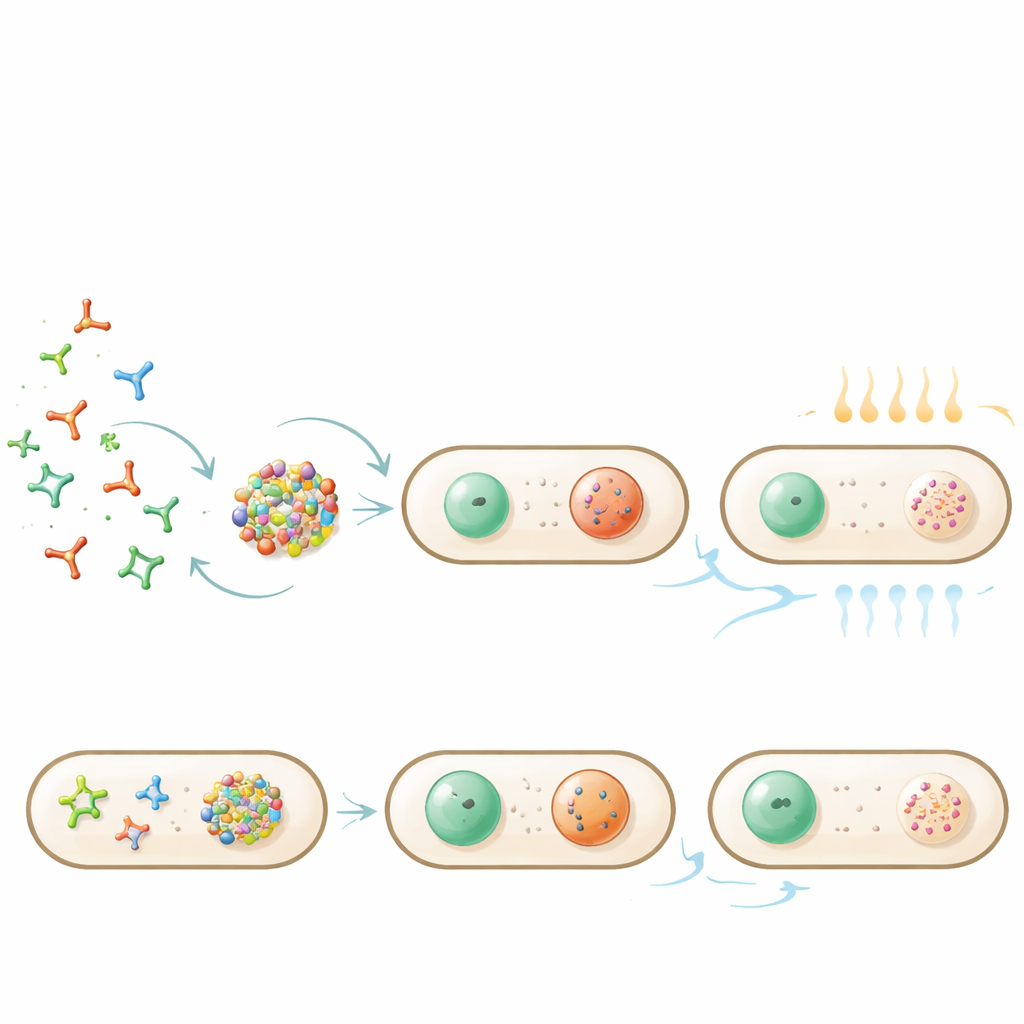
Tröpfchen mit Hitze an‑ und ausschalten
Weil die Nanostars durch Basenpaarung zusammenkleben, bietet die Temperatur einen einfachen Regelknopf. Sanftes Erwärmen der Bakterien ließ die Tröpfchen verschwinden, als die Basenpaare schmolzen; Abkühlung ließ sie an ihren üblichen Polstellen wieder erscheinen. Die genaue „Schmelz“temperatur hing vom Nanostar‑Design und vom Ausmaß enzymatischer Beschneidung ab, aber der Prozess blieb für viele Zellen reversibel. Wenn Tröpfchen mit gebundenem GFP stärker erhitzt wurden, verteilten sich sowohl RNA als auch Protein im ganzen Zellinneren; nach dem Abkühlen bildeten sich die Tröpfchen wieder und konzentrierten das Protein erneut, was zeigt, dass Ladung durch einen einfachen thermischen Zyklus freigegeben und wieder restriktiert werden kann.
Was das für die künftige Zelltechnik bedeutet
Alltäglich ausgedrückt haben die Forschenden programmierbare, RNA‑basierte „Pop‑up‑Räume“ in Bakterien gebaut — Räume, die dupliziert, getrennt gehalten, mit ausgewählten Werkzeugen gefüllt und bei Bedarf wieder eingeklappt werden können. Da die zugrunde liegenden Wechselwirkungen einfach und entwerfbar sind, bieten diese synthetischen Organellen eine flexible Möglichkeit, Stoffwechselwege zu lenken, toxische Zwischenprodukte zu isolieren oder zu erforschen, wie natürliche Tröpfchen die Chemie des Lebens steuern. Die Arbeit legt nahe, dass nano‑konstruktierte RNA‑Kondensate zu Kernkomponenten der nächsten Generation mikrobieller Fabriken und zu mächtigen Werkzeugen zur Umgestaltung zellulären Verhaltens werden könnten.
Zitation: Ng, B., Fan, C., Dordevic, M. et al. Expression of nano-engineered RNA organelles in bacteria. Nat Commun 17, 2752 (2026). https://doi.org/10.1038/s41467-026-69336-w
Schlüsselwörter: synthetische Organellen, RNA‑Nanotechnologie, biomolekulare Kondensate, bakterielle Zelltechnik, Stoffwechseltechnik