Clear Sky Science · es
Expresión de orgánulos de ARN nanoingenierizados en bacterias
Fábricas diminutas dentro de células simples
Incluso las bacterias más humildes realizan una asombrosa cantidad de reacciones químicas. Los científicos están aprendiendo a añadir nuevas “estaciones de trabajo” artificiales dentro de estas células: pequeños compartimentos en forma de gotas que pueden concentrar moléculas específicas. Este artículo muestra cómo construir esos compartimentos a partir de ARN, el mismo tipo de molécula que normalmente transporta mensajes genéticos, y cómo hacer que aparezcan, desaparezcan y capturen proteínas por demanda dentro de bacterias vivas.
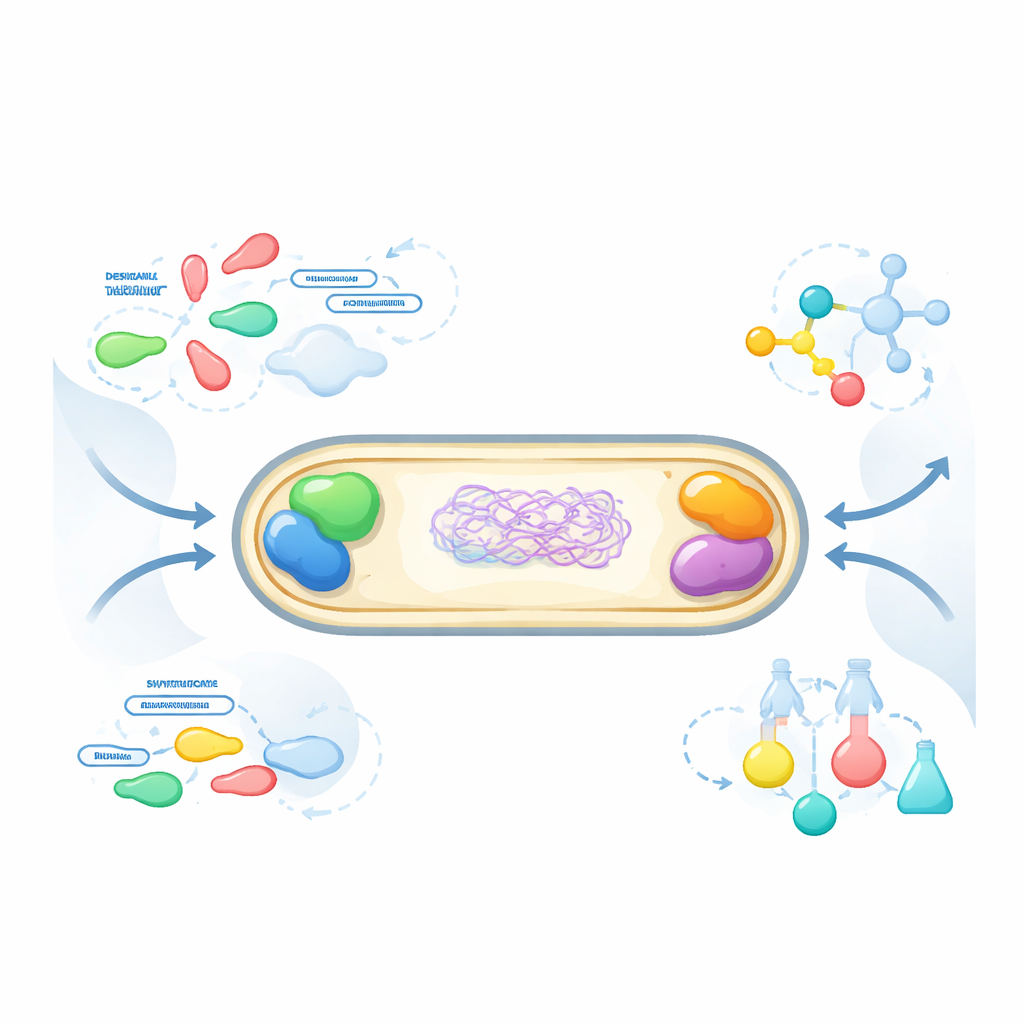
Gotas sin membranas
Muchas células organizan su química mediante orgánulos sin membrana: gotas de proteínas y ácidos nucleicos que se forman por separación de fases, algo parecido a gotas de aceite en agua. Se pensaba que las bacterias eran demasiado simples para tal arquitectura interna, pero ellas también usan gotas similares para controlar la duplicación del ADN, las respuestas al estrés y otros procesos. Los investigadores esperan diseñar versiones artificiales de estos compartimentos para dirigir el metabolismo, ensamblar productos útiles o estudiar cómo funcionan las gotas naturales. Los sistemas sintéticos existentes a menudo dependen de proteínas desordenadas, cuyas interacciones adhesivas son difíciles de predecir e ingenierizar.
Construir con formas de ARN programables
Los autores recurren en su lugar a la nanotecnología de ARN, que explota las reglas predecibles de apareamiento de bases de los ácidos nucleicos. Diseñaron “nanostars”: uniones de ARN en forma de estrella de cuatro brazos cuyos extremos llevan bucles cortos que pueden aparearse con bucles correspondientes en otras nanostars. Dos diseños, llamados A y B, tienen bucles auto‑complementarios, por lo que las nanostars del mismo tipo se atraen y condensan en gotas. Las versiones alteradas (scrambled) carecen de esa complementariedad y deberían permanecer disueltas. El equipo insertó planos genéticos para estas nanostars en E. coli, usando etiquetas fluorescentes de ARN para que las estructuras pudieran verse al microscopio.
Gotas diseñadas dentro de bacterias vivas
Cuando se expresaron las nanostars A o B, aparecieron gotas brillantes dentro de las células bacterianas, mayormente en los polos. El análisis de los patrones de fluorescencia y películas en lapso de tiempo mostró que la mayoría de las células contenían dos o tres gotas que podían fusionarse y volver a crecer, comportándose como pequeños líquidos. En contraste, los diseños scrambled produjeron un resplandor difuso con solo ocasionales agrupamientos débiles, confirmando que el apareamiento específico de bases impulsa la formación de las gotas. A pesar de que enzimas naturales que cortan ARN recortaron algunos brazos de las nanostars, quedaron suficientes estructuras de cuatro y tres brazos para sostener una condensación robusta, lo que destaca la resiliencia del diseño.
Múltiples tipos de gotas y captura de proteínas
Como las nanostars A y B reconocen solo a su propio tipo, las células diseñadas para producir ambas generaron dos tipos de gotas que no se mezclan en la misma bacteria. Estas permanecieron mayormente separadas en el espacio, a menudo en extremos opuestos de la célula. Los autores añadieron después una nueva función: un aptámero de ARN corto dentro de la nanostar A que se une a la proteína fluorescente verde (GFP). Cuando las bacterias produjeron tanto las nanostars modificadas como la GFP, la proteína se concentró fuertemente dentro de las gotas, mientras que en las células de control sin el aptámero permaneció distribuida de forma homogénea. Mediciones de recuperación de fluorescencia tras foto-blanqueado revelaron que la GFP y las nanostars seguían intercambiándose con el citoplasma circundante, lo cual es coherente con un estado de tipo líquido.
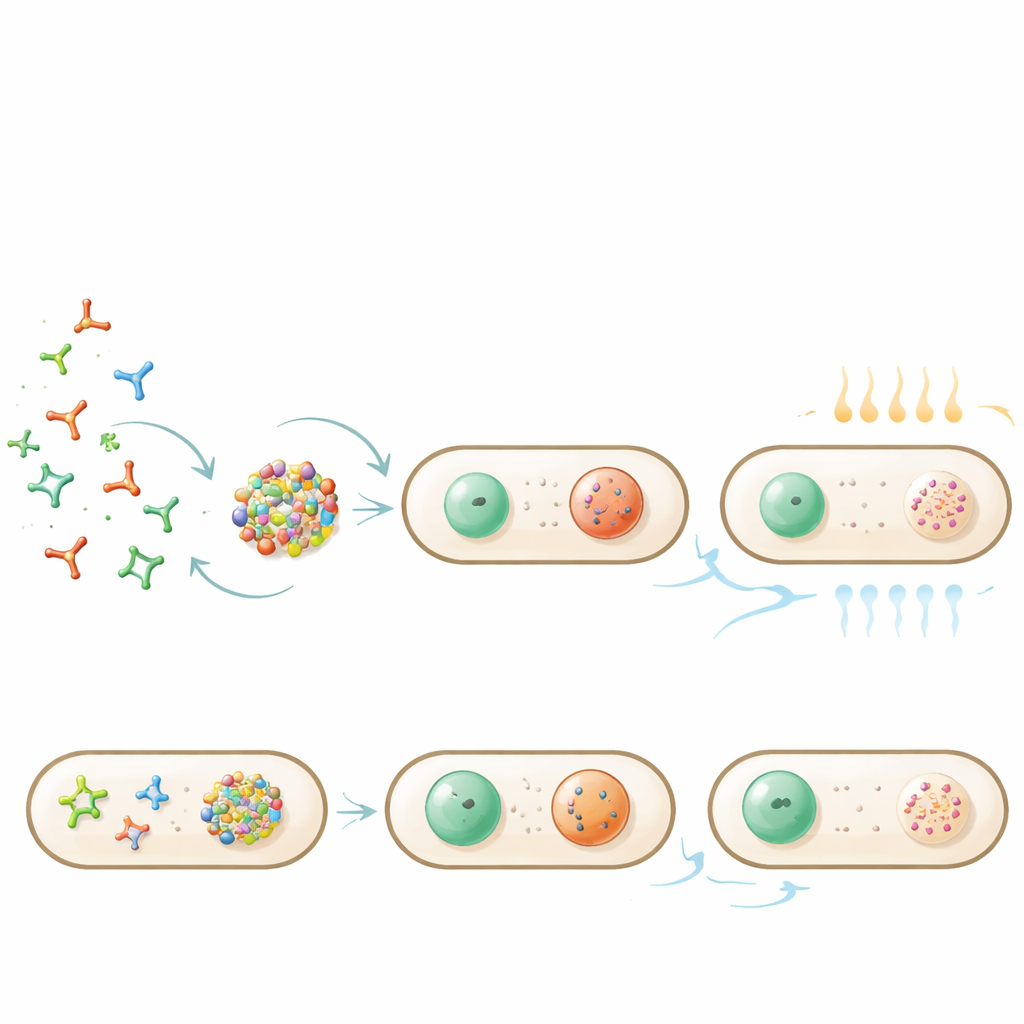
Encender y apagar gotas con calor
Porque las nanostars se adhieren mediante apareamiento de bases, la temperatura ofrece una perilla de control sencilla. Calentar suavemente las bacterias provocó la disolución de las gotas al fundirse los pares de bases; enfriar las hizo reaparecer en sus posiciones polares habituales. La temperatura de “fusión” precisa dependía del diseño de la nanostar y de cuánto recorte enzimático se había producido, pero el proceso se mantuvo reversible en muchas células. Cuando las gotas que contenían GFP capturada se calentaron con más intensidad, tanto ARN como proteína se dispersaron por toda la célula; tras el enfriamiento, las gotas se re-formaron y volvieron a concentrar la proteína, demostrando que la carga puede liberarse y re-aislarse mediante un simple ciclo térmico.
Qué significa esto para la ingeniería celular futura
En términos cotidianos, los investigadores han construido “habitaciones emergentes” programables basadas en ARN dentro de bacterias: habitaciones que se pueden duplicar, mantener separadas, llenar con herramientas seleccionadas y plegar bajo demanda. Dado que las interacciones subyacentes son simples y diseñables, estos orgánulos sintéticos ofrecen una forma flexible de encaminar rutas metabólicas, aislar intermediarios tóxicos o sondear cómo las gotas naturales controlan la química de la vida. El trabajo sugiere que los condensados de ARN nanoingenierizados podrían convertirse en componentes centrales de fábricas microbianas de próxima generación y en herramientas potentes para remodelar el comportamiento celular.
Cita: Ng, B., Fan, C., Dordevic, M. et al. Expression of nano-engineered RNA organelles in bacteria. Nat Commun 17, 2752 (2026). https://doi.org/10.1038/s41467-026-69336-w
Palabras clave: orgánulos sintéticos, nanotecnología de ARN, condensados biomoleculares, ingeniería de células bacterianas, ingeniería metabólica