Clear Sky Science · sv
Elektrokemisk Ferrier-omläggning av glycaler i flöde
Att förvandla enkla sockerarter till kraftfulla byggstenar
Många livräddande läkemedel, från antibiotika till cancerläkemedel, förlitar sig på noggrant utformade sockerstrukturer. Att framställa dessa sockerbaserade delar i laboratoriet har traditionellt krävt hårda kemikalier och energikrävande förhållanden, vilket skapar avfall och begränsar storskalig produktion. Denna artikel beskriver ett nytt sätt att omforma enkla socker-molekyler med elektricitet och en liten flödesreaktor, vilket erbjuder en snabbare, renare och mer skalbar väg till viktiga ingredienser för läkemedel och andra avancerade material.
En klassisk sockerdons, med moderna begränsningar
Kemister har länge använt en omvandling kallad Ferrier-omläggning för att omvandla ”glycaler” – ringformade sockerderivat – till 2,3-omättade glykosider. Dessa produkter är viktiga byggstenar i komplexa naturliga molekyler såsom anticancer-läkemedlet paklitaxel och vissa antibiotika. Traditionellt förlitar sig omläggningen på starka syror eller kraftfulla oxiderande medel för att aktivera sockret, vilket genererar ett mycket reaktivt intermediär som kan attackerad av en annan molekyl, nukleofilen. Även om dessa metoder är effektiva kräver de frätande reagenser, kan vara farliga att hantera, genererar betydande avfall och är inte idealiska för miljöansvarig eller industriell syntes.
Använd elektricitet istället för hårda reagenser
Under de senaste åren har organisk elektrokemi vuxit fram som en grönare strategi, där elektrisk ström används för att driva kemiska reaktioner istället för kemiska oxidanter och reduktanser. Författarna visade tidigare att Ferrier-omläggningen kunde genomföras i en elektrokemisk batch-reaktor, men det tillvägagångssättet led av långa reaktionstider, stora mängder stödjande salt och högt elektriskt energiinsats. I detta arbete förde de processen till en kontinuerlig flödes-elektrokemisk mikroreaktor utrustad med billiga grafitelektroder. Det lilla avståndet mellan elektroderna och den slingrande flödeskanalen förbättrar blandning och laddningsöverföring avsevärt, så reaktionen kan slutföras på under 20 sekunders uppehållstid samtidigt som man använder minimalt med stödjande elektrolyt och en bråkdel av den laddning som tidigare krävdes.

En liten flödesreaktor med stor flexibilitet
För att testa den nya uppställningen började teamet med en vanlig glycal (tri-O-acetyl-D-glucal) och bensylalkohol som partnermolekyl. Under optimerade förhållanden i acetonitril fick de önskad 2,3-omättad glykosid i upp till 94 % utbyte med endast 0,05 enheter elektrisk laddning per mol utgångsmaterial, långt mindre än i tidigare metoder. De undersökte sedan hur generell processen är. Olika glycals, inklusive de härledda från D-galaktos eller med alternativa skyddsgrupper, reagerade smidigt. Reaktorn tolererade också ett brett spektrum av nukleofiler: enkla alkoholer, en sockerbaserad alkohol som bildade ett disackarid, kolbaserade partner som bildade nya kol–kol-bindningar, azider, kväveinnehållande sulfonamider och svavelbaserade nukleofiler. I många fall erhölls produkterna i höga utbyten och med fördelaktig kontroll över den tredimensionella arrangemanget av atomer vid den nya bindningen.
Snabbt, skalbart och grönare
Den kontinuerliga flödesdesignen lämpar sig naturligt för uppskalning. Författarna visade en förberedelse i multigramsskala genom att pumpa reaktanterna genom mikroreaktorn vid högre flödeshastighet, vilket krympte uppehållstiden till bara 18 sekunder samtidigt som hög omvandling och utbyte bibehölls. Detta motsvarade en produktivitet på över 10 millimol per timme och en imponerande volym-tids-yield, vilket betyder att en stor mängd material kan produceras per enhetsreaktortillvolym och tid. Med hjälp av ett standardiserat verktyg för bedömning av grön kemi jämförde de sin metod med tidigare elektrokemiska Ferrier-protokoll. Den nya processen undviker kryogena temperaturer och särskilt farliga lösningsmedel, förbättrar utbyten och minskar dramatiskt processens massintensitet – ett mått på hur mycket material, inklusive avfall, som krävs per enhetsprodukt.
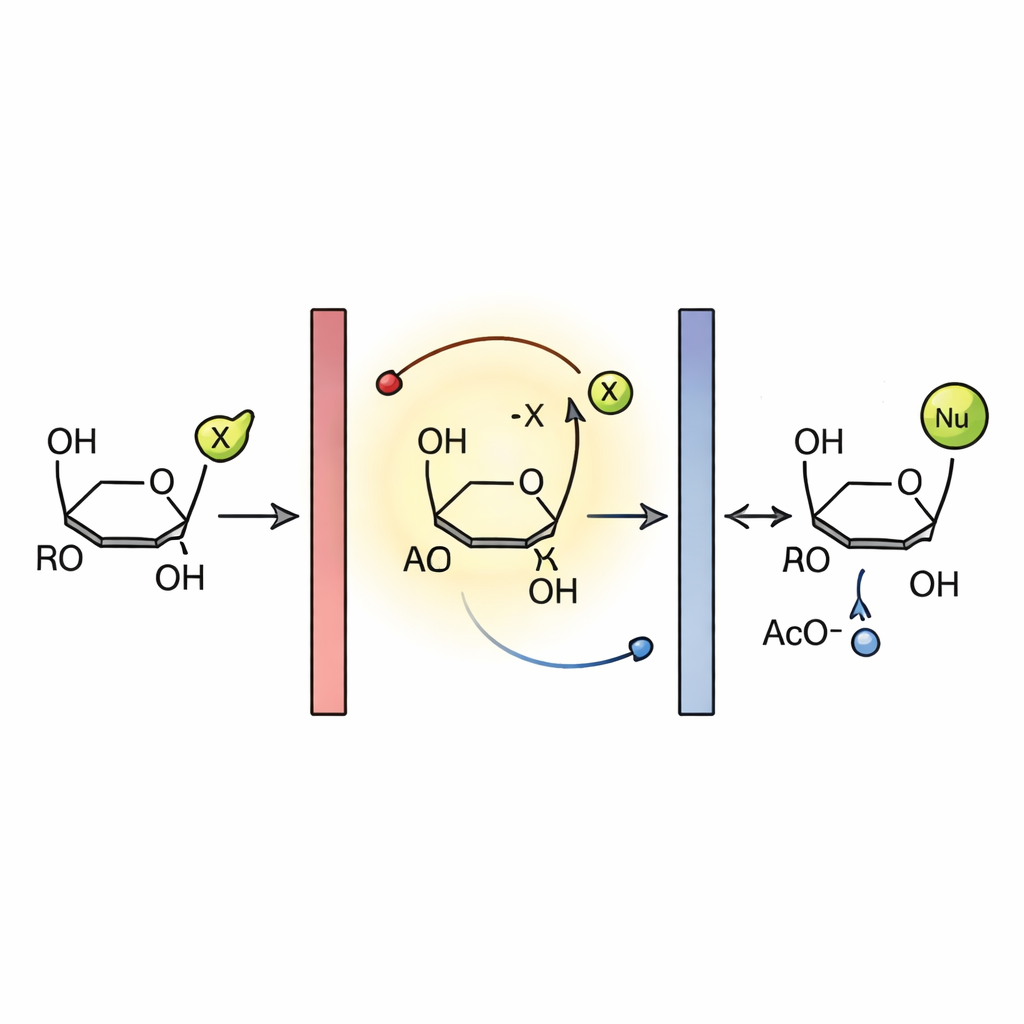
Hur elektricitet driver sockerväxlingen
Elektrokemiska mätningar och tidigare studier pekar på en radikal kedjemekanism. I reaktorn oxideras glycalen först vid anoden och bildar en kortlivad radikalkation. Denna art avger en acetoxyradikalen, vilket ger ett positivt laddat intermediär som snabbt attackeras av nukleofilen för att bilda den nya glykosiden efter protonförlust. Den utsläppta acetoxyradikalen hjälper till att förlänga kedjan genom att oxidera en annan glycalmolekyl, medan överskottsradikaler så småningom reduceras vid katoden. Impermeabla grafitelektroder var avgörande: andra material visade dålig prestanda, troligen eftersom reaktiva arter fastnade på deras ytor och blockerade effektiv elektronöverföring. Kombinationen av denna robusta elektrod, snabbt flöde och korta diffusionsvägar utgör grunden för processens höga effektivitet och selektivitet.
En renare framtid för komplexa sockerarter
Sammanfattningsvis visar studien att en klassisk sockeromläggande reaktion kan omformas för moderna behov genom att köra den i en elektrokemisk flödesmikroreaktor. Metoden omvandlar en mängd enkla glycals och partnermolekyler till värdefulla 2,3-omättade glykosider snabbt, i höga utbyten och med betydligt mindre avfall och energiinmatning än traditionella vägar. För icke-specialister är huvudbudskapet att elektricitet, när den används omsorgsfullt i miniatyra flödesanordningar, kan ersätta hårda reagenser och möjliggöra en mer hållbar produktion av de sofistikerade sockerfragment som ligger till grund för många avancerade läkemedel och material.
Citering: Suman, P., Fokin, M., Hunt, K.E. et al. Electrochemical Ferrier rearrangement of glycals in flow. Commun Chem 9, 145 (2026). https://doi.org/10.1038/s42004-026-01948-1
Nyckelord: elektrokemisk syntes, flödeskemi, kolhydratkemi, glykosylering, grön kemi