Clear Sky Science · pl
Elektrochemiczna przemiana Ferriera glikali w przepływie
Przekształcanie prostych cukrów w potężne blokii konstrukcyjne
Wiele leków ratujących życie, od antybiotyków po środki przeciwnowotworowe, opiera się na precyzyjnie ukształtowanych strukturach cukrowych. Wytwarzanie tych fragmentów w laboratorium tradycyjnie wymagało ostrych reagentów i warunków energochłonnych, co generuje odpady i ogranicza skalowalność produkcji. Artykuł opisuje nowy sposób przebudowy prostych cząsteczek cukru przy użyciu prądu i niewielkiego reaktora przepływowego, oferując szybszą, czystszą i bardziej skalowalną drogę do ważnych składników farmaceutycznych i zaawansowanych materiałów.
Klasyczny trik cukrowy, z nowoczesnymi ograniczeniami
Chemicy od dawna stosują przemianę zwaną rekonstrukcją Ferriera do przekształcania „glikali” – pochodnych cukrów w postaci pierścienia – w 2,3-nienasycone glikozydy. Produkty te są kluczowymi cegiełkami w złożonych naturalnych cząsteczkach, takich jak lek przeciwnowotworowy paklitaksel czy niektóre antybiotyki. Tradycyjnie reakcja ta wymaga silnych kwasów lub silnych utleniaczy do aktywacji cukru, prowadząc do wysoce reaktywnego intermediatu podatnego na atak nukleofila. Choć skuteczne, metody te posługują się korozyjnymi reagentami, mogą być niebezpieczne w obsłudze, generują znaczne ilości odpadów i nie są idealne z perspektywy odpowiedzialnej środowiskowo ani dla syntez przemysłowych.
Zamiast ostrych reagentów — prąd
W ostatnich latach chemia organiczna wykorzystująca prąd stała się bardziej zieloną strategią, używając przepływu elektrycznego do napędzania reakcji zamiast utleniaczy i reduktorów chemicznych. Autorzy wcześniej wykazali, że rekonstrukcję Ferriera można przeprowadzić w elektrochemicznym reaktorze porcjowym, ale to podejście nadal wiązało się z długimi czasami reakcji, dużymi ilościami soli wspomagającej i wysokim poborem energii elektrycznej. W tej pracy przenoszą proces do ciągłego elektrochemicznego mikroreaktora wyposażonego w tanie elektrody grafitowe. Mały odstęp między elektrodami i meandrowy kanał przepływu znacznie poprawiają mieszanie i transfer ładunku, dzięki czemu reakcja może się zakończyć w czasie rezydencji poniżej 20 sekund, używając minimalnej ilości elektrolitu wspomagającego i ułamka ładunku wcześniej wymaganego.

Maleńki reaktor przepływowy o dużej elastyczności
Aby przetestować nowe urządzenie, zespół zaczął od powszechnego glikala (tri-O-acetyl-D-glukalu) i alkoholu benzylowego jako partnera. W zoptymalizowanych warunkach w acetonitrylu uzyskali pożądany 2,3-nienasycony glikozyd w wydajności sięgającej 94% przy użyciu zaledwie 0,05 jednostki ładunku na mol substratu, znacznie mniej niż w wcześniejszych metodach. Następnie zbadali ogólność procesu. Różne glikali, w tym pochodne D-galaktozy czy noszące alternatywne grupy ochronne, reagowały gładko. Reaktor tolerował też szerokie spektrum nukleofilów: proste alkohole, alkohol pochodzenia cukrowego prowadzący do disacharydu, partnerów węglowych tworzących nowe wiązania węglowo-węglowe, azydy, zawierające azot sulfonamidy oraz nukleofile siarkowe. W wielu przypadkach produkty otrzymywano w wysokich wydajnościach i z korzystną kontrolą nad trójwymiarowym układem atomów przy nowym wiązaniu.
Szybko, skalowalnie i bardziej ekologicznie
Konstrukcja ciągła naturalnie sprzyja skalowaniu. Autorzy zaprezentowali przygotowanie wielogramowe, pompując reagent przez mikroreaktor z wyższą prędkością przepływu, skracając czas rezydencji do zaledwie 18 sekund przy zachowaniu wysokiej konwersji i wydajności. Przełożyło się to na wydajność ponad 10 milimoli na godzinę i imponującą wydajność przestrzenno-czasową, co oznacza dużą ilość materiału produkowaną na jednostkę objętości reaktora i czasu. Korzystając ze standardowego zestawu narzędzi oceny zielonej chemii, porównali swoją metodę z wcześniejszymi elektrochemicznymi protokołami Ferriera. Nowy proces unika niskich temperatur kriogenicznych i szczególnie niebezpiecznych rozpuszczalników, poprawia wydajności i dramatycznie zmniejsza intensywność masową procesu — wskaźnik określający, ile materiału, w tym odpadów, jest wymagane na jednostkę produktu.
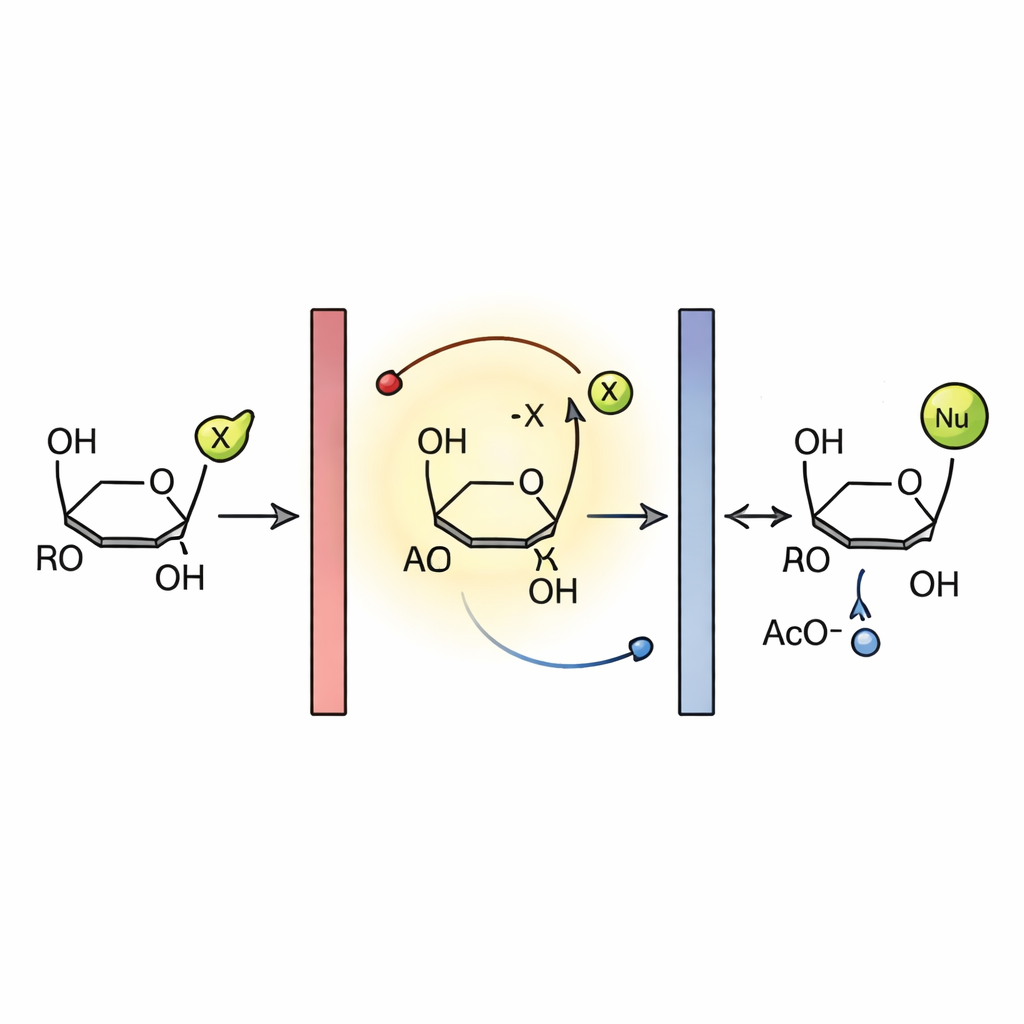
Jak prąd napędza cukrową przemianę
Pomiary elektrochemiczne i wcześniejsze badania wskazują na mechanizm łańcuchowy z rodnikami. W reaktorze glikal jest najpierw utleniany na anodzie, tworząc krótkotrwały kation-radikal. Gatunek ten wyrzuca rodnik acetoksylowy, dając dodatnio naładowany intermediat, który szybko ulega atakowi nukleofila, tworząc nowy glikozyd po utracie protonu. Wyrzucony rodnik acetoksylowy pomaga propagować łańcuch, utleniając kolejny cząsteczkę glikala, podczas gdy nadmiar rodników ostatecznie ulega redukcji na katodzie. Imperwialne elektrody grafitowe okazały się kluczowe: inne materiały wykazywały słabsze działanie, prawdopodobnie dlatego, że reaktywne gatunki przywierały do ich powierzchni i blokowały efektywny transfer elektronów. Połączenie tej trwałej elektrody, szybkiego przepływu i krótkich dróg dyfuzji leży u podstaw wysokiej wydajności i selektywności procesu.
Czystsza przyszłość dla złożonych cukrów
Podsumowując, badanie pokazuje, że klasyczna reakcja przebudowy cukrów może zostać przeprojektowana na potrzeby współczesne poprzez prowadzenie jej w elektrochemicznym mikroreaktorze przepływowym. Metoda przekształca różnorodne proste glikali i partnerów w wartościowe 2,3-nienasycone glikozydy szybko, w wysokiej wydajności i przy znacznie mniejszej ilości odpadów i nakładzie energetycznym niż tradycyjne drogi. Dla niespecjalistów kluczowy przekaz jest taki, że prąd, gdy jest starannie stosowany w miniaturowych urządzeniach przepływowych, może zastąpić ostre reagenty i umożliwić bardziej zrównoważoną produkcję złożonych fragmentów cukrowych, które stanowią podstawę wielu zaawansowanych leków i materiałów.
Cytowanie: Suman, P., Fokin, M., Hunt, K.E. et al. Electrochemical Ferrier rearrangement of glycals in flow. Commun Chem 9, 145 (2026). https://doi.org/10.1038/s42004-026-01948-1
Słowa kluczowe: synteza elektrochemiczna, chemia przepływowa, chemia węglowodanów, glikosylacja, zielona chemia