Clear Sky Science · de
Elektrochemische Ferrier-Umlagerung von Glykalen im Fluss
Einfache Zucker in leistungsfähige Bausteine verwandeln
Viele lebensrettende Medikamente, von Antibiotika bis zu Krebswirkstoffen, beruhen auf sorgfältig gestalteten Zuckerstrukturen. Die Herstellung dieser zuckerbasierten Bausteine im Labor erforderte traditionell oft aggressive Chemikalien und energieintensive Bedingungen, die Abfall erzeugen und die großtechnische Produktion erschweren. Diese Arbeit beschreibt einen neuen Weg, einfache Zuckermoleküle mit Elektrizität und einem winzigen Flussreaktor umzuwandeln und bietet eine schnellere, sauberere und besser skalierbare Route zu wichtigen Bestandteilen für Pharmazeutika und andere Hightech-Materialien.
Ein klassischer Zuckertrick mit modernen Einschränkungen
Chemiker nutzen seit langem eine Umwandlung, die als Ferrier-Umlagerung bekannt ist, um „Glykale“ – ringförmige Zuckederivate – in 2,3-ungesättigte Glykoside zu überführen. Diese Produkte sind Schlüsselbausteine in komplexen Naturstoffen wie dem Krebsmedikament Paclitaxel und bestimmten Antibiotika. Traditionell beruht die Umlagerung auf starken Säuren oder kräftigen Oxidationsmitteln, die den Zucker aktivieren und ein hochreaktives Zwischenprodukt erzeugen, das von einem Nukleophil angegriffen werden kann. Zwar wirksam, erfordern diese Methoden korrosive Reagenzien, sind oft gefährlich in der Handhabung, erzeugen beträchtliche Abfälle und sind für umweltbewusste oder industrielle Synthesen suboptimal.
Elektrizität statt aggressiver Reagenzien
In den letzten Jahren hat sich die organische Elektrochemie als umweltfreundlichere Strategie etabliert, bei der elektrischer Strom chemische Reaktionen antreibt statt chemischer Oxidantien oder Reduktantien. Die Autoren zeigten zuvor, dass die Ferrier-Umlagerung in einem elektrochemischen Batch-Reaktor durchführbar ist, doch litt dieser Ansatz weiterhin unter langen Reaktionszeiten, großen Mengen an Unterstützungssalz und hohem Strombedarf. In dieser Arbeit verlegen sie den Prozess in einen kontinuierlichen elektrochemischen Mikroflussreaktor mit preiswerten Graphitelektroden. Der winzige Spalt zwischen den Elektroden und der verschlungene Flusskanal verbessern Mischung und Ladungstransfer stark, sodass die Reaktion in unter 20 Sekunden Verweilzeit abgeschlossen werden kann, wobei nur minimale Mengen an Unterstützungselektrolyt und ein Bruchteil der zuvor benötigten Ladung benötigt werden.

Ein winziger Flussreaktor mit großer Flexibilität
Um das neue System zu testen, begannen die Forscher mit einem gebräuchlichen Glykal (tri-O-acetyl-D-glucal) und Benzylalkohol als Reaktionspartner. Unter optimierten Bedingungen in Acetonitril erreichten sie das gewünschte 2,3-ungesättigte Glykosid in bis zu 94 % Ausbeute bei nur 0,05 Einheiten elektrischer Ladung pro Mol Ausgangsmaterial, weit weniger als bei früheren Methoden. Anschließend prüften sie die Allgemeingültigkeit des Verfahrens. Verschiedene Glykale, einschließlich Derivate aus D-Galactose oder mit alternativen Schutzgruppen, reagierten problemlos. Der Reaktor vertrug außerdem eine breite Palette von Nukleophilen: einfache Alkohole, ein zuckerbasiertes Alkohol, das ein Disaccharid bildete, kohlenstoffbasierte Partner, die neue C–C-Bindungen knüpften, Azide, stickstoffhaltige Sulfonamide und schwefelbasierte Nukleophile. In vielen Fällen wurden die Produkte in hohen Ausbeuten und mit günstiger Kontrolle über die dreidimensionale Anordnung der Atome an der neuen Bindung erhalten.
Schnell, skalierbar und grüner
Das Continuous-Flow-Design eignet sich von Natur aus für die Skalierung. Die Autoren demonstrierten eine Mehrgramm‑Synthese, indem sie die Reaktanten mit höherer Flussrate durch den Mikroreaktor pumpten und die Verweilzeit auf nur 18 Sekunden verkürzten, während hohe Umsetzungen und Ausbeuten beibehalten wurden. Dies entsprach einer Produktivität von mehr als 10 Millimol pro Stunde und einer beeindruckenden Raum‑Zeit-Ausbeute, also einer großen Materialmenge pro Reaktorvolumen und Zeit. Mit einem üblichen Green‑Chemistry-Bewertungstoolkit verglichen sie ihr Verfahren mit früheren elektrochemischen Ferrier‑Protokollen. Der neue Prozess vermeidet kryogene Temperaturen und besonders gefährliche Lösungsmittel, verbessert die Ausbeuten und reduziert die Prozessmasseintensität drastisch – ein Maß dafür, wie viel Material einschließlich Abfall pro Einheit Produkt erforderlich ist.
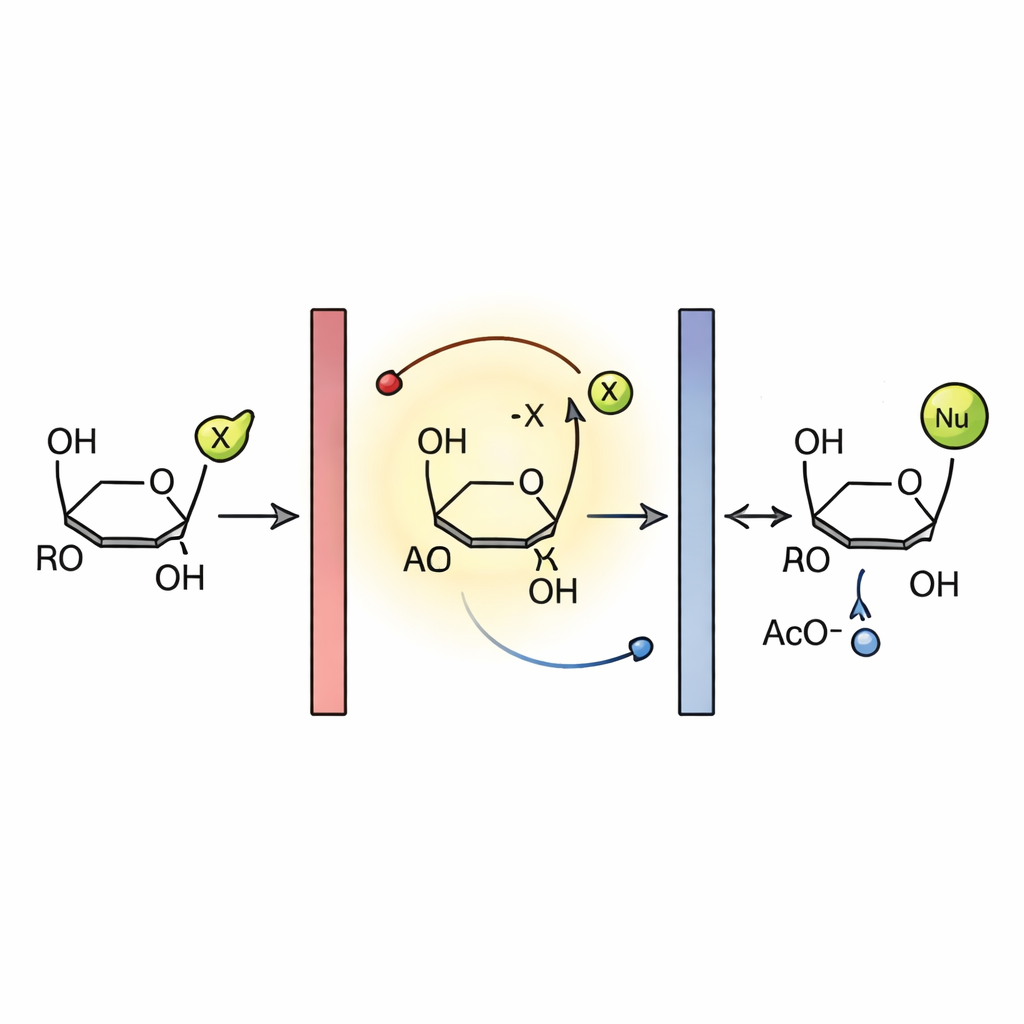
Wie Elektrizität den Zuckerumbau antreibt
Elektrochemische Messungen und vorherige Studien deuten auf einen Radikal‑Ketten‑Mechanismus hin. Im Reaktor wird das Glykal zunächst an der Anode oxidiert und bildet ein kurzlebiges Radikal-Kation. Diese Spezies stößt ein Acetoxy‑Radikal aus und ergibt ein positiv geladenes Zwischenprodukt, das schnell vom Nukleophil angegriffen wird, um nach Protonenverlust das neue Glykosid zu bilden. Das ausgestoßene Acetoxy‑Radikal hilft, die Kette fortzupflanzen, indem es ein weiteres Glykal oxidiert, während überschüssige Radikale schließlich an der Kathode reduziert werden. Undurchlässige Graphitelektroden waren entscheidend: Andere Materialien zeigten schlechte Leistung, vermutlich weil reaktive Spezies an ihren Oberflächen haften und den effizienten Elektronentransfer blockieren. Die Kombination aus dieser robusten Elektrode, schnellem Fluss und kurzen Diffusionswegen bildet die Grundlage für die hohe Effizienz und Selektivität des Prozesses.
Eine sauberere Zukunft für komplexe Zucker
Insgesamt zeigt die Studie, dass eine klassische Zucker‑Umlagerung für moderne Anforderungen neu gedacht werden kann, indem man sie in einem elektrochemischen Flow‑Mikroreaktor betreibt. Das Verfahren wandelt eine Vielzahl einfacher Glykale und Reaktionspartner rasch in wertvolle 2,3‑ungesättigte Glykoside um, mit hohen Ausbeuten und deutlich weniger Abfall und Energieaufwand als traditionelle Routen. Für Nicht‑Spezialisten lautet die zentrale Botschaft: Elektrizität kann, wenn sie gezielt in miniaturisierten Flussgeräten eingesetzt wird, aggressive Reagenzien ersetzen und eine nachhaltigere Produktion der komplexen Zuckerfragmenten ermöglichen, die vielen modernen Medikamenten und Materialien zugrunde liegen.
Zitation: Suman, P., Fokin, M., Hunt, K.E. et al. Electrochemical Ferrier rearrangement of glycals in flow. Commun Chem 9, 145 (2026). https://doi.org/10.1038/s42004-026-01948-1
Schlüsselwörter: elektrochemische Synthese, Flow-Chemie, Kohlenhydratchemie, Glycosylierung, Grüne Chemie