Clear Sky Science · fr
Réarrangement électrochimique de Ferrier des glycals en flux
Transformer des sucres simples en blocs de construction puissants
De nombreux médicaments vitaux, des antibiotiques aux traitements anticancéreux, reposent sur des structures glucidiques finement ajustées. La fabrication de ces fragments sucrés en laboratoire a traditionnellement nécessité des produits chimiques agressifs et des conditions énergivores, générant des déchets et limitant la production à grande échelle. Cet article décrit une nouvelle manière de remodeler des molécules de sucre simples à l'aide de l'électricité et d'un micro‑réacteur en flux, offrant une voie plus rapide, plus propre et plus facilement extensible vers des ingrédients importants pour les produits pharmaceutiques et d'autres matériaux avancés.
Un tour classique des sucres, avec des limites modernes
Les chimistes utilisent depuis longtemps une transformation appelée réarrangement de Ferrier pour convertir des « glycals » – des dérivés cycliques du sucre – en glycosides 2,3‑insaturés. Ces produits sont des blocs essentiels dans des molécules naturelles complexes telles que le paclitaxel anticancéreux et certains antibiotiques. Classiquement, le réarrangement repose sur des acides forts ou des agents oxydants puissants pour activer le sucre, générant un intermédiaire très réactif susceptible d’être attaqué par un autre composé, le nucléophile. Bien que efficaces, ces méthodes exigent des réactifs corrosifs, peuvent être dangereux à manipuler, produisent des déchets importants et ne sont pas idéales pour une synthèse respectueuse de l’environnement ou à l’échelle industrielle.
Utiliser l’électricité au lieu de réactifs agressifs
Ces dernières années, l’électrochimie organique a émergé comme une stratégie plus verte, utilisant le courant électrique pour piloter des réactions chimiques au lieu d’oxydants et réducteurs chimiques. Les auteurs avaient montré précédemment que le réarrangement de Ferrier pouvait être réalisé dans un réacteur batch électrochimique, mais cette approche souffrait encore de temps de réaction longs, d’un usage important de sel support et d’un apport électrique élevé. Dans ce travail, ils transfèrent le procédé dans un micro‑réacteur électrochimique en flux continu équipé d’électrodes en graphite peu coûteuses. L’écartement minime entre électrodes et le canal en flux en forme de serpentin améliorent fortement le mélange et le transfert de charge, permettant à la réaction de s’achever en moins de 20 secondes de temps de résidence tout en utilisant un minimum d’électrolyte support et une fraction de la charge électrique précédemment requise.

Un micro‑réacteur compact à grande flexibilité
Pour tester le nouveau dispositif, l’équipe a commencé avec un glycal courant (tri‑O‑acétyl‑D‑glucal) et l’alcool benzilyque comme partenaire. Dans des conditions optimisées en acétonitrile, ils ont obtenu le glycoside 2,3‑insaturé souhaité avec des rendements allant jusqu’à 94 % en n’utilisant que 0,05 équivalent de charge électrique par mole de matière de départ, bien moins que dans les méthodes antérieures. Ils ont ensuite exploré la généralité du procédé. Différents glycals, y compris ceux dérivés du D‑galactose ou portant d’autres groupes protecteurs, ont réagi sans difficulté. Le réacteur a également toléré une large gamme de nucléophiles : des alcools simples, un alcool dérivé d’un sucre donnant un disaccharide, des partenaires carbonés formant de nouvelles liaisons carbone–carbone, des azotures, des sulfonamides azotés, et des nucléophiles à base de soufre. Dans de nombreux cas, les produits ont été obtenus en rendements élevés et avec un bon contrôle de la stéréochimie au niveau de la nouvelle liaison.
Rapide, extensible et plus écologique
La conception en flux continu se prête naturellement à la montée en échelle. Les auteurs ont démontré une préparation multi‑grammes en pompant les réactifs à travers le micro‑réacteur à un débit plus élevé, réduisant le temps de résidence à seulement 18 secondes tout en maintenant une conversion et un rendement élevés. Cela s’est traduit par une productivité de plus de 10 millimoles par heure et un rendement espace‑temps remarquable, c’est‑à‑dire une grande quantité de matière produite par unité de volume de réacteur et par unité de temps. À l’aide d’un outil d’évaluation standard en chimie verte, ils ont comparé leur méthode aux protocoles électrochimiques de Ferrier antérieurs. Le nouveau procédé évite les températures cryogéniques et les solvants particulièrement dangereux, améliore les rendements et réduit drastiquement l’intensité massique du procédé – une mesure de la quantité de matière, y compris les déchets, requise par unité de produit.
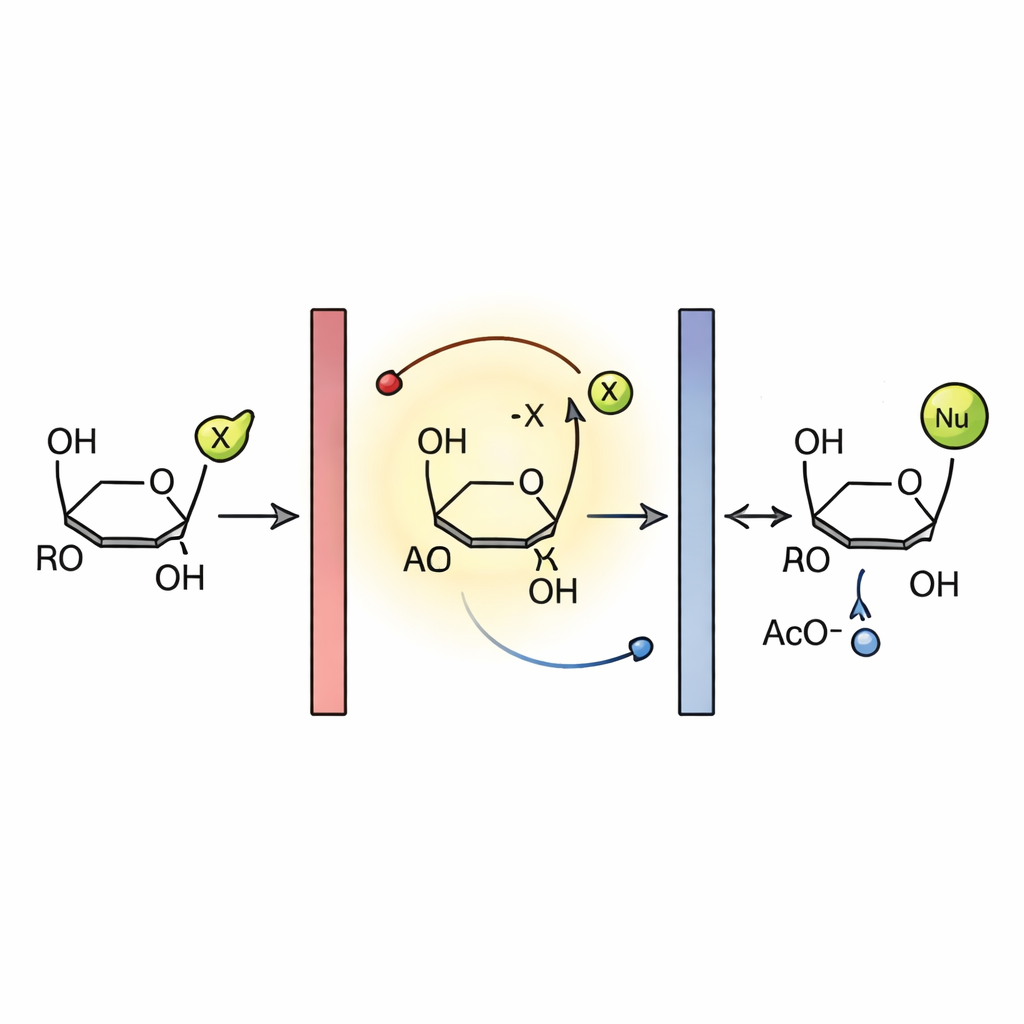
Comment l’électricité pilote le basculement sucré
Les mesures électrochimiques et des études antérieures suggèrent un mécanisme en chaîne radicalaire. Dans le réacteur, le glycal est d’abord oxydé à l’anode, formant un radical cation éphémère. Cette espèce éjecte un radical acétoxy, donnant un intermédiaire chargé positivement qui est rapidement attaqué par le nucléophile pour former le nouveau glycoside après perte d’un proton. Le radical acétoxy expulsé aide à propager la chaîne en oxydant une autre molécule de glycal, tandis que les radicaux excédentaires sont finalement réduits à la cathode. Des électrodes en graphite imperméables ont été cruciales : d’autres matériaux ont montré de faibles performances, probablement parce que des espèces réactives adhéraient à leurs surfaces et entravaient le transfert d’électrons. La combinaison de cette électrode robuste, du flux rapide et des courts chemins de diffusion sous‑tend la grande efficacité et la sélectivité du procédé.
Un avenir plus propre pour les sucres complexes
Dans l’ensemble, l’étude montre qu’une réaction classique de réarrangement des sucres peut être réinventée pour répondre aux besoins modernes en la réalisant dans un micro‑réacteur électrochimique en flux. La méthode convertit une variété de glycals simples et de partenaires en précieux glycosides 2,3‑insaturés rapidement, en bon rendement et avec beaucoup moins de déchets et d’apport énergétique que les voies traditionnelles. Pour les non‑spécialistes, le message clé est que l’électricité, correctement exploitée dans des dispositifs miniatures en flux, peut remplacer des réactifs agressifs et permettre une production plus durable des fragments glucidiques sophistiqués qui sous‑tendent de nombreux médicaments et matériaux avancés.
Citation: Suman, P., Fokin, M., Hunt, K.E. et al. Electrochemical Ferrier rearrangement of glycals in flow. Commun Chem 9, 145 (2026). https://doi.org/10.1038/s42004-026-01948-1
Mots-clés: synthèse électrochimique, chimie en flux, chimie des glucides, glycosylation, chimie verte