Clear Sky Science · sv
Jämförelse mellan mikroskopi, metabarcoding och multispektral bildflödescytometri för identifiering och relativ abundansanalys av insektsspritt pollen
Varför pollenräkning är viktig
Pollen kan se ut som enkelt gult damm, men för vilda blommor, grödor och de insekter som besöker dem är det en livlina. Att förstå vilka växter insekter besöker, och hur mycket pollen de bär på, hjälper forskare att följa ekosystemens hälsa, livsmedelsproduktion och pollinatörernas näringsstatus. Att faktiskt identifiera och räkna dessa mikroskopiska korn är dock mödosamt arbete. Denna artikel ställer en praktisk fråga med stora implikationer: vilka moderna verktyg gör bäst jobb att säga vilka pollensorter som finns och i vilka mängder på pollinerande insekter?
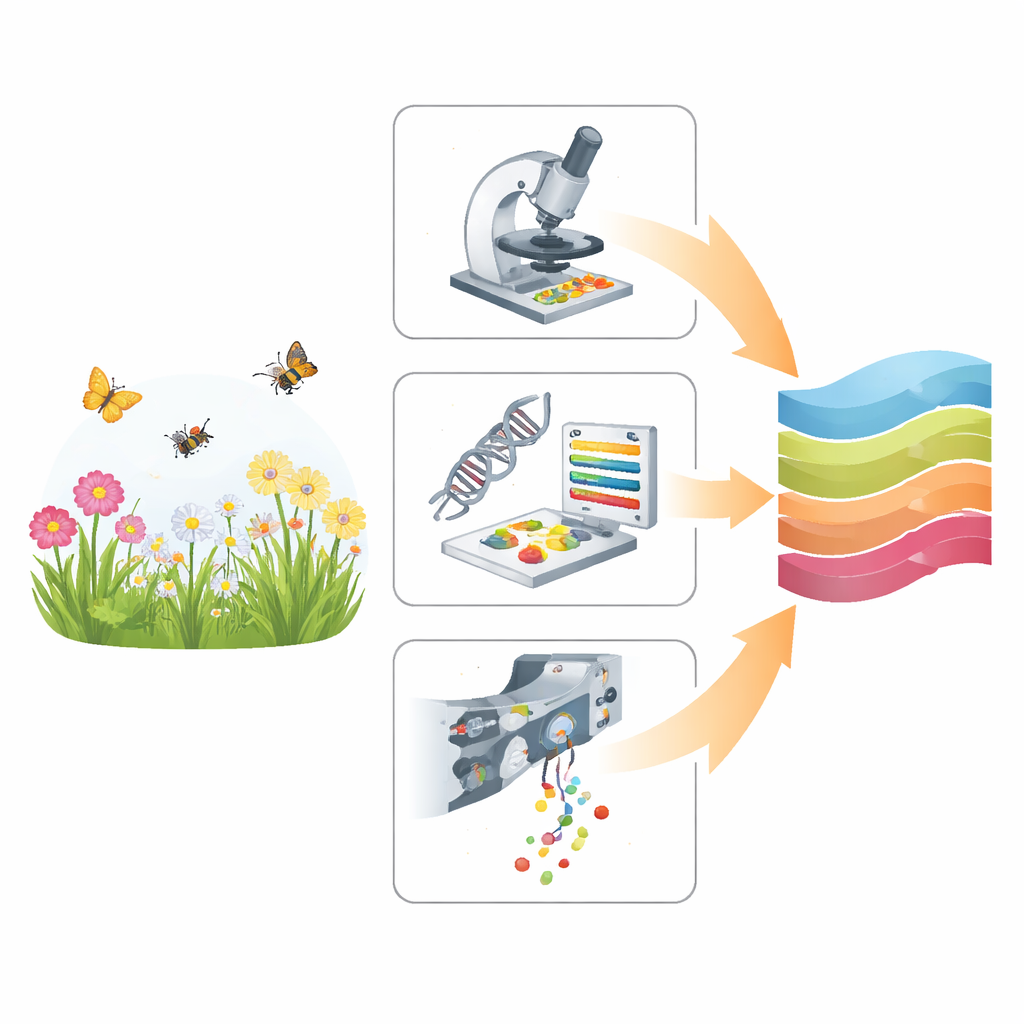
Tre olika sätt att läsa pollen
Studien jämför tre tillvägagångssätt som alla utgår från samma grundmaterial—blandade pollen samlade från blommor och från insektskroppar—men som extraherar information på mycket olika sätt. Traditionell ljusmikroskopi förlitar sig på en utbildad expert som tittar på förstoringar av kornen och känner igen deras former och ytmönster. Metabarcoding hoppar över formbedömning och läser istället korta DNA‑segment från pollenet, som matchas mot stora genetiska referensbibliotek. En nyare teknik, multispektral bildflödescytometri (MIFC), för tusentals korn förbi kameror och sensorer, fångar bilder och ljussignaler som en datoralgoritm använder för att sortera dem till arter. Tillsammans täcker dessa metoder spektrat från långsamt, handgripligt arbete till högt automatiserad, höggenomströmmande analys.
Sätta metoderna på rättvisa prov
För att jämföra prestanda byggde forskarna först “artificiella” pollenblandningar i labbet av nio vanliga vildblomartsarter från rumänska ängar. För dessa prover var de exakta arterna och deras verkliga andelar kända, vilket möjliggjorde ett direkt test av noggrannheten. De skapade tre blandningstyper som främst skiljde sig åt i hur vanliga småkorniga pollen var, och delade sedan identiska portioner av varje blandning mellan de tre metoderna. I ett andra steg analyserade de pollen som naturligt fallit av vilda bin, humlor och flugor fångade i fält, där den verkliga sammansättningen var okänd men nära den variation man ser i verkliga ekologiska studier.
Vem är bäst på att namnge arter?
När utmaningen var att helt enkelt upptäcka vilka växtslag som fanns i de artificiella blandningarna—utan ledtrådar—var DNA‑metabarcoding en klar vinnare. Den plockade upp en högre andel av målgenerna korrekt än vare sig mikroskopi eller MIFC och gav färre felaktiga påvisanden. Eftersom den bygger på skillnader i DNA snarare än form kan metabarcoding skilja åt liknande korn och till och med urskilja nära besläktade arter, något som ofta övergår både människans öga och automatiska bildklassificerare. Alla metoder missade dock ibland vissa taxon, och de morfologibaserade verktygen var särskilt känsliga för pollen som krympt eller förändrats under förvaring eller som avvek subtilt från de referensbilder som använts för att träna datorn.
Vem är bäst på rättvis räkning?
Noggrannheten såg annorlunda ut när uppgiften var att uppskatta hur mycket av varje pollentyp som fanns. Efter korrigering för felidentifieringar och under antagandet att artuppsättningen i provet var känd låg traditionell mikroskopi närmast de verkliga proportionerna i de artificiella blandningarna, följd av MIFC. Metabarcoding presterade sämst i detta avseende: vissa arter var konsekvent överrepresenterade i DNA‑läsantal, medan andra var underrepresenterade. Dessa skevheter uppstår troligen från ojämna mängder DNA per korn, skillnader i hur lätt DNA extraheras, och särdrag i amplifieringsprocessen. MIFC bearbetade långt fler korn än mikroskopi och visade generellt god precision, men dess noggrannhet berodde fortfarande i hög grad på hur väl bildbiblioteket speglade verklig variation i pollen.
Blandade signaler från riktiga insekter
När teamet vände sig till pollen från vilda insekter sjönk överensstämmelsen mellan metoder markant. För vissa insekter som bar mestadels en pollentyp konvergerade alla tre metoder mot liknande bilder. För mer diversifierade prover hölls metoderna ofta inte med varandra, även när de morfologibaserade verktygen "guidades" av artlistan från metabarcoding. Intressant nog stämde de två bildbaserade metoderna—ljusmikroskopi och MIFC—sämst överens med varandra, medan båda i viss mån låg närmare DNA‑resultaten. Dessa avvikelser belyser hur provhantering, klumpning av korn, förvaringseffekter och blinda fläckar i varje referensbibliotek kan forma den slutliga bilden av vad en insekt besökt.
Ett praktiskt recept för framtida pollenstudier
Författarna drar slutsatsen att ingen enskild teknik ännu kan leverera både perfekt identifiering och perfekt kvantifiering. För studier som främst behöver veta vilka växter som besöks rekommenderas DNA‑metabarcoding som det mest tillförlitliga alternativet. När prioriteten är att kvantifiera hur mycket pollen som bärs presterar traditionell mikroskopi eller MIFC bättre, där MIFC erbjuder en betydande tidsfördel för stora provserier. För att få både identitet och relativ abundans—situationer som är vanliga i många ekologiska och bevarandeinriktade projekt—förespråkar studien en tvåstegsstrategi: använd först metabarcoding för att bygga en pålitlig artlista för varje prov, och använd sedan den informationen för att styra höggenomströmmande bildbaserad räkning, särskilt med MIFC. Författarna menar att denna kombinerade metod är väl lämpad för att följa pollinering och pollinatörsdieter över de stora rumsliga och tidsmässiga skalor som dagens biologiska mångfalds‑ och klimatutmaningar kräver.
Citering: Motivans Švara, E., Rakosy, D., Knight, T.M. et al. Method comparison of microscopy, metabarcoding, and multispectral imaging flow cytometry for identification and relative abundance analysis of insect-dispersed pollen. Sci Rep 16, 12578 (2026). https://doi.org/10.1038/s41598-026-47800-3
Nyckelord: pollenanalys, pollinatörer, DNA-metabarcoding, mikroskopi, bildflödescytometri