Clear Sky Science · es
Comparación de métodos: microscopía, metabarcoding y citometría de flujo con imagen multiespectral para la identificación y el análisis de abundancia relativa de polen dispersado por insectos
Por qué importa contar el polen
El polen puede parecer un simple polvo amarillo, pero para las flores silvestres, los cultivos y los insectos que las visitan es una línea de vida. Comprender qué plantas visitan los insectos y cuánto polen transportan ayuda a los científicos a vigilar la salud de los ecosistemas, la producción de alimentos y la nutrición de los polinizadores. Sin embargo, identificar y contar estos granos microscópicos es un trabajo laborioso. Este artículo plantea una pregunta práctica con grandes implicaciones: ¿qué herramientas modernas hacen el mejor trabajo para decirnos qué polen está presente y en qué cantidades en los insectos polinizadores?
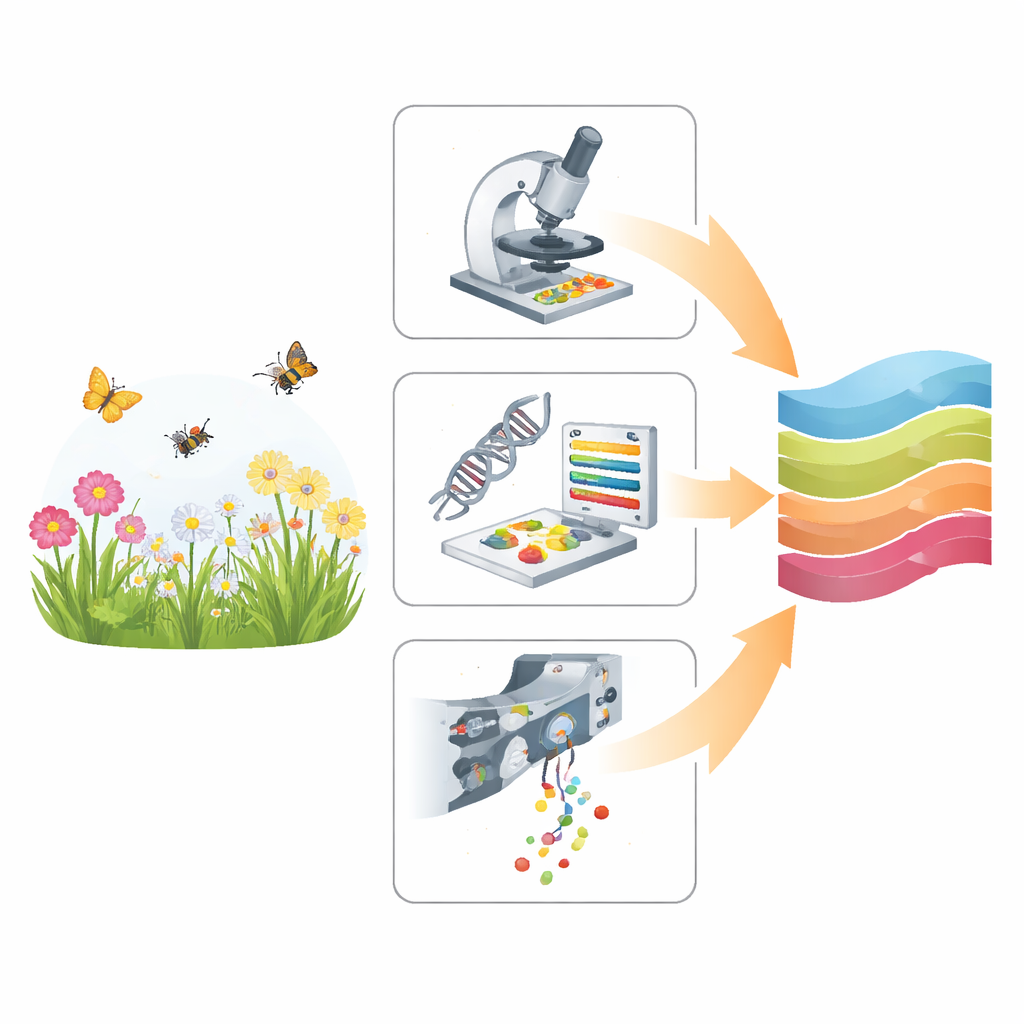
Tres maneras distintas de leer el polen
El estudio compara tres enfoques que parten del mismo material básico: mezclas de polen recogidas de flores y de cuerpos de insectos, pero extraen información de formas muy diferentes. La microscopía óptica tradicional depende de un experto que observa los granos ampliados y reconoce sus formas y patrones superficiales. El metabarcoding omite las formas y lee fragmentos cortos de ADN del polen, asociándolos con grandes bibliotecas genéticas de referencia. Una técnica más reciente, la citometría de flujo con imagen multiespectral (MIFC), hace pasar miles de granos frente a cámaras y sensores, capturando imágenes y señales de luz que un modelo informático utiliza para clasificarlos por especies. En conjunto, estos métodos cubren el espectro desde la observación manual lenta hasta el análisis altamente automatizado y de alto rendimiento.
Poner los métodos a prueba de forma justa
Para comparar el rendimiento, los investigadores primero construyeron mezclas “artificiales” de polen en el laboratorio a partir de nueve especies comunes de flores silvestres de praderas húngaras (Rumanía). Para estas muestras, se conocían las especies exactas y sus proporciones reales, lo que permitió una prueba directa de precisión. Crearon tres tipos de mezcla que diferían principalmente en la abundancia de polen de grano pequeño y luego dividieron porciones idénticas de cada mezcla para los tres métodos. En un segundo paso, analizaron polen que se había desprendido naturalmente de abejas silvestres, abejorros y moscas capturados en el campo, donde la composición real era desconocida pero reflejaba de cerca estudios ecológicos del mundo real.
¿Quién es mejor nombrando especies?
Cuando el reto era simplemente detectar qué tipos de plantas estaban presentes en las mezclas artificiales —sin pistas—, el metabarcoding de ADN fue el claro ganador. Detectó correctamente una mayor proporción de los géneros objetivo que la microscopía o la MIFC y produjo menos detecciones espurias. Al basarse en diferencias en el ADN en lugar de en la forma, el metabarcoding puede separar granos de aspecto similar e incluso distinguir especies estrechamente relacionadas, algo que a menudo supera a la vista humana y a los clasificadores de imágenes automáticos. Sin embargo, todos los métodos ocasionalmente pasaron por alto ciertos taxones, y las herramientas basadas en morfología fueron especialmente sensibles al polen que se había encogido o cambiado durante el almacenamiento, o que difería sutilmente de las imágenes de referencia utilizadas para entrenar el modelo informático.
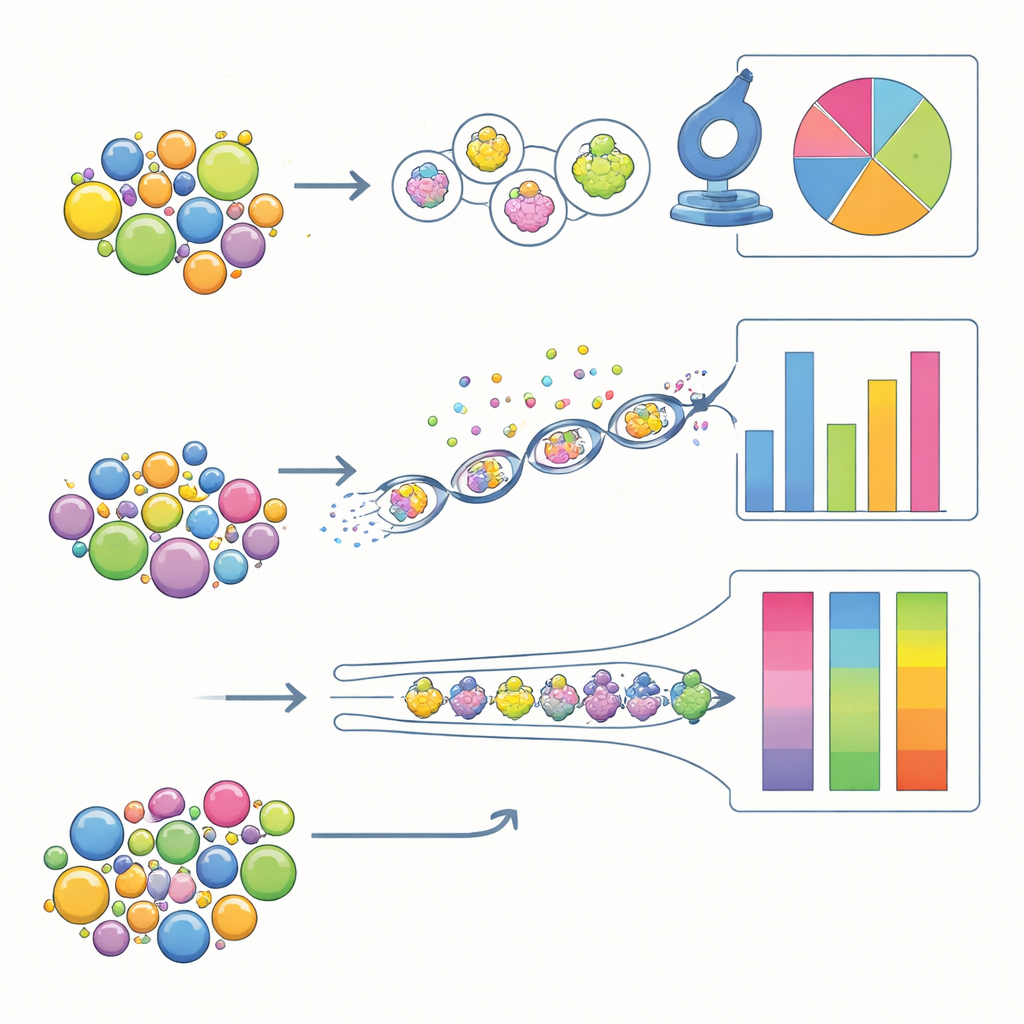
¿Quién es mejor a la hora de contar con justicia?
La precisión se vio diferente cuando la tarea fue estimar cuánto de cada tipo de polen estaba presente. Tras corregir las identificaciones erróneas y asumiendo que el conjunto de especies en la muestra era conocido, la microscopía tradicional se aproximó más a las proporciones reales en las mezclas artificiales, seguida por la MIFC. El metabarcoding fue el que peor resultado obtuvo en este aspecto: algunas especies aparecían sistemáticamente sobrerepresentadas en los conteos de lecturas de ADN, mientras que otras estaban subrepresentadas. Estos sesgos probablemente surgen de cantidades desiguales de ADN por grano, diferencias en la facilidad de extracción del ADN y peculiaridades del proceso de amplificación. La MIFC procesó muchos más granos que la microscopía y mostró en general buena precisión, pero su exactitud aún dependía en gran medida de hasta qué punto la biblioteca de imágenes reflejaba la variación real del polen.
Señales mezcladas de insectos reales
Cuando el equipo analizó polen de insectos silvestres, el acuerdo entre métodos cayó notablemente. Para algunos insectos que transportaban mayoritariamente un tipo de polen, los tres enfoques convergieron en imágenes similares. Sin embargo, en muestras más diversas, los métodos a menudo discreparon, incluso cuando las herramientas basadas en morfología fueron “orientadas” por la lista de especies obtenida por metabarcoding. Curiosamente, los dos métodos basados en imagen —microscopía óptica y MIFC— fueron los que peor coincidieron entre sí, mientras que ambos se alinearon algo mejor con los resultados de ADN. Estas discrepancias ponen de relieve cómo la manipulación de muestras, la aglomeración de granos, los efectos del almacenamiento y los puntos ciegos en cada biblioteca de referencia pueden dar forma a la imagen final de qué plantas ha visitado un insecto.
Una receta práctica para futuros trabajos sobre polen
Los autores concluyen que ninguna técnica por sí sola puede aún ofrecer tanto identificación perfecta como conteo perfecto. Para estudios que principalmente necesitan saber qué plantas se visitan, se recomienda el metabarcoding de ADN como la opción más fiable. Cuando la prioridad es cuantificar cuánto polen se transporta, la microscopía tradicional o la MIFC rinden mejor, con la MIFC ofreciendo una importante ventaja temporal para conjuntos de muestras grandes. Para obtener tanto la identidad como la abundancia relativa —la situación en muchos proyectos ecológicos y de conservación—, el estudio aboga por una estrategia en dos pasos: primero usar metabarcoding para construir una lista de plantas fiable para cada muestra y luego emplear esa información para guiar el conteo de alto rendimiento basado en imágenes, especialmente con MIFC. Según los autores, este enfoque combinado es adecuado para rastrear la polinización y las dietas de los polinizadores a través de las amplias escalas espaciales y temporales que exigen los retos actuales de biodiversidad y clima.
Cita: Motivans Švara, E., Rakosy, D., Knight, T.M. et al. Method comparison of microscopy, metabarcoding, and multispectral imaging flow cytometry for identification and relative abundance analysis of insect-dispersed pollen. Sci Rep 16, 12578 (2026). https://doi.org/10.1038/s41598-026-47800-3
Palabras clave: análisis de polen, polinizadores, metabarcoding de ADN, microscopía, citometría de flujo con imagen