Clear Sky Science · fr
Comparaison des méthodes de microscopie, métabarcoding et cytométrie d’imagerie en flux multispectrale pour l’identification et l’analyse de l’abondance relative du pollen dispersé par les insectes
Pourquoi compter le pollen est important
Le pollen peut ressembler à une simple poussière jaune, mais pour les fleurs sauvages, les cultures et les insectes qui les visitent, il représente une bouée de survie. Savoir quelles plantes les insectes fréquentent et quelle quantité de pollen ils transportent aide les scientifiques à suivre la santé des écosystèmes, la production alimentaire et la nutrition des pollinisateurs. Pourtant, identifier et compter ces grains microscopiques est un travail minutieux. Cet article pose une question pratique aux grandes implications : quels outils modernes font le meilleur travail pour nous dire quel pollen est présent et en quelles quantités sur les insectes pollinisateurs ?
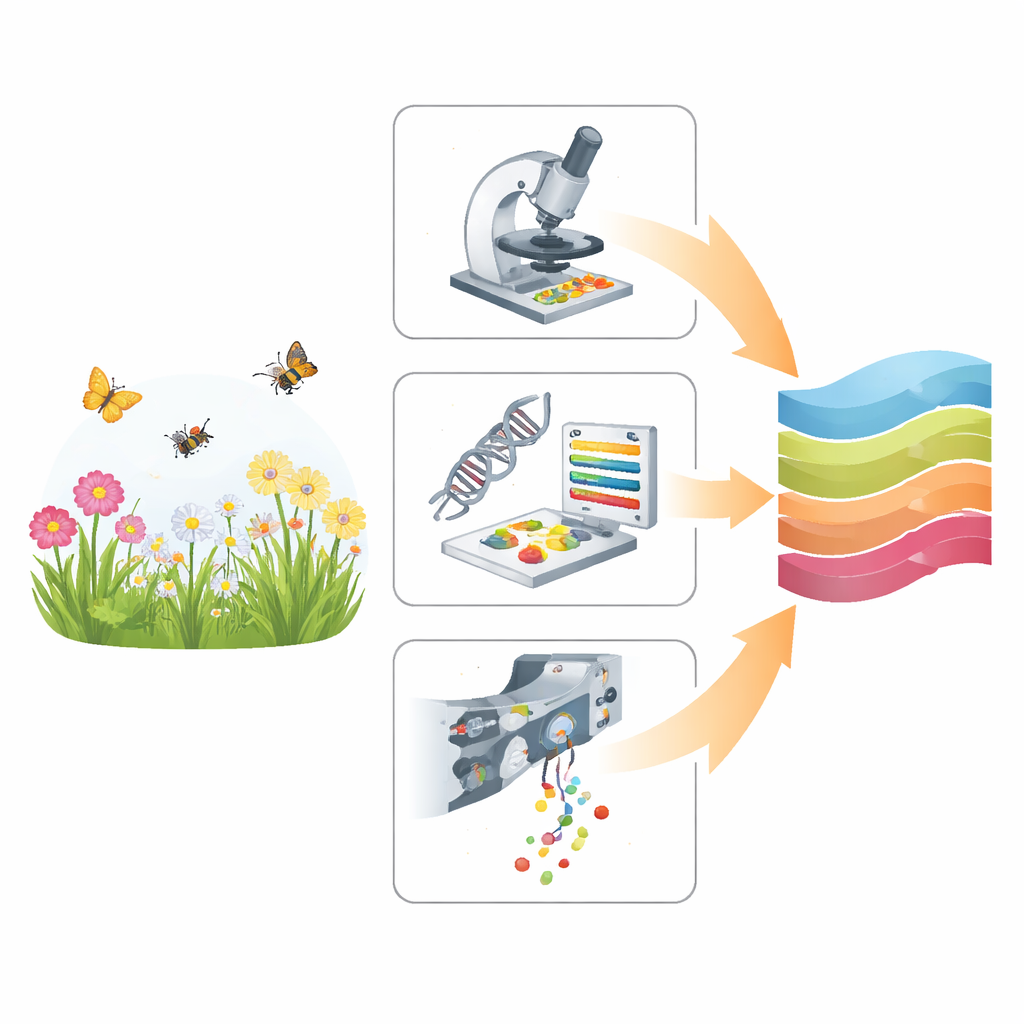
Trois manières différentes d’analyser le pollen
L’étude compare trois approches qui partent toutes du même matériau de base — des mélanges de pollen collectés sur des fleurs et sur des insectes — mais extraient l’information de façons très différentes. La microscopie optique traditionnelle repose sur un expert formé qui observe les grains grossis et reconnaît leurs formes et motifs de surface. Le métabarcoding passe outre les formes et lit de courts fragments d’ADN du pollen, les comparant à de larges bibliothèques génétiques de référence. Une technique plus récente, la cytométrie d’imagerie en flux multispectrale (MIFC), fait défiler des milliers de grains devant des caméras et des capteurs, capturant images et signaux lumineux qu’un modèle informatique utilise pour les trier par espèces. Ensemble, ces méthodes couvrent le spectre allant de l’observation lente et manuelle à l’analyse très automatisée et à haut débit.
Mettre les méthodes à l’épreuve de manière équitable
Pour comparer les performances, les chercheurs ont d’abord constitué des mélanges de pollen « artificiels » en laboratoire à partir de neuf espèces de fleurs sauvages communes des prairies de fauche roumaines. Pour ces échantillons, les espèces exactes et leurs proportions réelles étaient connues, ce qui permettait un test direct de l’exactitude. Ils ont créé trois types de mélanges qui différaient principalement par la fréquence du pollen à petit grain, puis ont réparti des portions identiques de chaque mélange entre les trois méthodes. Dans un second temps, ils ont analysé le pollen naturellement détaché d’abeilles sauvages, de bourdons et de mouches capturés sur le terrain, dont la composition réelle était inconnue mais reflétait fidèlement les études écologiques du monde réel.
Quelle méthode nomme le mieux les espèces ?
Quand le défi consistait simplement à détecter quelles plantes étaient présentes dans les mélanges artificiels — sans indices — le métabarcoding ADN est apparu comme le gagnant net. Il a correctement détecté une plus grande part des genres cibles que la microscopie ou la MIFC et a produit moins de détections erronées. Parce qu’il repose sur des différences d’ADN plutôt que sur la forme, le métabarcoding peut séparer des grains au même aspect et même distinguer des espèces étroitement apparentées, ce qui échappe souvent à l’œil humain et aux classificateurs d’images automatisés. Cependant, toutes les méthodes ont parfois manqué certains taxons, et les outils basés sur la morphologie étaient particulièrement sensibles au pollen qui avait rétréci ou changé pendant le stockage, ou qui différait subtilement des images de référence utilisées pour entraîner le modèle informatique.
Quelle méthode compte le plus justement ?
L’exactitude prenait un autre visage lorsque la tâche consistait à estimer la proportion de chaque type de pollen présent. Après correction des erreurs d’identification et en supposant que l’ensemble des espèces dans l’échantillon était connu, la microscopie traditionnelle s’est approchée le plus des proportions réelles dans les mélanges artificiels, suivie par la MIFC. Le métabarcoding a été le moins performant sur ce plan : certaines espèces étaient systématiquement sur‑représentées dans les comptes de lectures ADN, tandis que d’autres étaient sous‑représentées. Ces biais proviennent probablement d’une quantité d’ADN inégale par grain, de différences dans la facilité d’extraction de l’ADN et des particularités du processus d’amplification. La MIFC a traité beaucoup plus de grains que la microscopie et a montré une bonne précision en général, mais son exactitude dépendait néanmoins fortement de la qualité de la bibliothèque d’images pour refléter la variation réelle du pollen.
Signaux mélangés chez les insectes réels
Lorsque l’équipe s’est tournée vers le pollen provenant d’insectes sauvages, l’accord entre les méthodes a fortement diminué. Pour certains insectes portant majoritairement un type de pollen, les trois approches ont convergé vers des résultats semblables. Pour des échantillons plus diversifiés, en revanche, les méthodes étaient souvent en désaccord, même lorsque les outils basés sur la morphologie étaient « guidés » par la liste d’espèces fournie par le métabarcoding. Fait intéressant, les deux méthodes basées sur l’image — la microscopie optique et la MIFC — s’accordaient le moins, tandis que chacune d’elles s’alignait quelque peu mieux avec les résultats ADN. Ces divergences soulignent comment la manipulation des échantillons, l’agglutination des grains, les effets du stockage et les angles morts de chaque bibliothèque de référence peuvent tous façonner l’image finale de ce que visite un insecte.
Une recette pratique pour les travaux futurs sur le pollen
Les auteurs concluent qu’aucune technique unique ne peut encore fournir à la fois une identification parfaite et un comptage parfait. Pour les études qui cherchent surtout à savoir quelles plantes sont visitées, le métabarcoding ADN est recommandé comme option la plus fiable. Lorsque la priorité est de quantifier la quantité de pollen transportée, la microscopie traditionnelle ou la MIFC donnent de meilleurs résultats, la MIFC offrant un avantage de temps majeur pour les grands lots d’échantillons. Pour obtenir à la fois l’identité et l’abondance relative — situation courante dans de nombreux projets écologiques et de conservation — l’étude préconise une stratégie en deux étapes : utiliser d’abord le métabarcoding pour établir une liste fiable de plantes pour chaque échantillon, puis utiliser cette information pour guider un comptage à haut débit basé sur l’imagerie, en particulier avec la MIFC. Cette approche combinée, soutiennent les auteurs, est bien adaptée au suivi de la pollinisation et des régimes alimentaires des pollinisateurs à l’échelle spatiale et temporelle exigée par les défis actuels de la biodiversité et du climat.
Citation: Motivans Švara, E., Rakosy, D., Knight, T.M. et al. Method comparison of microscopy, metabarcoding, and multispectral imaging flow cytometry for identification and relative abundance analysis of insect-dispersed pollen. Sci Rep 16, 12578 (2026). https://doi.org/10.1038/s41598-026-47800-3
Mots-clés: analyse du pollen, pollinisateurs, métabarcoding ADN, microscopie, cytométrie d’imagerie en flux