Clear Sky Science · de
Methodenvergleich von Mikroskopie, Metabarcoding und multispektraler Imaging-Flow-Zytometrie zur Bestimmung und relativen Häufigkeitsanalyse von von Insekten verbreitetem Pollen
Warum das Zählen von Pollen wichtig ist
Pollen mag wie einfacher gelber Staub aussehen, für Wildblumen, Nutzpflanzen und die Insekten, die sie besuchen, ist er jedoch eine Lebensader. Zu wissen, welche Pflanzen Insekten besuchen und wie viel Pollen sie tragen, hilft Wissenschaftlern, die Gesundheit von Ökosystemen, die Nahrungsmittelproduktion und die Ernährung von Bestäubern zu überwachen. Das Identifizieren und Zählen dieser mikroskopischen Körnchen ist jedoch mühsame Detailarbeit. In dieser Studie wird eine praktische Frage mit weitreichenden Folgen gestellt: Welche modernen Methoden liefern die besten Informationen darüber, welche Pollen vorhanden sind und in welchen Mengen sie sich auf Bestäubern befinden?
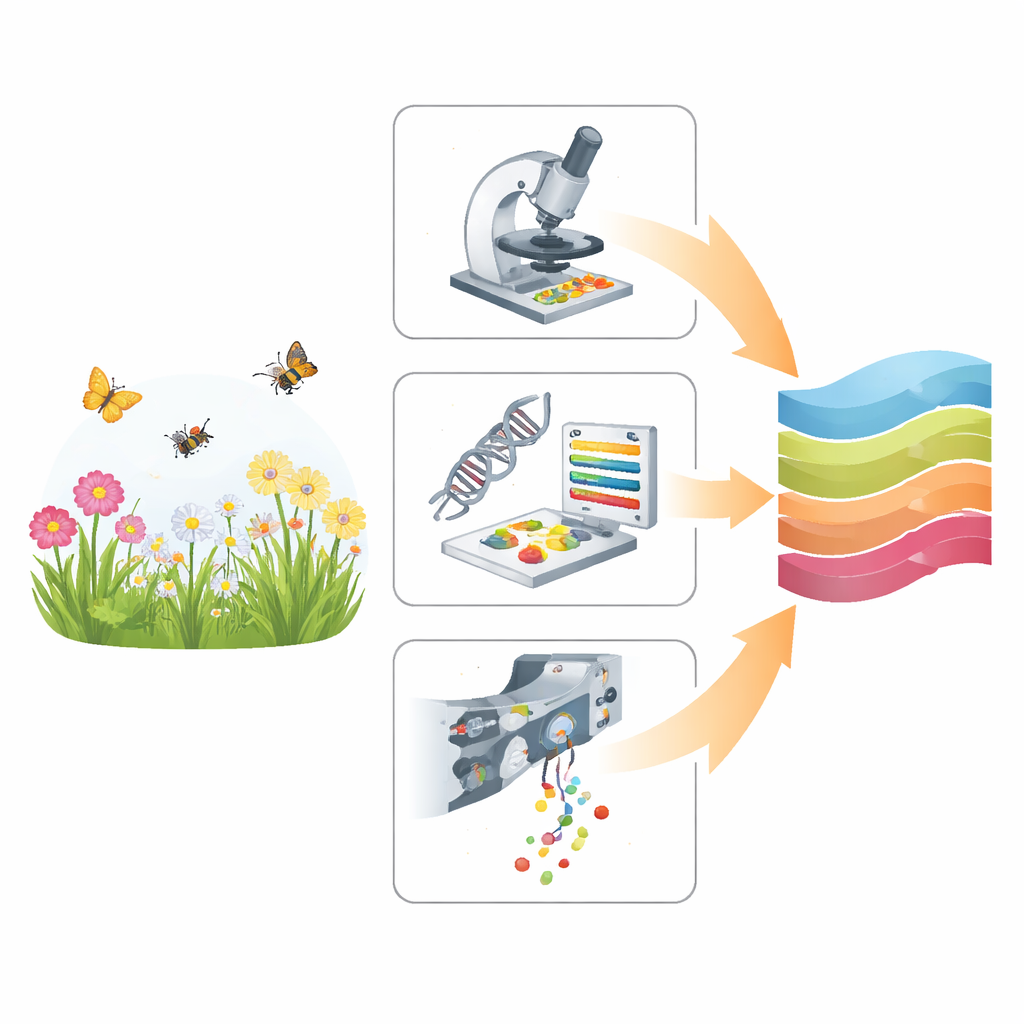
Drei verschiedene Wege, Pollen zu lesen
Die Studie vergleicht drei Ansätze, die alle vom gleichen Ausgangsmaterial ausgehen—gemischter Pollen, der von Blumen und Körpern von Insekten gesammelt wurde—aber Informationen auf sehr unterschiedliche Weise gewinnen. Die traditionelle Lichtmikroskopie setzt auf eine geschulte Fachperson, die vergrößerte Körnchen betrachtet und Form sowie Oberflächenstruktur erkennt. Metabarcoding überspringt die Formmerkmale und liest kurze DNA‑Fragmente aus dem Pollen, die mit großen genetischen Referenzdatenbanken abgeglichen werden. Eine neuere Technik, die multispektrale Imaging-Flow-Zytometrie (MIFC), lässt Tausende von Körnchen an Kameras und Sensoren vorbeiströmen und erfasst Bilder sowie Lichtsignale, die ein Computermodell zur Einordnung in Arten nutzt. Zusammen decken diese Methoden das Spektrum von langsamer, manueller Beobachtung bis hin zu hochautomatisierter, hochdurchsatzfähiger Analyse ab.
Die Methoden fair auf die Probe stellen
Um die Leistung zu vergleichen, stellten die Forschenden zunächst im Labor „künstliche“ Pollengemische aus neun häufigen Wildblumenarten aus rumänischen Heuwiesen her. Für diese Proben waren die exakten Arten und ihre tatsächlichen Anteile bekannt, sodass sich die Genauigkeit direkt testen ließ. Sie erzeugten drei Gemischtypen, die sich vor allem in der Häufigkeit von klein gekörntem Pollen unterschieden, und teilten von jedem Gemisch identische Portionen für alle drei Methoden auf. In einem zweiten Schritt analysierten sie Pollen, die natürlich von Wildbienen, Hummeln und Fliegen abgefallen waren, welche im Feld gefangen wurden; hier war die reale Zusammensetzung unbekannt, spiegelte aber reale ökologische Studien wider.
Wer ist am besten darin, Arten zu benennen?
Als die Aufgabe lediglich darin bestand, in den künstlichen Mischungen zu erkennen, welche Pflanzenarten vorhanden waren—ohne Hinweise—war das DNA‑Metabarcoding klar überlegen. Es erfasste einen höheren Anteil der Zielgenera als Mikroskopie oder MIFC und erzeugte weniger falsche Nachweise. Weil es auf DNA‑Unterschieden statt auf Formmerkmalen beruht, kann Metabarcoding ähnlich aussehende Körnchen auseinanderhalten und sogar nahe verwandte Arten unterscheiden, was dem menschlichen Auge und automatischen Bildklassifikatoren oft schwerfällt. Allerdings übersahen alle Methoden gelegentlich bestimmte Taxa, und die morphologiebasierten Verfahren reagierten besonders empfindlich auf Pollen, der beim Lagern geschrumpft oder verändert war oder der in feinen Details von den Referenzbildern abwich, mit denen das Computermodell trainiert worden war.
Wer kann am fairsten zählen?
Die Bewertung der Genauigkeit änderte sich, als die Aufgabe darin bestand, abzuschätzen, wie viel von jedem Pollentyp vorhanden war. Nach Korrektur von Fehlbestimmungen und unter der Annahme, dass die Artenzusammenstellung der Probe bekannt war, kam die traditionelle Mikroskopie den tatsächlichen Anteilen in den künstlichen Mischungen am nächsten, gefolgt von MIFC. Metabarcoding schnitt in dieser Hinsicht am schlechtesten ab: Einige Arten waren in den DNA‑Lesesätzen beständig überrepräsentiert, andere unterrepräsentiert. Diese Verzerrungen entstehen wahrscheinlich durch ungleiche DNA‑Mengen pro Körnchen, Unterschiede darin, wie leicht DNA extrahiert werden kann, und Eigenheiten des Amplifikationsprozesses. MIFC verarbeitete deutlich mehr Körnchen als die Mikroskopie und zeigte allgemein gute Präzision, doch seine Genauigkeit hing weiterhin stark davon ab, wie gut die Bildbibliothek die realweltliche Variation im Pollen abbildete.
Gemischte Signale von echten Insekten
Als das Team Pollen von Wildinsekten untersuchte, nahm die Übereinstimmung zwischen den Methoden deutlich ab. Bei einigen Insekten, die überwiegend einen Pollentyp trugen, lieferten alle drei Ansätze ähnliche Ergebnisse. Bei vielfältigeren Proben jedoch waren die Methoden oft uneinig, selbst wenn die morphologiebasierten Werkzeuge durch die Artenliste aus dem Metabarcoding „geleitet“ wurden. Interessanterweise wichen die beiden bildbasierten Methoden—Lichtmikroskopie und MIFC—am stärksten voneinander ab, während beide sich etwas besser an den DNA‑Ergebnissen orientierten. Diese Diskrepanzen zeigen, wie Probennahme, Verklumpung der Körnchen, Lagerungseffekte und Lücken in den jeweiligen Referenzbibliotheken das endgültige Bild davon beeinflussen können, welche Pflanzen ein Insekt besucht hat.
Ein praktisches Rezept für künftige Pollenarbeit
Die Autorinnen und Autoren kommen zu dem Schluss, dass keine Einzelmethode bisher sowohl perfekte Identifikation als auch perfektes Zählen liefern kann. Für Studien, die vor allem wissen müssen, welche Pflanzen besucht werden, wird DNA‑Metabarcoding als die verlässlichste Option empfohlen. Steht die Quantifizierung der mitgeführten Pollenmengen im Vordergrund, schneiden traditionelle Mikroskopie oder MIFC besser ab, wobei MIFC bei großen Probenmengen einen erheblichen Zeitvorteil bietet. Um sowohl Identität als auch relative Häufigkeit zu erhalten—wie es in vielen ökologischen und Naturschutzprojekten nötig ist—empfiehlt die Studie eine zweistufige Strategie: Zuerst Metabarcoding einsetzen, um für jede Probe eine verlässliche Pflanzenliste zu erstellen, und diese dann nutzen, um hochdurchsatzfähiges bildbasiertes Zählen zu steuern, insbesondere mit MIFC. Dieser kombinierte Ansatz, so argumentieren die Autoren, eignet sich gut, um Bestäubung und die Ernährung von Bestäubern über die großen räumlichen und zeitlichen Skalen zu verfolgen, die die heutige Biodiversitäts- und Klimaforschung verlangt.
Zitation: Motivans Švara, E., Rakosy, D., Knight, T.M. et al. Method comparison of microscopy, metabarcoding, and multispectral imaging flow cytometry for identification and relative abundance analysis of insect-dispersed pollen. Sci Rep 16, 12578 (2026). https://doi.org/10.1038/s41598-026-47800-3
Schlüsselwörter: Pollenanalyse, Bestäuber, DNA-Metabarcoding, Mikroskopie, Imaging-Flow-Zytometrie