Clear Sky Science · sv
Målinriktning mot STAT3‑vägen dämpar makrofaginflammation och hjärt-kärlskada i en modell för Kawasakis sjukdom
Varför en barnhjärtsjukdom spelar roll
Kawasakis sjukdom är en akut inflammatorisk sjukdom som framför allt drabbar barn under fem år och kan lämna bestående ärr på hjärtats blodkärl. Trots dagens standardbehandling med immunglobuliner (IVIG) och aspirin utvecklar vissa barn ändå utbuktningar eller förträngningar i kranskärlen, vilket ökar risken för hjärtinfarkt senare i livet. Denna studie undersöker ett nytt sätt att dämpa överaktiva immunceller som angriper blodkärlen vid Kawasakis sjukdom och pekar mot ett möjligt framtida läkemedel som bättre kan skydda barns hjärtan.
Immuncellerna som fyller hjärtats kärl
Läkare har länge vetat att Kawasakis sjukdom drivs av okontrollerad kärlinflammation, särskilt i kranskärlen som försörjer hjärtmuskeln. När forskare undersöker hjärtvävnad från drabbade patienter eller från musmodeller som efterliknar sjukdomen hittar de stora mängder makrofager — immunceller som normalt hjälper till att rensa infektioner — samlade i och runt kärlväggen. Vid Kawasakis sjukdom övergår många av dessa makrofager till ett mycket aggressivt tillstånd och släpper ut mängder av inflammatoriska molekyler som försvagar och skadar kärlet. Författarna använde en väletablerad musmodell, framkallad av ett bakteriecellväggsextrakt kallat LCWE, för att återskapa dessa kärlförändringar och studera hur makrofager bidrar till skadan.
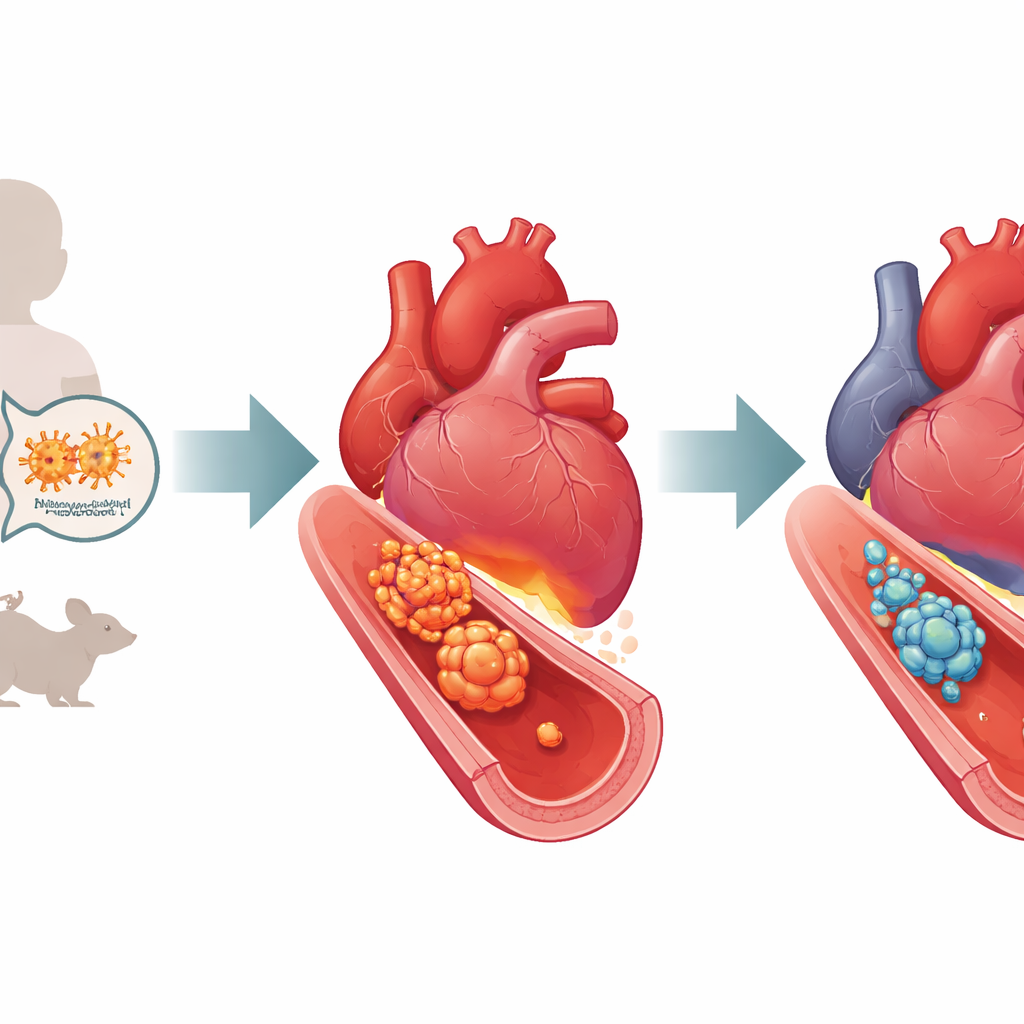
En molekylär omkopplare som höjer inflammationen
I makrofager fungerar ett protein kallat STAT3 som en kopplingscentral som slår på gener som driver inflammation. Teamet frågade först om denna omkopplare är aktiverad i deras Kawasaki‑lika modell. I odlade musmakrofager exponerade för LCWE fann de att den aktiverade, fosforylerade formen av STAT3 ökade kraftigt över tid, medan den totala mängden STAT3‑protein förblev oförändrad. Liknande aktivering syntes i hjärtvävnad från LCWE‑behandlade möss, där kärlinflammation och förtjockning var uttalade och nivåerna av flera inflammatoriska signaler var höga. Dessa fynd antyder att STAT3 inte bara finns närvarande utan aktivt driver makrofager mot ett skadligt, överstimulerat tillstånd i denna sjukdomsmodell.
Sänka signalen för att skydda kärlen
För att testa om blockering av STAT3 kunde tygla detta skadliga svar använde forskarna AG490, en liten molekyl som förhindrar att STAT3 aktiveras. Både i en makrofagcellinje och i primära makrofager tagna från möss reducerade förbehandling med AG490 före LCWE‑exponering kraftigt cellernas utsläpp av viktiga inflammatoriska faktorer, inklusive välkända cytokiner och enzymer som kan skada vävnad eller bryta ner kärlstrukturen. När teamet samlade "soppan" av substanser som frigjordes av dessa makrofager och applicerade den på muskranskärlets endotelceller — cellerna som bekläder insidan av hjärtkärlen — var skillnaden slående. Medium från obehandlade, LCWE‑stimulerade makrofager minskade endotelcellernas överlevnad och ökade markörer för skada, medan medium från AG490‑behandlade makrofager orsakade mindre skada, vilket tyder på att minskad STAT3‑aktivitet i makrofager indirekt skyddar kärlens innerfoder.
Från celler i skålar till hjärtan i levande möss
Gruppen gick sedan vidare till levande djur för att se om STAT3‑blockad kunde dämpa skador på hjärtats kärl i hela Kawasakisyndromet. Möss injicerades med LCWE för att framkalla vaskulit och behandlades i två veckor med antingen AG490 eller ett neutralt kontrollmedel. Fyra veckor efter LCWE‑exponering visade kontrollbehandlade möss täta immuncellsinfiltrat och förtjockade kranskärl, tillsammans med förhöjda nivåer av inflammatoriska proteiner i hjärtvävnaden. I kontrast hade möss som fick AG490 mildare kärlinflammation, tunnare artärväggar och lägre nivåer av samma inflammatoriska signaler. Viktigt nog tyder ytterligare tester på att AG490:s skyddande effekt främst verkade genom makrofager snarare än genom en direkt verkan på endotelceller, vilket understryker dessa immuncellers centrala roll och deras STAT3‑omkopplare i att driva kärlskada.
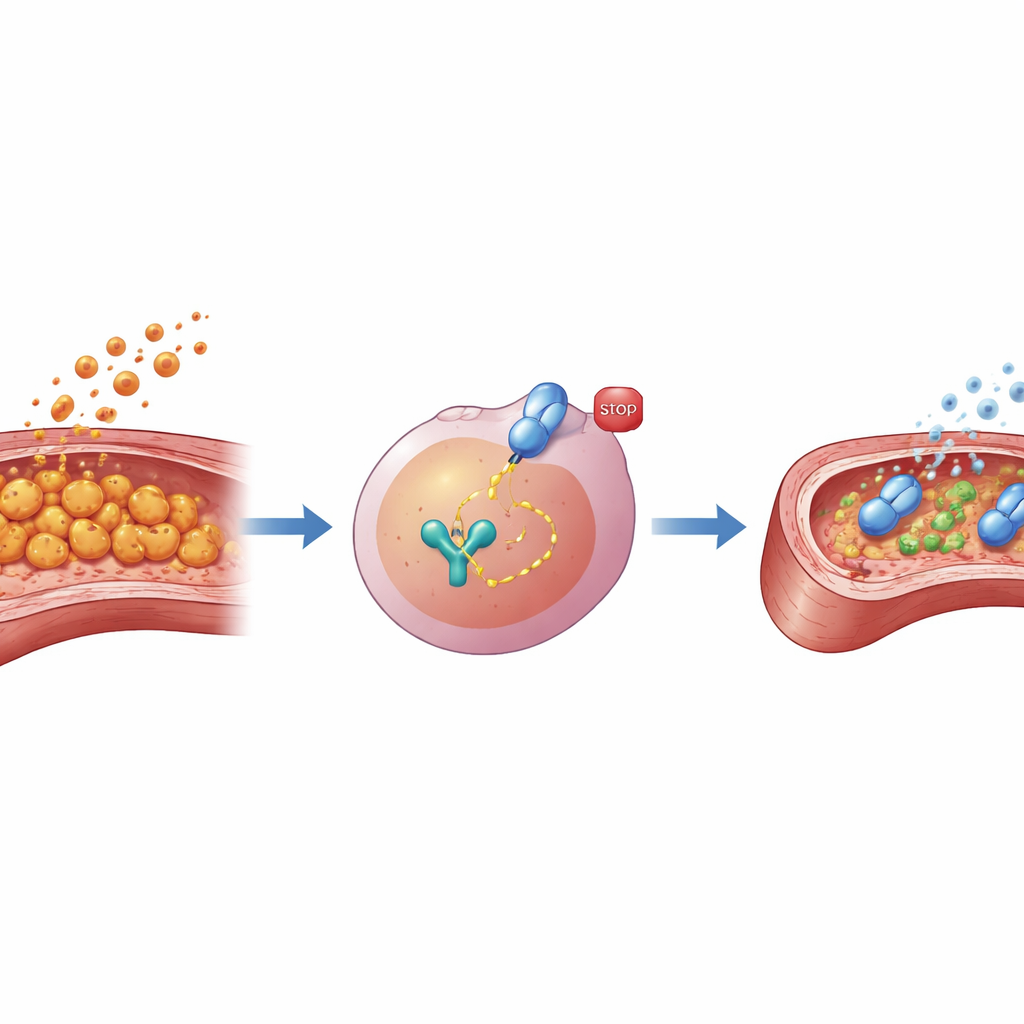
Vad detta kan betyda för barn med Kawasakis sjukdom
Tillsammans visar resultaten att STAT3 fungerar som en nyckelförstärkare av makrofagdriven inflammation och skada på hjärtats kärl i en musmodell av Kawasakis sjukdom, och att blockering av denna väg kan minska både de inflammatoriska signalerna och den strukturella skadan på kranskärlen. Medan AG490 i sig riktar sig mot ett uppströmsprotein och kanske inte blir det slutliga läkemedlet för patienter, placerar arbetet STAT3 som ett lovande mål för framtida terapier som kan komplettera nuvarande behandling och bättre förebygga långsiktiga hjärtkomplikationer. Ytterligare studier i djurmodeller och så småningom hos barn kommer att behövas för att utveckla säkrare, mer precisa STAT3‑hämmare och för att bekräfta att dämpning av denna väg tryggt kan minska Kawasakisrelaterade hjärtrisker.
Citering: Zheng, F., Xu, J., Bi, Y. et al. Targeting STAT3 pathway attenuates macrophages inflammation and cardiovascular injury in a model of Kawasaki disease. Sci Rep 16, 14358 (2026). https://doi.org/10.1038/s41598-026-45051-w
Nyckelord: Kawasakis sjukdom, makrofager, STAT3, kärlinflammation, pediatrisk hjärtsjukdom