Clear Sky Science · de
Die Hemmung des STAT3-Signalwegs verringert Makrophagen-Entzündung und kardiovaskuläre Schädigung in einem Modell der Kawasaki-Krankheit
Warum eine Kinderherzerkrankung wichtig ist
Die Kawasaki-Krankheit ist eine akute Entzündungskrankheit, die vor allem Kinder unter fünf Jahren betrifft und bleibende Schäden an den Herzgefäßen hinterlassen kann. Selbst mit der heute üblichen Therapie mit Antikörpern (IVIG) und Aspirin entwickeln einige Kinder weiterhin Ausbuchtungen oder Verengungen der Koronararterien, was ihr Risiko für Herzinfarkte im späteren Leben erhöht. Diese Studie untersucht einen neuen Weg, überaktives Verhalten von Immunzellen zu beruhigen, die in der Kawasaki-Krankheit Gefäße angreifen, und zeigt auf eine mögliche zukünftige Medizin, die die Herzen von Kindern besser schützen könnte.
Die Immunzellen, die die Herzgefäße überschwemmen
Ärzte wissen seit Langem, dass die Kawasaki-Krankheit durch eine entfesselte Entzündung in Blutgefäßen vorangetrieben wird, insbesondere in den Koronararterien, die den Herzmuskel versorgen. Bei der Untersuchung von Herzgewebe betroffener Patienten oder von Mausmodellen, die die Erkrankung nachahmen, finden Forschende große Ansammlungen von Makrophagen — Immunzellen, die normalerweise bei der Beseitigung von Infektionen helfen — in und um die Gefäßwand. Bei Kawasaki schalten viele dieser Makrophagen in einen hochaggressiven Zustand um und setzen Fluten entzündlicher Moleküle frei, die das Gefäß schwächen und schädigen. Die Autorinnen und Autoren verwendeten ein gut etabliertes Mausmodell, ausgelöst durch einen bakteriellen Zellwandextrakt namens LCWE, um diese Gefäßveränderungen zu reproduzieren und zu untersuchen, wie Makrophagen zur Schädigung beitragen.
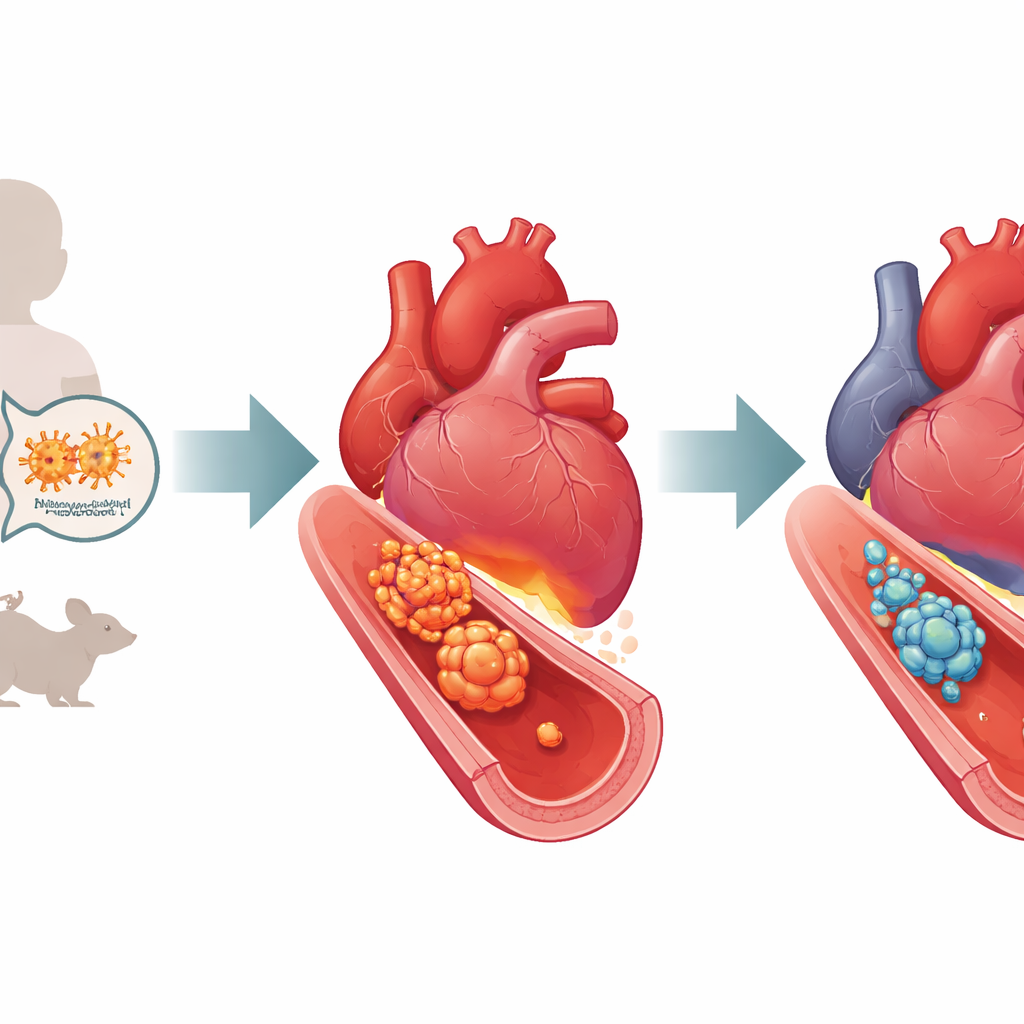
Ein molekularer Schalter, der die Entzündung hochdreht
Im Inneren von Makrophagen fungiert ein Protein namens STAT3 wie ein Schaltpult, das Gene aktiviert, die Entzündungen antreiben. Das Team fragte zunächst, ob dieser Schalter in ihrem Kawasaki-ähnlichen Modell eingeschaltet ist. In kultivierten Mausmakrophagen, die LCWE ausgesetzt wurden, stieg die aktivierte, phosphorylierte Form von STAT3 im Verlauf deutlich an, während die Gesamtmenge an STAT3-Protein gleich blieb. Eine ähnliche Aktivierung zeigte sich im Herzgewebe von LCWE-behandelten Mäusen, wo Gefäßentzündung und Wandverdickung ausgeprägt waren und die Konzentration mehrerer entzündlicher Signale erhöht war. Diese Befunde deuten darauf hin, dass STAT3 nicht nur vorhanden ist, sondern aktiv Makrophagen in einen schädigenden, übererregten Zustand treibt in diesem Krankheitsmodell.
Das Signal dämpfen, um Gefäße zu schützen
Um zu prüfen, ob die Blockade von STAT3 diese schädliche Reaktion eindämmen kann, setzten die Forschenden AG490 ein, ein kleines Molekül, das verhindert, dass STAT3 aktiviert wird. Sowohl in einer Makrophagen-Zelllinie als auch in primären Makrophagen aus Mäusen reduzierte eine Vorbehandlung mit AG490 vor LCWE-Exposition deutlich die Ausschüttung wichtiger entzündlicher Faktoren, darunter bekannte Zytokine und Enzyme, die Gewebe schädigen oder die Gefäßstruktur abbauen können. Als das Team die „Suppe“ von Substanzen, die von diesen Makrophagen freigesetzt wurde, sammelte und auf endotheliale Zellen der Maus-Koronararterien — die die Innenseite der Herzgefäße auskleiden — auftrug, war der Unterschied auffällig. Medium von unbehandelten, mit LCWE stimulierten Makrophagen verringerte das Überleben der Endothelzellen und erhöhte Verletzungsmarker, während Medium von AG490-behandelten Makrophagen weniger Schaden verursachte. Das legt nahe, dass das Herunterregeln von STAT3 in Makrophagen indirekt die Gefäßauskleidung schützt.
Von Zellen in der Schale zu Herzen in lebenden Mäusen
Die Gruppe ging dann zu lebenden Tieren über, um zu sehen, ob die STAT3-Blockade die Schäden an den Herzgefäßen im vollständigen Kawasaki-ähnlichen Syndrom lindern kann. Mäuse wurden mit LCWE injiziert, um eine Vaskulitis auszulösen, und zwei Wochen lang entweder mit AG490 oder einem neutralen Vehikel behandelt. Vier Wochen nach der LCWE-Exposition zeigten die vehikelbehandelten Mäuse dichte Infiltrate von Immunzellen und verdickte Koronararterien sowie erhöhte Konzentrationen entzündlicher Proteine im Herzgewebe. Im Gegensatz dazu wiesen Mäuse, die AG490 erhielten, mildere Gefäßentzündungen, dünnere Arterienwände und niedrigere Werte derselben entzündlichen Signale auf. Wichtig ist, dass zusätzliche Tests nahelegten, dass die schützende Wirkung von AG490 hauptsächlich über Makrophagen vermittelt wird und nicht direkt auf Endothelzellen wirkt, was die zentrale Rolle dieser Immunzellen und ihres STAT3-Schalters bei der Treibarbeit der Gefäßschädigung unterstreicht.
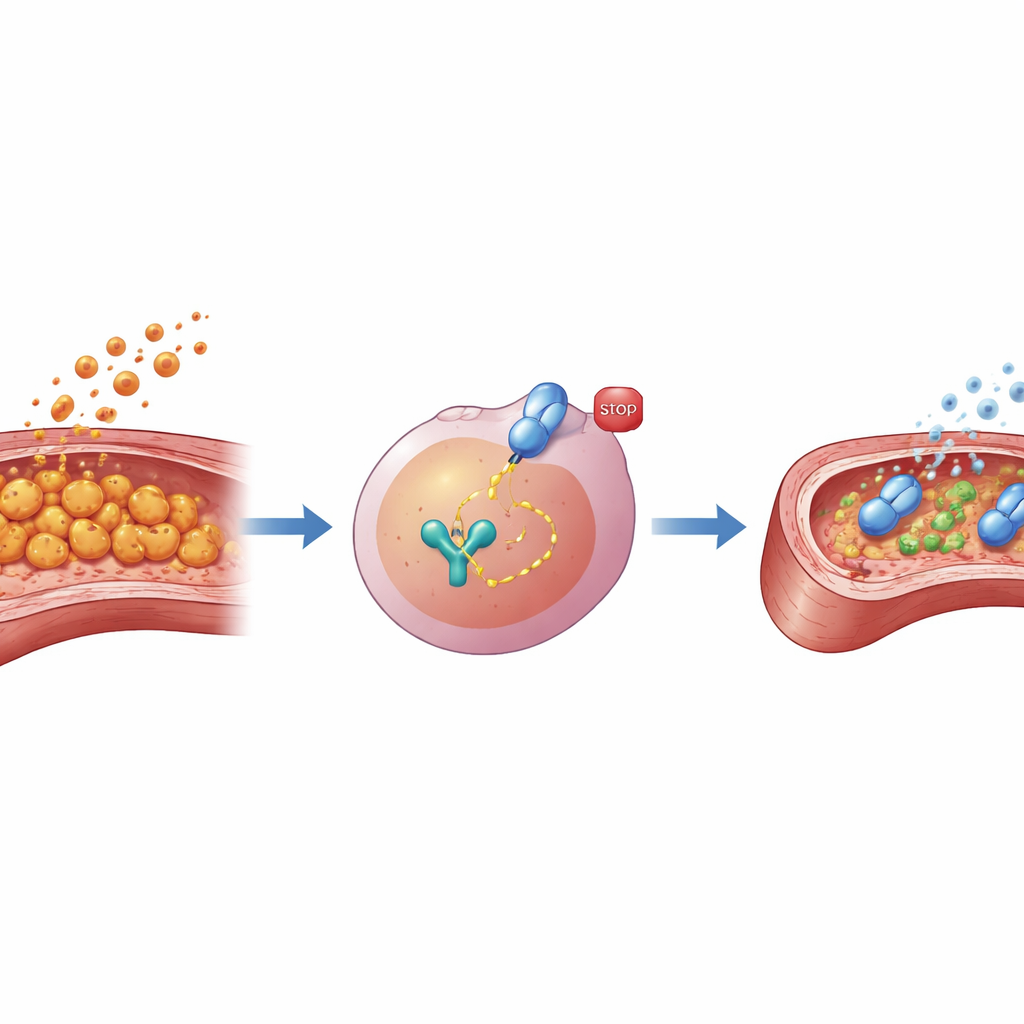
Was das für Kinder mit Kawasaki-Krankheit bedeuten könnte
Zusammengefasst zeigen die Ergebnisse, dass STAT3 als wichtiger Verstärker makrophagengetriebener Entzündung und Schädigung der Herzgefäße in einem Mausmodell der Kawasaki-Krankheit wirkt und dass die Blockade dieses Wegs sowohl die entzündlichen Signale als auch die strukturellen Schäden an den Koronararterien vermindern kann. Während AG490 selbst ein upstream-ligiertes Protein anvisiert und möglicherweise nicht das letztlich bei Patienten eingesetzte Medikament ist, positioniert die Arbeit STAT3 als vielversprechendes Ziel für künftige Therapien, die die aktuelle Behandlung ergänzen und Langzeitkomplikationen am Herzen besser verhindern könnten. Weiterführende Studien in Tiermodellen und letztlich bei Kindern werden nötig sein, um sichere, präzise STAT3-Blocker zu entwickeln und zu bestätigen, dass das Abschwächen dieses Wegs Kawasaki-bedingte Herzrisiken sicher reduziert.
Zitation: Zheng, F., Xu, J., Bi, Y. et al. Targeting STAT3 pathway attenuates macrophages inflammation and cardiovascular injury in a model of Kawasaki disease. Sci Rep 16, 14358 (2026). https://doi.org/10.1038/s41598-026-45051-w
Schlüsselwörter: Kawasaki-Krankheit, Makrophagen, STAT3, gefäßentzündung, pädiatrische Herzkrankheit