Clear Sky Science · it
Mirare la via STAT3 attenua l’infiammazione dei macrofagi e il danno cardiovascolare in un modello di malattia di Kawasaki
Perché una malattia cardiaca infantile importa
La malattia di Kawasaki è un’insorgenza infiammatoria acuta che colpisce principalmente i bambini sotto i cinque anni e può lasciare cicatrici durature sui vasi sanguigni del cuore. Anche con il trattamento standard odierno, che prevede immunoglobuline endovenose (IVIG) e aspirina, alcuni bambini sviluppano comunque dilatazioni o restringimenti delle arterie coronarie, aumentando il rischio di infarti in età adulta. Questo studio esplora un nuovo modo per calmare le cellule immunitarie iperattive che attaccano i vasi nella malattia di Kawasaki, indicando una possibile futura terapia in grado di proteggere meglio il cuore dei bambini.
Le cellule immunitarie che affollano i vasi cardiaci
I medici sanno da tempo che la malattia di Kawasaki è guidata da un’infiammazione sfrenata nei vasi, in particolare nelle arterie coronarie che nutrono il muscolo cardiaco. Quando i ricercatori esaminano il tessuto cardiaco di pazienti colpiti o di modelli murini che riproducono la malattia, trovano un gran numero di macrofagi—cellule immunitarie che normalmente aiutano a eliminare le infezioni—raggruppati dentro e intorno alla parete vascolare. Nella malattia di Kawasaki molti di questi macrofagi passano a uno stato altamente aggressivo, rilasciando ondate di molecole infiammatorie che indeboliscono e danneggiano il vaso. Gli autori hanno usato un modello murino consolidato, indotto da un estratto di parete cellulare batterica chiamato LCWE, per riprodurre questi cambiamenti vascolari e studiare come i macrofagi contribuiscono al danno.
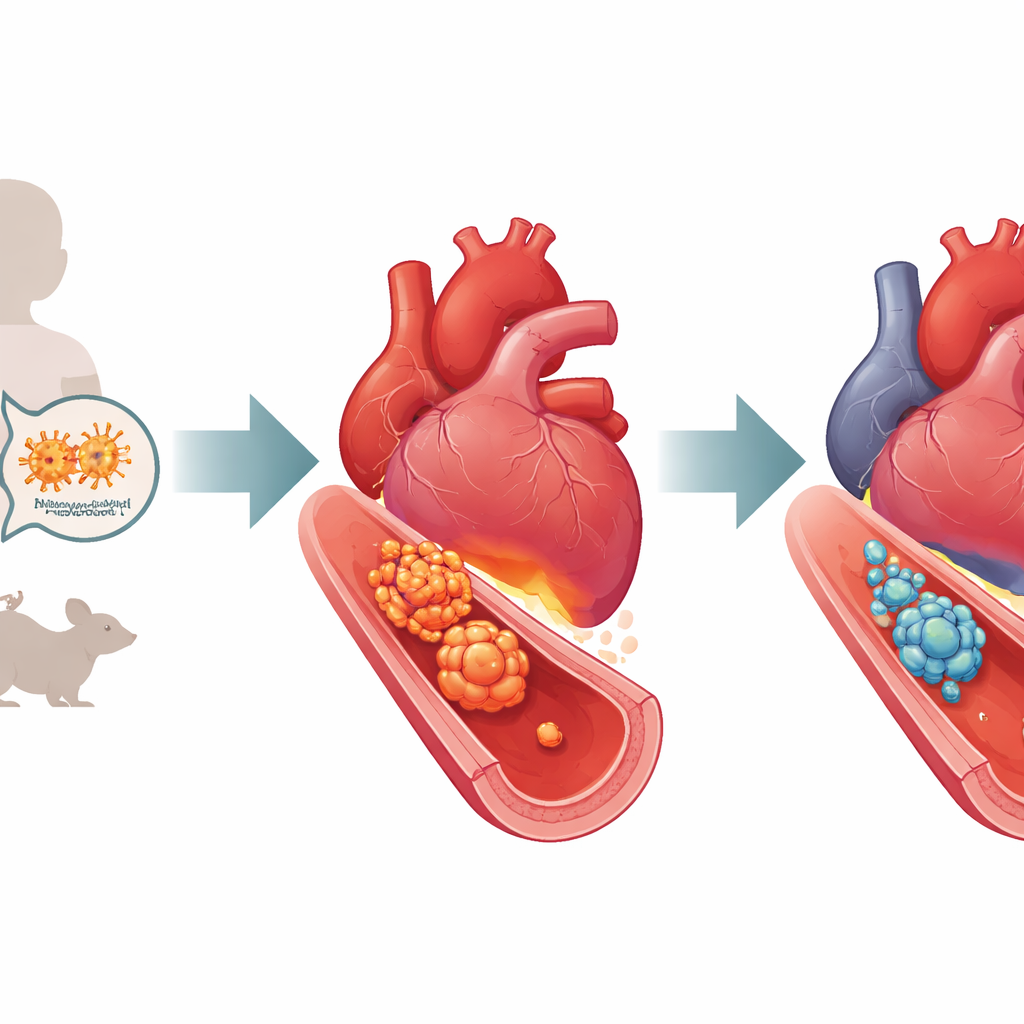
Un interruttore molecolare che aumenta l’infiammazione
All’interno dei macrofagi, una proteina chiamata STAT3 funziona come un commutatore, attivando geni che guidano l’infiammazione. Il gruppo ha prima verificato se questo interruttore fosse acceso nel loro modello simile alla Kawasaki. In macrofagi murini coltivati esposti a LCWE hanno osservato che la forma attivata e fosforilata di STAT3 aumentava rapidamente nel tempo, mentre la quantità totale di proteina STAT3 rimaneva invariata. Una simile attivazione è apparsa anche nel tessuto cardiaco di topi trattati con LCWE, dove l’infiammazione e l’ispessimento dei vasi erano pronunciati e i livelli di diversi segnali infiammatori erano elevati. Questi risultati suggeriscono che STAT3 non è solo presente, ma spinge attivamente i macrofagi verso uno stato dannoso e iperattivato in questo modello di malattia.
Abbassare il segnale per proteggere i vasi
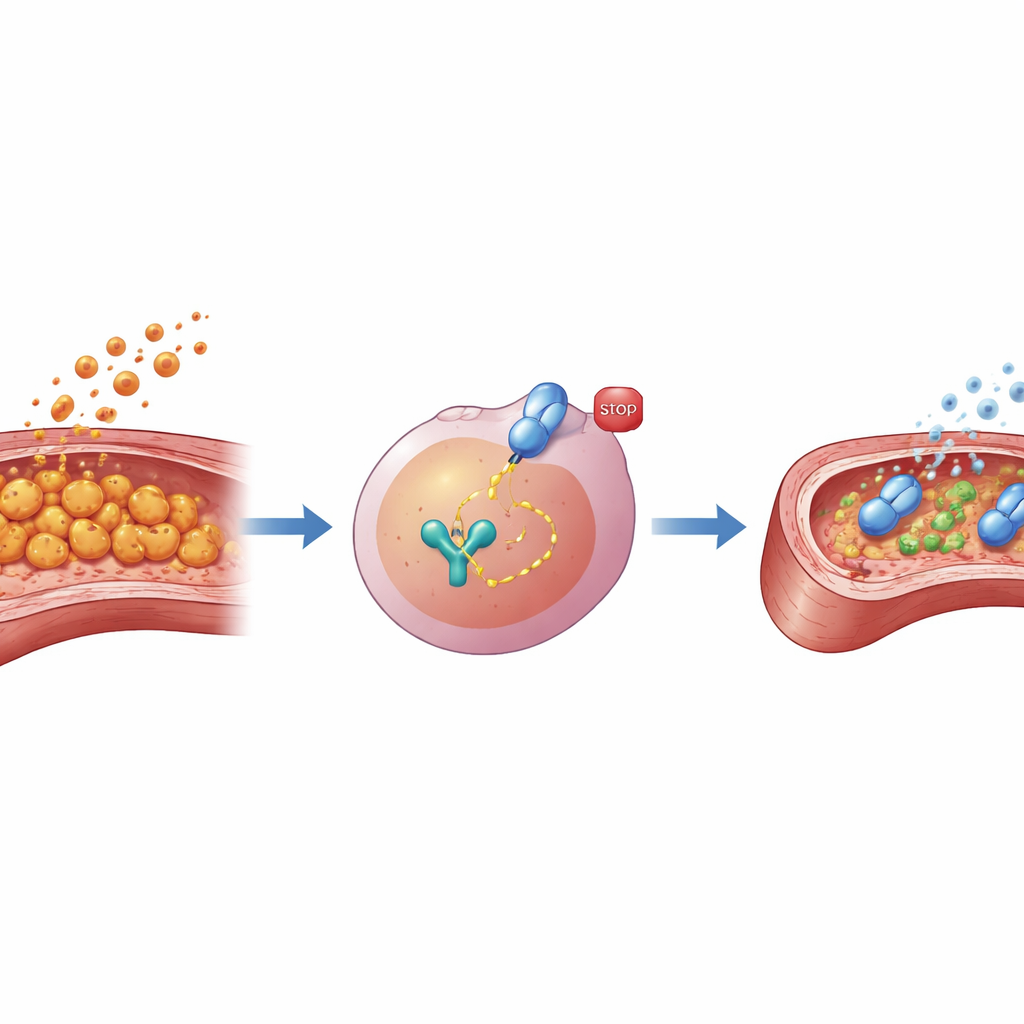
Per verificare se bloccare STAT3 potesse contenere questa risposta dannosa, i ricercatori hanno utilizzato AG490, una piccola molecola che impedisce l’attivazione di STAT3. In una linea cellulare di macrofagi e in macrofagi primari raccolti da topi, il pretrattamento con AG490 prima dell’esposizione a LCWE ha ridotto drasticamente la produzione di fattori infiammatori chiave, comprese citochine note ed enzimi in grado di danneggiare i tessuti o degradare la struttura vascolare. Quando il gruppo ha raccolto il “brodo” di sostanze rilasciate da questi macrofagi e lo ha applicato a cellule endoteliali di arterie coronarie murine—le cellule che rivestono l’interno dei vasi cardiaci—la differenza è stata netta. Il mezzo proveniente da macrofagi stimolati con LCWE non trattati riduceva la sopravvivenza endoteliale e aumentava i marcatori di danno, mentre il mezzo da macrofagi trattati con AG490 provocava meno lesioni, suggerendo che abbassare STAT3 nei macrofagi protegge indirettamente l’endotelio vascolare.
Dalle cellule in coltura ai cuori nei topi vivi
Il gruppo è quindi passato agli animali vivi per valutare se il blocco di STAT3 potesse attenuare il danno vascolare nel quadro completo della sindrome simile alla Kawasaki. Ai topi è stato somministrato LCWE per indurre vasculite e trattati per due settimane con AG490 o con un veicolo neutro. A quattro settimane dall’esposizione a LCWE, i topi trattati con il veicolo mostravano densi infiltrati di cellule immunitarie e arterie coronarie ispessite, insieme a livelli elevati di proteine infiammatorie nel tessuto cardiaco. Al contrario, i topi trattati con AG490 presentavano un’infiammazione vascolare più lieve, pareti arteriose più sottili e livelli inferiori degli stessi segnali infiammatori. Di rilievo, test aggiuntivi hanno suggerito che l’effetto protettivo di AG490 operava principalmente tramite i macrofagi, piuttosto che agire direttamente sulle cellule endoteliali, sottolineando il ruolo centrale di queste cellule immunitarie e del loro interruttore STAT3 nel promuovere il danno vascolare.
Cosa potrebbe significare per i bambini con malattia di Kawasaki
Complessivamente, i risultati mostrano che STAT3 agisce come un importante amplificatore dell’infiammazione mediata dai macrofagi e del danno ai vasi cardiaci in un modello murino della malattia di Kawasaki, e che bloccare questa via può ridurre sia i segnali infiammatori sia il danno strutturale alle arterie coronarie. Pur essendo AG490 un inibitore che agisce a monte e non necessariamente il farmaco definitivo per i pazienti, il lavoro individua STAT3 come un bersaglio promettente per future terapie che potrebbero integrare il trattamento attuale e prevenire meglio le complicanze cardiache a lungo termine. Saranno necessari ulteriori studi in modelli animali e, infine, nei bambini per perfezionare inibitori di STAT3 più sicuri e specifici e per confermare che attenuare questa via possa ridurre in modo sicuro i rischi cardiaci associati alla Kawasaki.
Citazione: Zheng, F., Xu, J., Bi, Y. et al. Targeting STAT3 pathway attenuates macrophages inflammation and cardiovascular injury in a model of Kawasaki disease. Sci Rep 16, 14358 (2026). https://doi.org/10.1038/s41598-026-45051-w
Parole chiave: malattia di Kawasaki, macrofagi, STAT3, infiammazione vascolare, malattie cardiache pediatriche