Clear Sky Science · ru
Таргетирование пути STAT3 ослабляет воспаление макрофагов и повреждение сердечно-сосудистой системы в модели болезни Кавасаки
Почему детальное сердечное заболевание важно
Болезнь Кавасаки — это внезапное воспалительное заболевание, которое главным образом поражает детей до пяти лет и может оставлять длительные рубцы на сосудах сердца. Даже при современной стандартной терапии антителами (IVIG) и аспирином некоторые дети все равно развивают выпячивания или сужения коронарных артерий, что повышает риск инфарктов в будущем. В этом исследовании рассматривается новый подход к угнетению чрезмерно активных иммунных клеток, атакующих сосуды при болезни Кавасаки, что указывает на возможный будущий препарат, способный лучше защищать детские сердца.
Иммунные клетки, скапливающиеся в сосудах сердца
Врачи давно знают, что болезнь Кавасаки обусловлена неконтролируемым воспалением в сосудах, особенно в коронарных артериях, питающих сердечную мышцу. При изучении сердечной ткани пациентов или мышиных моделей, имитирующих болезнь, исследователи обнаруживают большое количество макрофагов — иммунных клеток, которые обычно помогают устранять инфекции — скопленных в стенке сосуда и вокруг неё. При болезни Кавасаки многие из этих макрофагов переходят в крайне агрессивное состояние, выделяя потоки воспалительных молекул, которые ослабляют и повреждают сосуд. Авторы использовали хорошо зарекомендовавшую себя мышиную модель, индуцируемую бактериальным клеточным экстрактом LCWE, чтобы воспроизвести эти сосудистые изменения и изучить вклад макрофагов в повреждение.
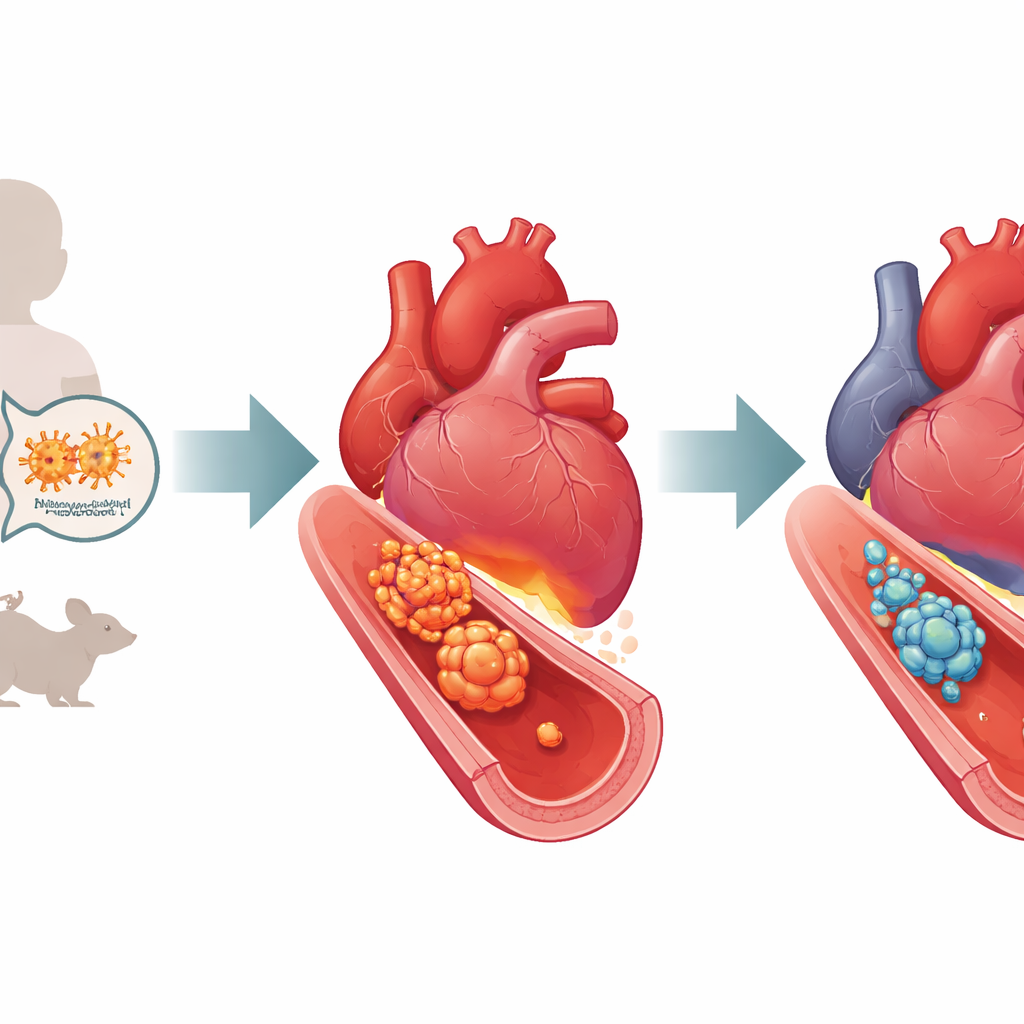
Молекулярный переключатель, усиливающий воспаление
Внутри макрофагов белок STAT3 действует как оператор коммутационной станции, включая гены, управляющие воспалением. Команда сначала проверила, активирован ли этот переключатель в их модели, похожей на болезнь Кавасаки. В культивированных мышиных макрофагах, подвергнутых воздействию LCWE, они обнаружили, что активированная, фосфорилированная форма STAT3 резко увеличивалась с течением времени, тогда как общий уровень белка STAT3 оставался неизменным. Подобная активация наблюдалась в сердечной ткани у мышей, получавших LCWE, где воспаление сосудов и утолщение были выражены, а уровни нескольких провоспалительных сигналов были повышены. Эти результаты указывали на то, что STAT3 не просто присутствует, а активно сдвигает макрофаги в повреждающее, чрезмерно возбужденное состояние в этой модели заболевания.
Понижение сигнала для защиты сосудов
Чтобы проверить, может ли блокада STAT3 сдержать этот вредный ответ, исследователи использовали AG490, малую молекулу, препятствующую активации STAT3. Как в клеточной линии макрофагов, так и в первичных макрофагах, взятых у мышей, предподготовка AG490 до воздействия LCWE резко уменьшала продукцию ключевых провоспалительных факторов, включая известные цитокины и ферменты, которые могут повреждать ткани или разрушать структуру сосудов. Когда команда собрала «суспензии» веществ, выделяемых этими макрофагами, и нанесла их на эндотелиальные клетки коронарных артерий мыши — клетки, выстилающие внутреннюю поверхность сосудов сердца — разница была поразительной. Среда от нелеченых макрофагов, стимулированных LCWE, снижала выживаемость эндотелиальных клеток и повышала маркеры повреждения, тогда как среда от макрофагов, обработанных AG490, вызывала меньше повреждений, что предполагает, что подавление STAT3 в макрофагах косвенно защищает выстилку сосудов.
От клеток в чашке до сердец живых мышей
Группа затем перешла к живым животным, чтобы выяснить, может ли блокада STAT3 смягчить повреждение сосудов сердца в полной картине, похожей на синдром Кавасаки. Мышей вводили LCWE для индукции васкулита и лечили в течение двух недель либо AG490, либо нейтральным растворителем. Через четыре недели после введения LCWE у мышей, получавших растворитель, наблюдали плотные инфильтраты иммунных клеток и утолщение коронарных артерий, а также повышенные уровни воспалительных белков в сердечной ткани. Напротив, мыши, получавшие AG490, имели более лёгкое воспаление сосудов, тоньшие стенки артерий и более низкие уровни тех же воспалительных сигналов. Важно, что дополнительные тесты показали, что защитный эффект AG490 действовал в основном через макрофаги, а не напрямую на эндотелиальные клетки, подчёркивая центральную роль этих иммунных клеток и их переключателя STAT3 в развитии повреждения сосудов.
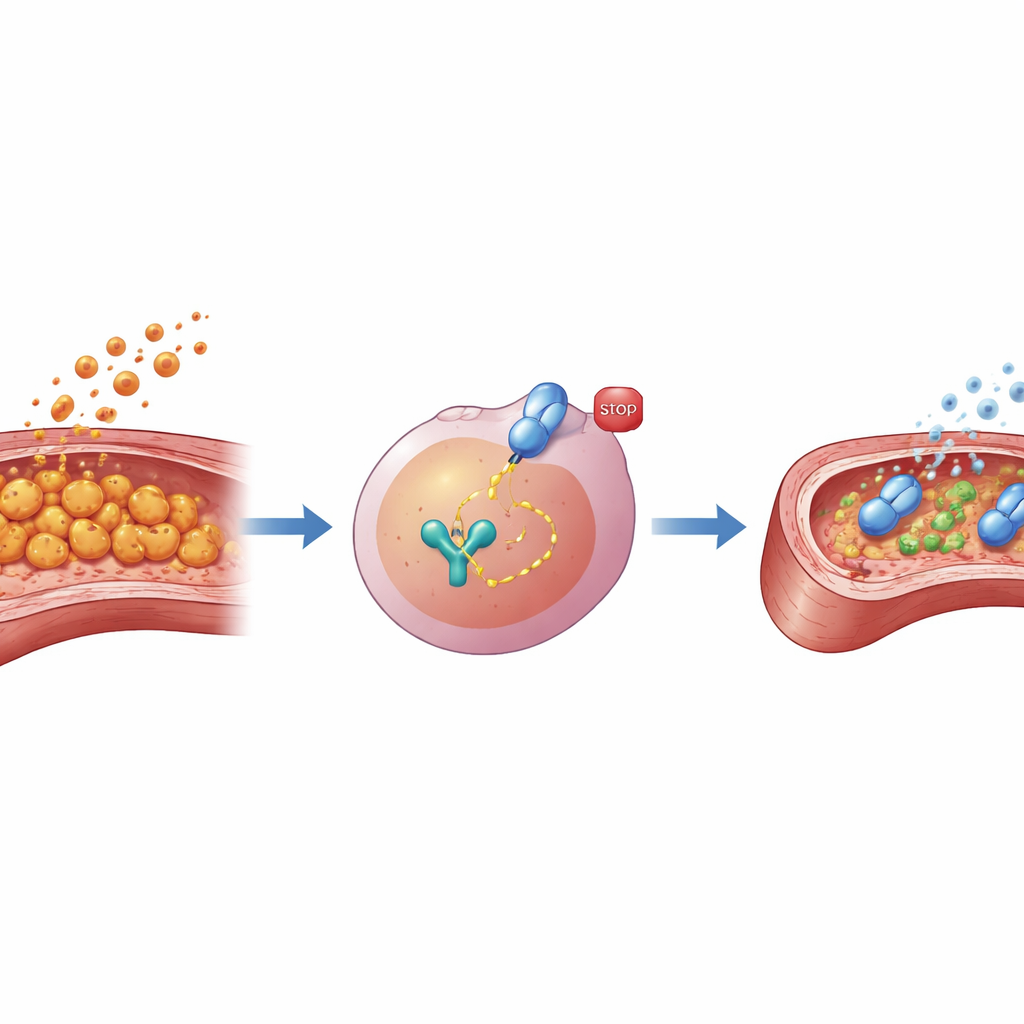
Что это может означать для детей с болезнью Кавасаки
В целом результаты показывают, что STAT3 является ключевым усилителем макрофаг-опосредованного воспаления и повреждения сосудов сердца в мышиной модели болезни Кавасаки, и что блокирование этого пути может уменьшить как провоспалительные сигналы, так и структурное повреждение коронарных артерий. Хотя сам AG490 нацелен на белок, действующий вверх по каскаду, и, возможно, не станет конечным препаратом для применения у пациентов, работа выделяет STAT3 как перспективную мишень для будущих терапий, которые могли бы дополнить текущие методы лечения и лучше предотвращать долгосрочные сердечные осложнения. Потребуются дальнейшие исследования на животных моделях и, в конечном счёте, у детей, чтобы разработать более безопасные и точные ингибиторы STAT3 и подтвердить, что подавление этого пути может безопасно снижать сердечные риски, связанные с болезнью Кавасаки.
Цитирование: Zheng, F., Xu, J., Bi, Y. et al. Targeting STAT3 pathway attenuates macrophages inflammation and cardiovascular injury in a model of Kawasaki disease. Sci Rep 16, 14358 (2026). https://doi.org/10.1038/s41598-026-45051-w
Ключевые слова: болезнь Кавасаки, макрофаги, STAT3, сосудистое воспаление, детские сердечные заболевания