Clear Sky Science · sv
AI-baserade förutsägelsemodeller från time-lapse-avbildning för bra embryon med implantationspotential och euploidi
Varför detta betyder något för hoppfulla föräldrar
För personer som genomgår in vitro-fertilisering (IVF) kan valet av vilket embryo som ska överföras skilja mellan ännu ett hjärtskärande bakslag och en framgångsrik graviditet. I dag baseras besluten ofta på hur embryon ser ut i mikroskop eller på invasiva genetiska tester där celler tas från embryot. Denna studie utforskar en annan väg: att använda artificiell intelligens (AI) för att följa embryons tillväxt över tid och tyst uppskatta vilka som mest sannolikt kommer att implantera och vilka som sannolikt har rätt antal kromosomer — allt utan att beröra embryot.
Från stillbilder till rörliga bilder
Traditionellt graderar embryologer embryon utifrån ett fåtal stillbilder och bedömer egenskaper som form och cellordning. Dessa graderingar är subjektiva och visar inte tillförlitligt om ett embryo har korrekt kromosomantal, en nyckelfaktor vid missfall. Genetiska tester kan besvara den frågan men kräver att celler avlägsnas från embryot. I detta arbete använde forskarna istället kontinuerliga time-lapse-videor inspelade i speciella inkubatorer. Dessa videor visar subtila förändringar i celldelning och utveckling under de första dagarna efter befruktningen, inklusive detaljer som är för fina eller för snabba för att ögat konsekvent ska fånga.
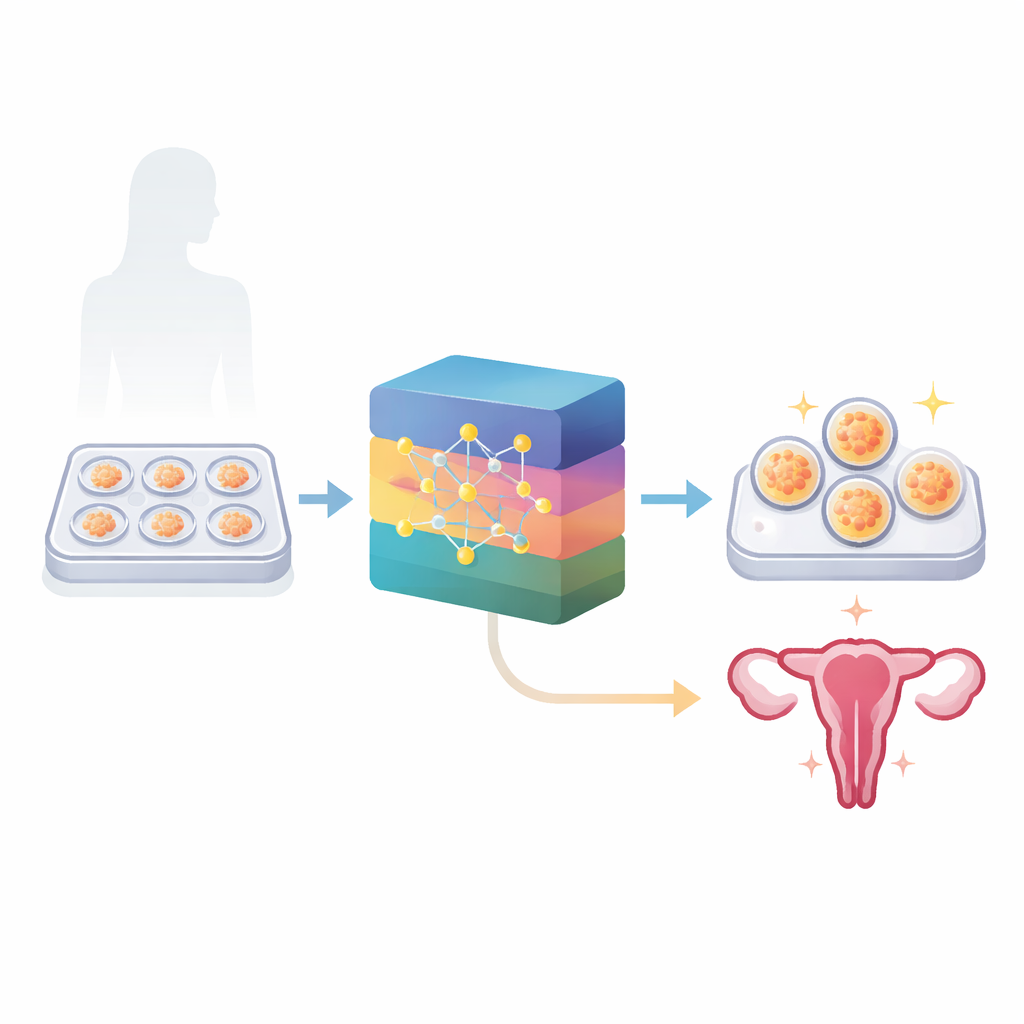
Träna AI att läsa tidigt liv på film
Teamet byggde två AI-modeller som lärde sig direkt från dessa embryofilmer tillsammans med moderns ålder. En modell uppskattade sannolikheten för att ett överfört embryo skulle leda till en klinisk graviditet (bekräftad med ultraljud). Den andra uppskattade om ett embryo sannolikt var ”euploid”, det vill säga hade rätt antal kromosomer, baserat på resultat från standard genetisk testning som gjordes på vissa embryon. Tillsammans innehöll dataseten över 2 400 embryon för graviditetsförutsägelse och mer än 1 600 för kromosomstatus. Istället för att förlita sig på människors utvalda markörer granskade AI:n hela videoströmmen och fångade tidpunkt och mönster i utvecklingen bildruta för bildruta.
Hur väl modellerna presterade
För att testa tillförlitligheten tränade forskarna en ensemble — tio separata versioner — av varje modell och kombinerade deras utslag så att ingen enskild modell dominerade beslutet. De utvärderade prestanda i tre oberoende grupper: en valideringsuppsättning, en intern testuppsättning och en extern testuppsättning från andra IVF-kliniker. Båda modellerna visade god förmåga att skilja embryon med bättre utfall från dem med sämre utfall. För graviditetsprognosen var modellens noggrannhet högst när den fokuserade på de första 20 till 50 timmarna av utveckling, vilket tyder på att mycket tidiga celldelningar rymmer starka ledtrådar om senare framgång. För kromosomstatus höll prestandan sig stark över hela odlingsperioden, vilket innebär att användbara signaler finns genom embryots tidiga tillväxt.
Vad poängen kan betyda i kliniken
I verklig IVF-praktik måste läkare avgöra vilka embryon som ska överföras eller testas vidare, inte bara rangordna dem. Forskarna valde därför praktiska gränsvärden för poäng med hjälp av valideringsdata och tillämpade dem oförändrade på testklinikerna, för att efterlikna verklig implementering. För graviditetsprognosen behöll det valda tröskelvärdet de flesta embryon som slutligen ledde till graviditet samtidigt som många som inte implanterade sorterades bort. För kromosomprognosen behöll tröskeln en stor andel av de embryon som tester visade var kromosomalt normala och satte åt sidan många som sannolikt var abnorma. Författarna betonar att dessa verktyg är tänkta att stödja, inte ersätta, kliniskt omdöme — hjälpa till att prioritera embryon, minska behovet av invasiv testning när det inte är lämpligt och potentiellt förkorta tiden till en framgångsrik graviditet.
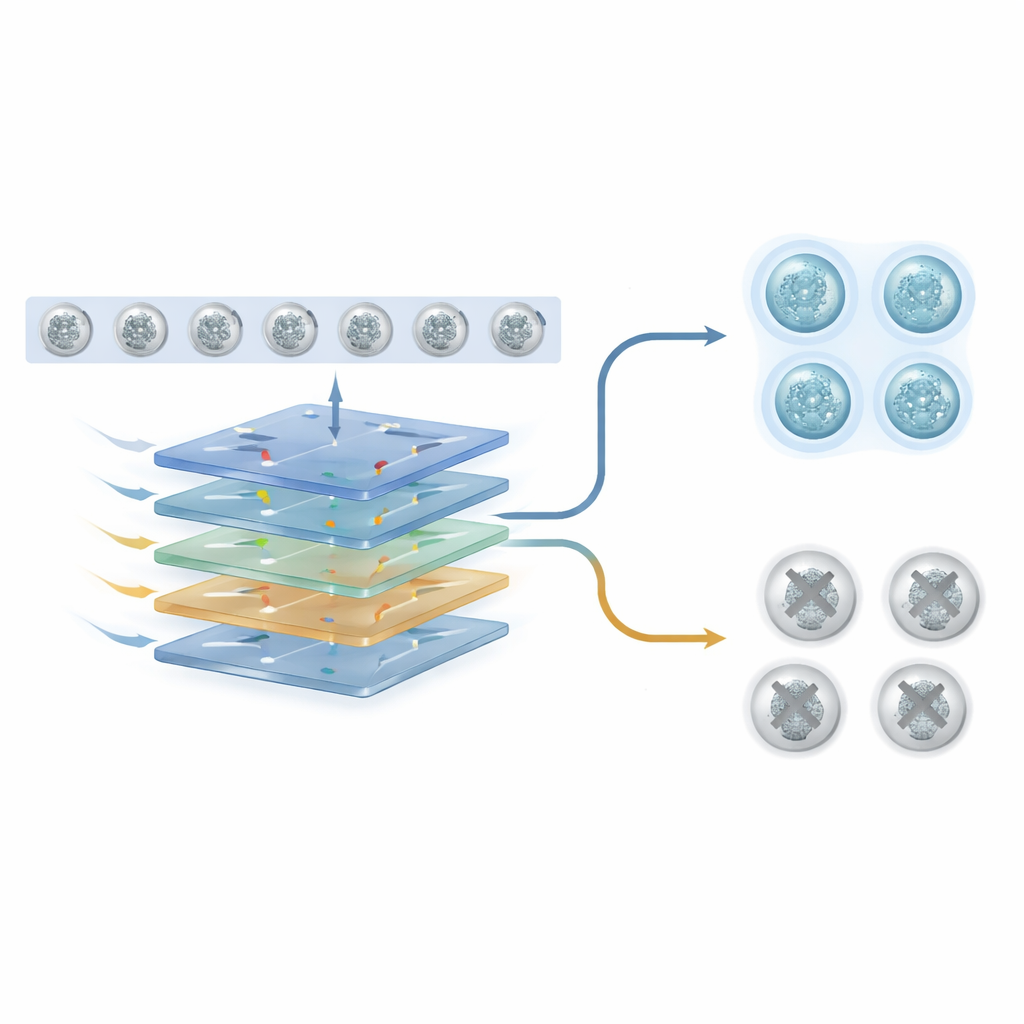
Framåt mot skonsammare embryourval
För en icke-specialist är huvudbudskapet att datorer nu kan lära sig av korta filmer av embryon för att ge icke-invasiva ledtrådar om vilka som är mest lovande. Genom att observera hur embryon delar sig och förändras från allra första början kan AI fånga information som mänskliga ögon och enstaka stillbilder kan missa. Även om ytterligare prövningar i mer varierade kliniker och patientgrupper behövs, pekar detta tillvägagångssätt mot IVF-behandlingar där embryoval är mer objektivt, säkrare och mindre beroende av biopsier — och erbjuder en skonsammare väg till att bilda familj.
Citering: Maekawa, R., Kiritani, T., Abe, T. et al. AI prediction models based on time-lapse imaging for good embryos with implantation potential and euploidy. Sci Rep 16, 9864 (2026). https://doi.org/10.1038/s41598-026-40917-5
Nyckelord: IVF, embryoval, time-lapse-avbildning, artificiell intelligens, icke-invasiv testning