Clear Sky Science · de
KI-Vorhersagemodelle auf Basis von Zeitrafferaufnahmen für vielversprechende Embryonen mit Implantationspotenzial und Euploidie
Warum das für hoffende Eltern wichtig ist
Für Paare und Einzelpersonen, die eine In-vitro-Fertilisation (IVF) durchlaufen, kann die Auswahl des Embryos, der übertragen wird, den Unterschied zwischen einer weiteren herzzerreißenden Enttäuschung und einer erfolgreichen Schwangerschaft bedeuten. Heute beruhen Entscheidungen häufig auf dem Aussehen der Embryonen unter dem Mikroskop oder auf invasiven genetischen Tests, bei denen Zellen vom Embryo entnommen werden. Diese Studie untersucht einen anderen Weg: den Einsatz von künstlicher Intelligenz (KI), die Embryonen beim Wachstum über die Zeit beobachtet und ohne Eingriff schätzt, welche am ehesten implantieren und welche wahrscheinlich die korrekte Chromosomenanzahl haben.
Von Momentaufnahmen zu Bewegtbildern
Traditionell bewerten Embryologen Embryonen anhand weniger Standbilder und beurteilen Merkmale wie Form und Zellanordnung. Diese Bewertungen sind subjektiv und geben nicht zuverlässig Auskunft darüber, ob ein Embryo die richtige Chromosomenanzahl hat — ein entscheidender Faktor für Fehlgeburten. Genetische Tests können diese Frage beantworten, erfordern jedoch die Entnahme von Zellen aus dem Embryo. In dieser Arbeit nutzten die Forschenden stattdessen kontinuierliche Zeitraffer-Videos, die in speziellen Inkubatoren aufgezeichnet wurden. Diese Videos zeigen subtile Veränderungen in der Zellteilung und Entwicklung während der ersten Tage nach der Befruchtung, darunter Details, die für das menschliche Auge zu fein oder zu schnell sind, um sie konsistent zu verfolgen.
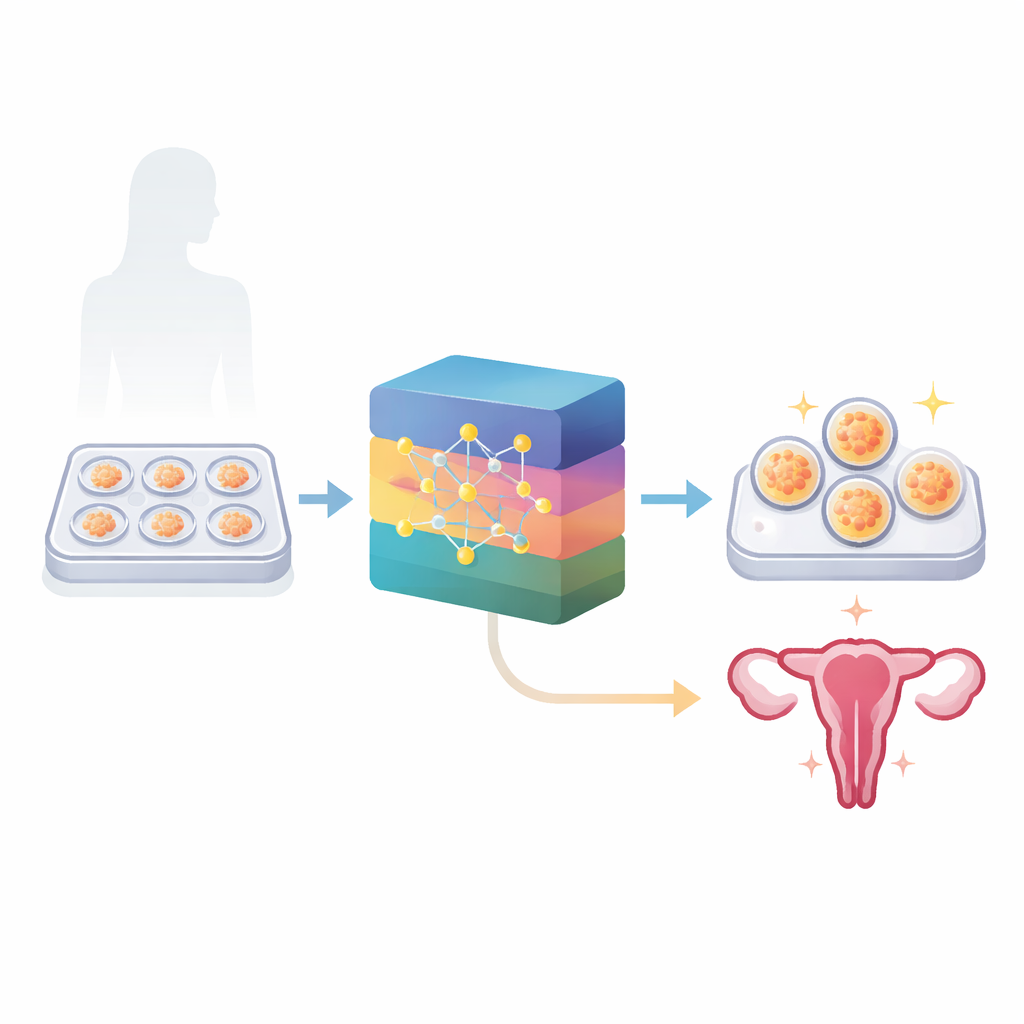
KI trainieren, frühes Leben im Film zu lesen
Das Team entwickelte zwei KI-Modelle, die direkt aus diesen Embryonenvideos zusammen mit dem Alter der Mutter lernten. Ein Modell schätzte die Wahrscheinlichkeit, dass ein transferierter Embryo zu einer klinischen Schwangerschaft führt (per Ultraschall bestätigt). Das andere schätzte, ob ein Embryo wahrscheinlich „euploid“ ist, also die korrekte Chromosomenanzahl besitzt, basierend auf Ergebnissen standardmäßiger genetischer Tests an einigen Embryonen. Insgesamt umfassten die Datensätze mehr als 2.400 Embryonen zur Schwangerschaftsvorhersage und über 1.600 zur Chromosomenbestimmung. Anstatt sich auf vom Menschen gewählte Marker zu verlassen, analysierte die KI den vollständigen Videostream und erfasste Zeitpunkt und Muster der Entwicklung Bild für Bild.
Wie gut die Modelle abschnitten
Zur Prüfung der Zuverlässigkeit trainierten die Forschenden für jedes Modell ein Ensemble — zehn separate Versionen — und kombinierten deren Ausgaben, sodass kein einzelnes Modell die Entscheidung dominierte. Sie evaluierten die Leistung in drei unabhängigen Gruppen: einem Validierungsdatensatz, einem internen Testdatensatz und einem externen Testdatensatz aus verschiedenen IVF-Kliniken. Beide Modelle zeigten eine gute Fähigkeit, Embryonen mit besseren Aussichten von solchen mit schlechteren zu trennen. Für die Schwangerschaftsvorhersage war die Genauigkeit des Modells am höchsten, wenn es sich auf die ersten 20 bis 50 Stunden der Entwicklung konzentrierte, was darauf hindeutet, dass sehr frühe Zellteilungen starke Hinweise auf späteren Erfolg liefern. Für den Chromosomenstatus blieb die Leistung über den gesamten Kulturzeitraum hinweg stabil, was bedeutet, dass während des frühen Wachstums des Embryos durchgehend nützliche Signale vorhanden sind.
Was die Scores in der Klinik bedeuten könnten
In der praktischen IVF-Praxis müssen Ärzte entscheiden, welche Embryonen transferiert oder weiter getestet werden sollen — nicht nur sie zu ordnen. Die Forschenden wählten daher praktische Score-Schwellenwerte anhand der Validierungsdaten und wandten diese unverändert auf die Testkliniken an, um einen realen Einsatz zu simulieren. Für die Schwangerschaftsvorhersage behielt die gewählte Schwelle die meisten Embryonen, die letztlich zu einer Schwangerschaft führten, während viele, die nicht implantierten, ausgeschlossen wurden. Für die Chromosomenvorhersage behielt die Schwelle einen großen Anteil Embryonen, die durch Tests als chromosomal normal erwiesen, und sortierte viele wahrscheinlich abnormale Embryonen aus. Die Autorinnen und Autoren betonen, dass diese Werkzeuge die klinische Beurteilung unterstützen und nicht ersetzen sollen — sie helfen, Embryonen zu priorisieren, den Bedarf an invasiven Tests zu verringern, wenn diese nicht praktikabel sind, und womöglich die Zeit bis zu einer erfolgreichen Schwangerschaft zu verkürzen.
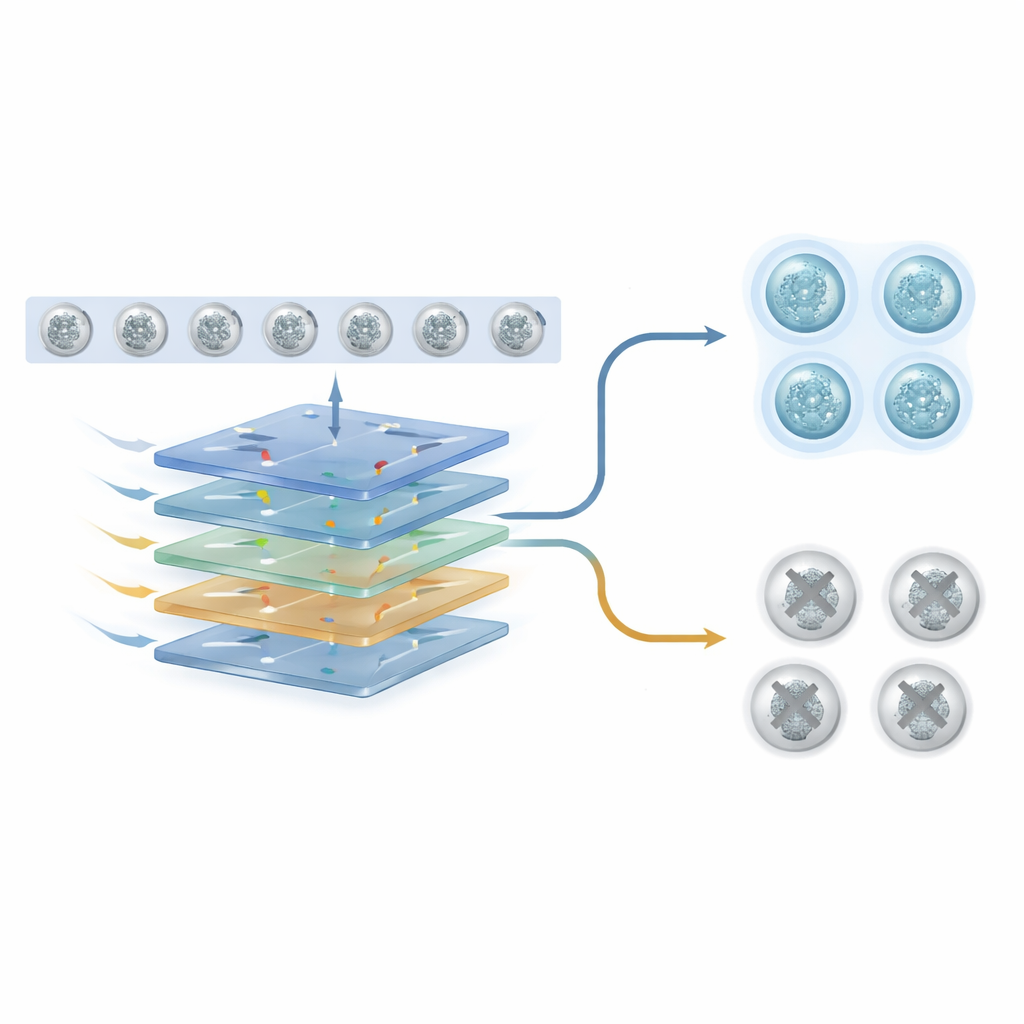
Ausblick auf eine schonendere Embryonenauswahl
Für Nicht-Spezialisten lautet die Kernaussage, dass Computer nun aus kurzen Filmen von Embryonen lernen können, um nicht-invasive Hinweise zu liefern, welche am vielversprechendsten sind. Indem sie beobachten, wie Embryonen von Anfang an teilen und sich verändern, kann KI Informationen erfassen, die dem menschlichen Auge und Einzelaufnahmen entgehen. Obwohl weitere Tests in vielfältigeren Kliniken und Patientengruppen nötig sind, weist dieser Ansatz auf IVF-Behandlungen hin, bei denen die Embryonenauswahl objektiver, sicherer und weniger biopsieabhängig ist — und so einen schonenderen Weg zum Familienaufbau bieten könnte.
Zitation: Maekawa, R., Kiritani, T., Abe, T. et al. AI prediction models based on time-lapse imaging for good embryos with implantation potential and euploidy. Sci Rep 16, 9864 (2026). https://doi.org/10.1038/s41598-026-40917-5
Schlüsselwörter: IVF, Embryonenauswahl, Zeitrafferaufnahmen, künstliche Intelligenz, nicht-invasive Tests