Clear Sky Science · nl
AI-voorspellingsmodellen op basis van time-lapse-opnames voor goede embryo’s met implantatiepotentieel en euploidie
Waarom dit belangrijk is voor hoopvolle ouders
Voor mensen die een in-vitrofertilisatie (IVF) ondergaan, kan de keuze welk embryo overgezet wordt het verschil betekenen tussen nog een hartverscheurend teleurstelling en een succesvolle zwangerschap. Vandaag de dag berusten beslissingen vaak op hoe embryo’s eruitzien onder een microscoop of op invasieve genetische tests waarbij cellen uit het embryo worden genomen. Deze studie onderzoekt een andere weg: het gebruik van kunstmatige intelligentie (AI) om embryo’s over tijd te observeren en stilletjes in te schatten welke het meest waarschijnlijk zullen innestelen en welke waarschijnlijk het juiste aantal chromosomen hebben — allemaal zonder het embryo aan te raken.
Van stilstaande beelden naar bewegende beelden
Traditioneel beoordelen embryologen embryo’s op basis van enkele stilstaande beelden en oordelen ze over kenmerken zoals vorm en celdispositie. Deze scores zijn subjectief en geven niet betrouwbaar aan of een embryo het juiste chromosoomaantal heeft, een belangrijke factor bij miskramen. Genetische tests kunnen die vraag beantwoorden, maar vereisen het wegnemen van cellen uit het embryo. In dit werk gebruikten onderzoekers in plaats daarvan continue time-lapse-video’s die in speciale incubatoren zijn vastgelegd. Deze video’s tonen subtiele veranderingen in celdeling en ontwikkeling in de eerste dagen na bevruchting, inclusief details die te fijn of te snel zijn voor het menselijke oog om consequent te volgen.
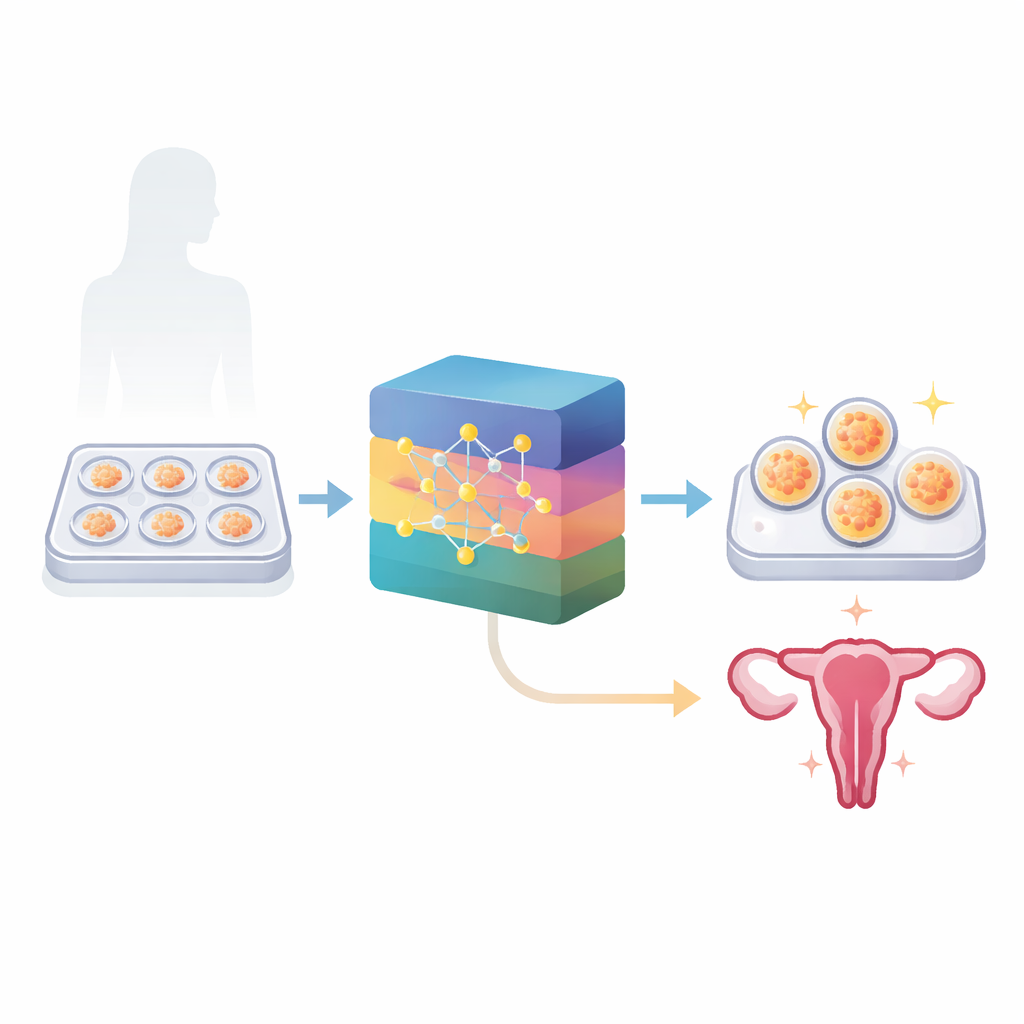
AI trainen om vroeg leven op film te lezen
Het team bouwde twee AI-modellen die rechtstreeks leerden van deze embryo-filmpjes plus de leeftijd van de moeder. Het ene model schatte de kans dat een overgezet embryo zou leiden tot een klinische zwangerschap (bevestigd door echo). Het andere schatte of een embryo waarschijnlijk euploid was, wat betekent dat het het juiste aantal chromosomen heeft, op basis van resultaten van standaard genetische tests die bij sommige embryo’s waren uitgevoerd. Gezamenlijk bevatten de datasets meer dan 2.400 embryo’s voor zwangerschapsvoorspelling en meer dan 1.600 voor chromosoomstatus. In plaats van te vertrouwen op door mensen gekozen markers, analyseerde de AI de volledige videostream en legde zo de timing en het patroon van ontwikkeling frame voor frame vast.
Hoe goed de modellen presteerden
Om de betrouwbaarheid te testen trainden de onderzoekers een ensemble — tien afzonderlijke versies — van elk model en combineerden ze hun uitkomsten zodat geen enkel model de beslissing domineerde. Ze evalueerden de prestaties in drie onafhankelijke groepen: een validatieset, een interne testset en een externe testset van andere IVF-klinieken. Beide modellen toonden een goede capaciteit om embryo’s met betere uitkomsten te onderscheiden van die met slechtere. Voor zwangerschapsvoorspelling was de nauwkeurigheid het hoogst wanneer het model zich richtte op de eerste 20 tot 50 uur van ontwikkeling, wat suggereert dat zeer vroege celdelingen krachtige aanwijzingen voor later succes bevatten. Voor chromosoomstatus bleef de prestatie sterk gedurende de hele kweekperiode, wat betekent dat bruikbare signalen aanwezig zijn tijdens de vroege groei van het embryo.
Wat de scores in de kliniek kunnen betekenen
In de dagelijkse IVF-praktijk moeten artsen beslissen welke embryo’s worden overgezet of verder getest, niet alleen ze rangschikken. De onderzoekers kozen daarom praktische score-drempels met behulp van de validatiegegevens en pasten die ongewijzigd toe op de testklinieken, als nabootsing van implementatie in de echte wereld. Voor zwangerschapsvoorspelling hield de gekozen drempel de meeste embryo’s in stand die uiteindelijk tot zwangerschap leidden, terwijl veel die niet innestelden werden uitgesloten. Voor chromosoomvoorspelling behield de drempel een groot aandeel embryo’s die door testen als chromosomaal normaal werden aangemerkt en zette vele waarschijnlijk afwijkende embryo’s opzij. De auteurs benadrukken dat deze hulpmiddelen bedoeld zijn ter ondersteuning van, en niet ter vervanging van, klinisch oordeel — ze helpen bij het prioriteren van embryo’s, verminderen de behoefte aan invasieve tests wanneer die niet haalbaar zijn, en kunnen mogelijk de tijd tot een succesvolle zwangerschap verkorten.
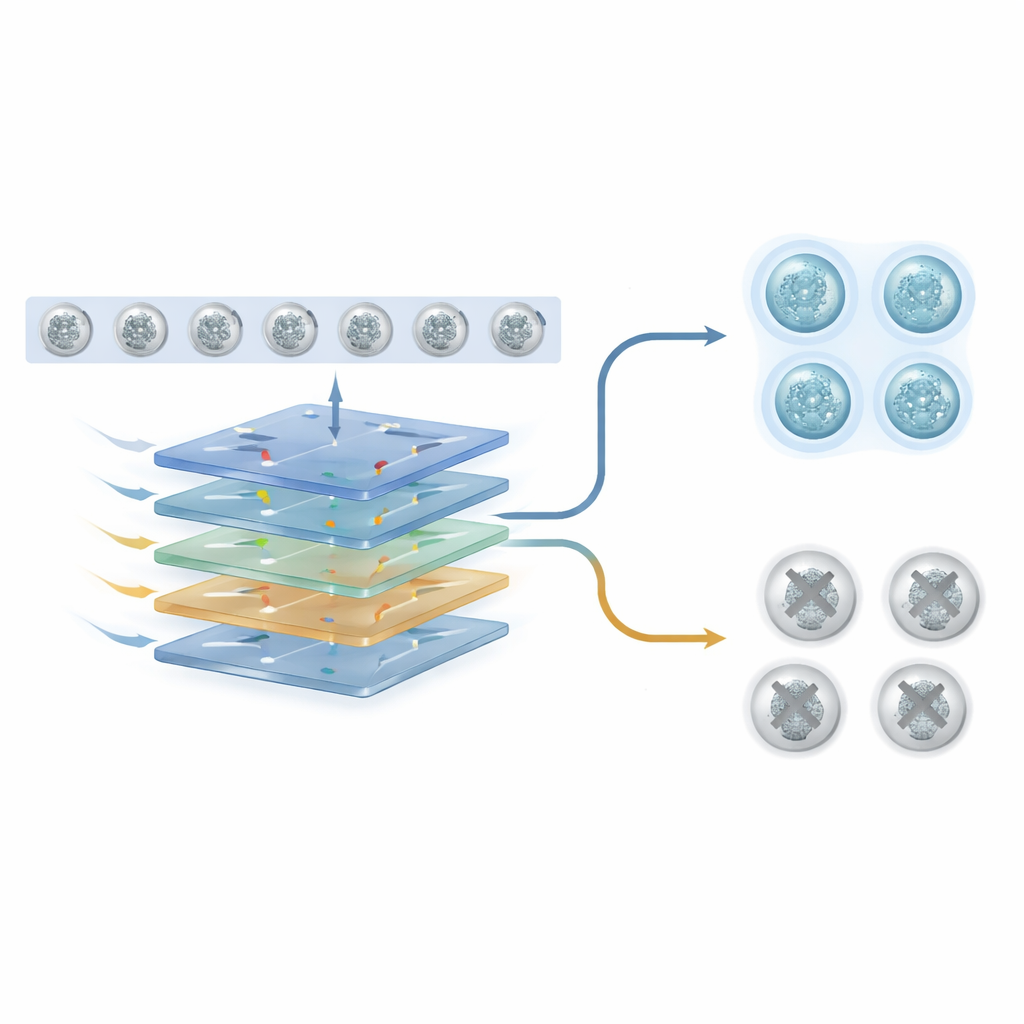
Vooruitkijken naar zachtere embryoselectie
Voor niet-specialisten is de hoofdboodschap dat computers nu van korte filmpjes van embryo’s kunnen leren om niet-invasieve aanwijzingen te geven over welke het meest veelbelovend zijn. Door te observeren hoe embryo’s vanaf het allereerste begin delen en veranderen, kan AI informatie vastleggen die menselijke ogen en eenmalige snapshots kunnen missen. Hoewel verder onderzoek in meer diverse klinieken en patiëntengroepen nodig is, wijst deze benadering richting IVF-behandelingen waarin embryo-keuze objectiever, veiliger en minder afhankelijk van biopsieën is — en zo een zachtere route naar het stichten van een gezin biedt.
Bronvermelding: Maekawa, R., Kiritani, T., Abe, T. et al. AI prediction models based on time-lapse imaging for good embryos with implantation potential and euploidy. Sci Rep 16, 9864 (2026). https://doi.org/10.1038/s41598-026-40917-5
Trefwoorden: IVF, embryoselectie, time-lapse-opnames, kunstmatige intelligentie, niet-invasieve testen