Clear Sky Science · pl
Modele predykcyjne AI oparte na obrazowaniu time-lapse dla dobrych zarodków z potencjałem implantacji i euploidii
Dlaczego to ma znaczenie dla par starających się o dziecko
Dla osób przechodzących zapłodnienie in vitro (IVF) wybór, który zarodek przetransferować, może przesądzić o różnicy między kolejnym bolesnym niepowodzeniem a udaną ciążą. Dziś decyzje często opierają się na wyglądzie zarodków pod mikroskopem lub na inwazyjnych badaniach genetycznych polegających na pobraniu komórek z zarodka. W tym badaniu zbadano inną drogę: użycie sztucznej inteligencji (AI) do obserwacji wzrostu zarodków w czasie i dyskretnego oszacowania, które z nich mają największe szanse na implantację i które najprawdopodobniej mają właściwą liczbę chromosomów — wszystko bez dotykania zarodka.
Od zdjęć do ruchomych obrazów
Tradycyjnie embriolodzy oceniają zarodki na podstawie kilku nieruchomych obrazów, oceniając cechy takie jak kształt i układ komórek. Te oceny są subiektywne i nie ujawniają wiarygodnie, czy zarodek ma prawidłową liczbę chromosomów, co jest kluczowym czynnikiem ryzyka poronienia. Testy genetyczne mogą to określić, ale wymagają usunięcia komórek z zarodka. W tej pracy badacze zamiast tego wykorzystali ciągłe filmy time-lapse rejestrowane w specjalnych inkubatorach. Filmy te pokazują subtelne zmiany w podziale komórek i rozwoju w ciągu pierwszych kilku dni po zapłodnieniu, w tym detale zbyt drobne lub zbyt szybkie, by ludzki wzrok mógł je konsekwentnie śledzić.
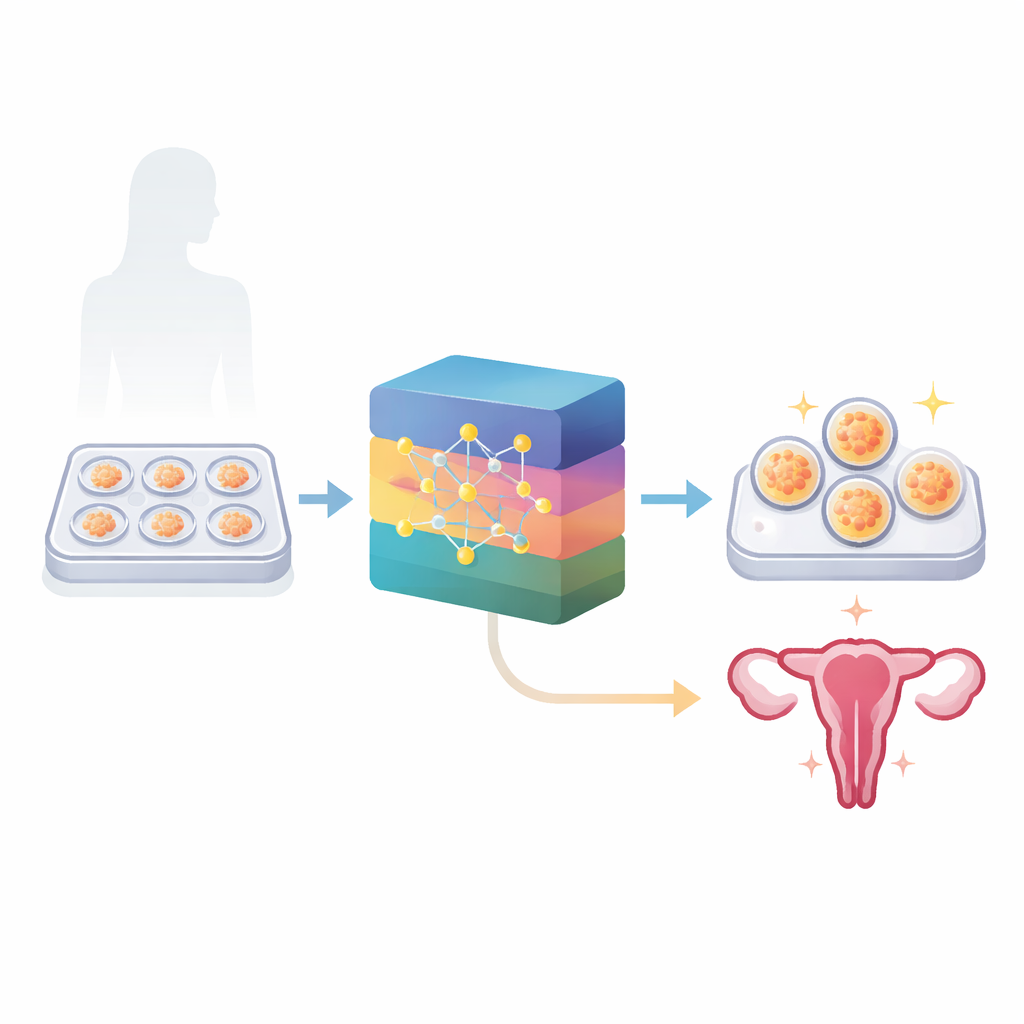
Uczenie AI rozpoznawania wczesnego życia na filmie
Zespół zbudował dwa modele AI, które uczyły się bezpośrednio z tych filmów zarodków oraz z wieku matki. Jeden model oszacowywał szansę, że przetransferowany zarodek doprowadzi do ciąży klinicznej (potwierdzonej USG). Drugi oceniał, czy zarodek prawdopodobnie jest „euploidalny”, czyli ma prawidłową liczbę chromosomów, na podstawie wyników standardowych badań genetycznych wykonanych na części zarodków. Łącznie zestawy danych obejmowały ponad 2400 zarodków do predykcji ciąży i więcej niż 1600 do oceny statusu chromosomalnego. Zamiast polegać na ręcznie wybranych przez ludzi wskaźnikach, AI analizowała cały strumień wideo, rejestrując czas i wzorce rozwoju klatka po klatce.
Jak dobrze działały modele
Aby sprawdzić niezawodność, badacze trenowali zespół—dziesięć niezależnych wersji—każdego modelu i łączyli ich wyniki, tak by żadna pojedyncza wersja nie dominowała decyzji. Oceny przeprowadzono w trzech niezależnych grupach: zestawie walidacyjnym, wewnętrznym zestawie testowym oraz zewnętrznym zestawie testowym z różnych klinik IVF. Oba modele wykazały dobrą zdolność do rozróżniania zarodków z lepszymi wynikami od tych z gorszymi. W przypadku predykcji ciąży dokładność modelu była najwyższa, gdy skupiał się na pierwszych 20–50 godzinach rozwoju, co sugeruje, że bardzo wczesne podziały komórkowe niosą silne wskazówki o późniejszym powodzeniu. W odniesieniu do statusu chromosomalnego wydajność pozostawała wysoka przez cały okres hodowli, co oznacza, że użyteczne sygnały obecne są w trakcie całego wczesnego rozwoju zarodka.
Co oceny mogą znaczyć w praktyce klinicznej
W rzeczywistej praktyce IVF lekarze muszą decydować, które zarodki przetransferować lub poddać dalszym badaniom, a nie tylko je uporządkować. Badacze wybrali więc praktyczne progi wyników, korzystając z danych walidacyjnych, i zastosowali je bez zmian w klinikach testowych, naśladując realne wdrożenie. Dla predykcji ciąży przyjęty próg zachował większość zarodków, które ostatecznie doprowadziły do ciąży, jednocześnie odrzucając wiele, które się nie zaimplantowały. W przypadku predykcji chromosomalnej próg utrzymywał dużą część zarodków, które badania wykazały jako chromosomalnie prawidłowe, i odsuwał wiele prawdopodobnie nieprawidłowych. Autorzy podkreślają, że narzędzia te mają wspierać, a nie zastępować, ocenę kliniczną — pomagając priorytetyzować zarodki, zmniejszać potrzebę inwazyjnych badań, gdy nie są one wykonalne, i potencjalnie skracać czas do osiągnięcia udanej ciąży.
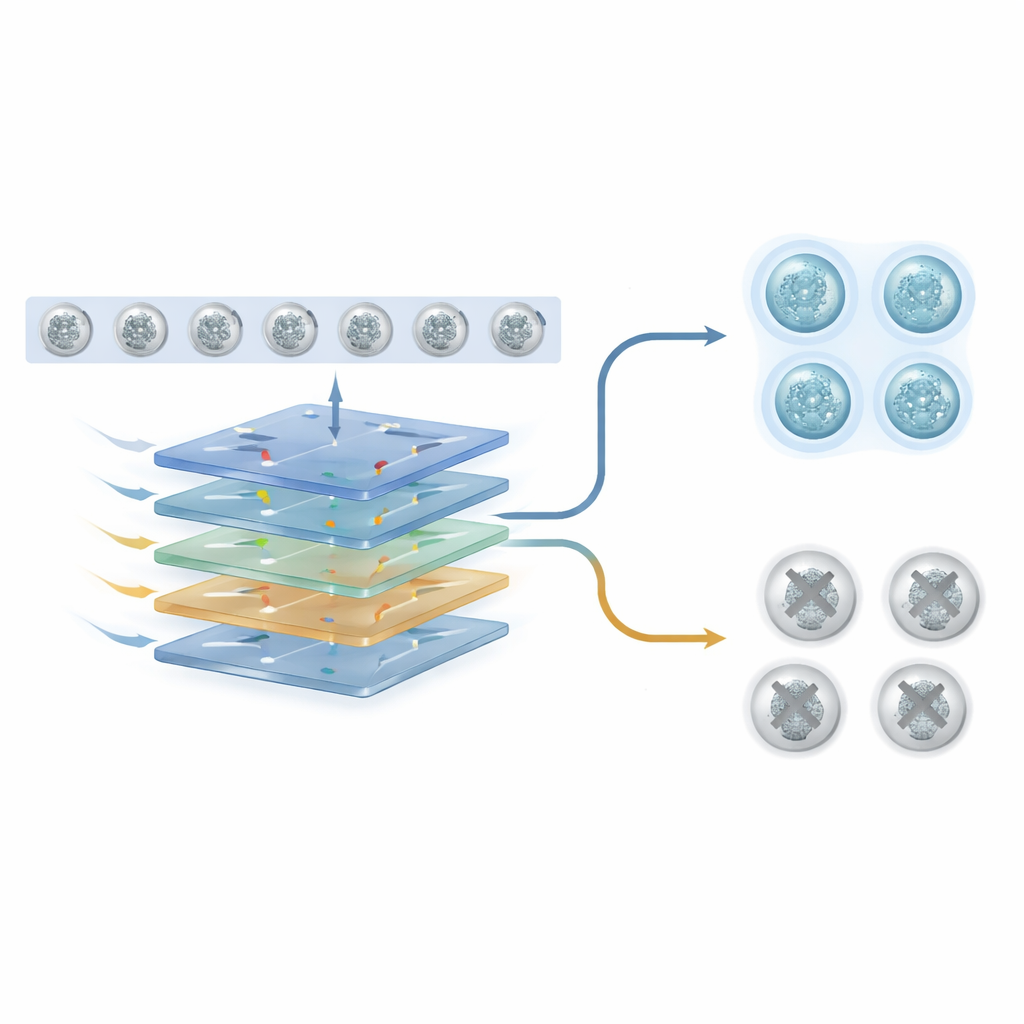
W kierunku delikatniejszej selekcji zarodków
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że komputery potrafią teraz uczyć się na podstawie krótkich filmów zarodków, by dostarczać nieinwazyjne wskazówki, które z nich są najbardziej obiecujące. Obserwując, jak zarodki dzielą się i zmieniają od samego początku, AI może wychwycić informacje, które umknęłyby ludzkim oczom i pojedynczym migawkom. Choć potrzebne są dalsze testy w bardziej zróżnicowanych klinikach i grupach pacjentów, to podejście wskazuje kierunek ku procedurom IVF, w których wybór zarodka będzie bardziej obiektywny, bezpieczniejszy i mniej zależny od biopsji — oferując łagodniejszą drogę do założenia rodziny.
Cytowanie: Maekawa, R., Kiritani, T., Abe, T. et al. AI prediction models based on time-lapse imaging for good embryos with implantation potential and euploidy. Sci Rep 16, 9864 (2026). https://doi.org/10.1038/s41598-026-40917-5
Słowa kluczowe: IVF, selekcja zarodków, obrazowanie time-lapse, sztuczna inteligencja, testy nieinwazyjne