Clear Sky Science · sv
Kväveoxid inducerar p53-medierad celldöd i mänskliga nässlemhinneceller
Varför näsans första försvarslinje spelar roll
Dina näsgångar är mer än bara luftkanaler; de utgör en levande sköld som hjälper till att hålla virus, bakterier och föroreningar borta från kroppen och hjärnan. Vid infektioner och kronisk inflammation badar denna sköld i kemiska signaler som bekämpar mikrober men som också kan skada våra egna celler. En sådan molekyl, kväveoxid, är både en välkänd försvarare och stökmakare. Denna studie ställer en enkel men viktig fråga: när kväveoxid dröjer kvar i höga nivåer runt nässlemhinnan, försvagar den då tyst denna första försvarslinje?
En hjälpsam gas med en mörk sida
Kväveoxid är en liten gasmolekyl som våra kroppar använder för att vidga blodkärl, underlätta nervsignalering och stärka immunsvaret. Immunceller släpper ut korta utbrott av den för att hjälpa till att döda invaderande mikrober, och i normala mängder stödjer den hälsosam funktion. Men vid kraftiga eller långvariga immunsvar kan kväveoxid bildas i överskott och reagera med syre för att bilda mycket reaktiva kemiska arter. Dessa kan skada DNA och andra viktiga cellulära komponenter och förvandla ett hjälpsamt vapen till en källa till kollaterala skador. Eftersom nässlemhinnan är direkt utsatt mot omvärlden och är en viktig ingångsport för luftvägsvirus som SARS-CoV-2, är det avgörande att förstå hur långvarig exponering för kväveoxid påverkar dessa celler.
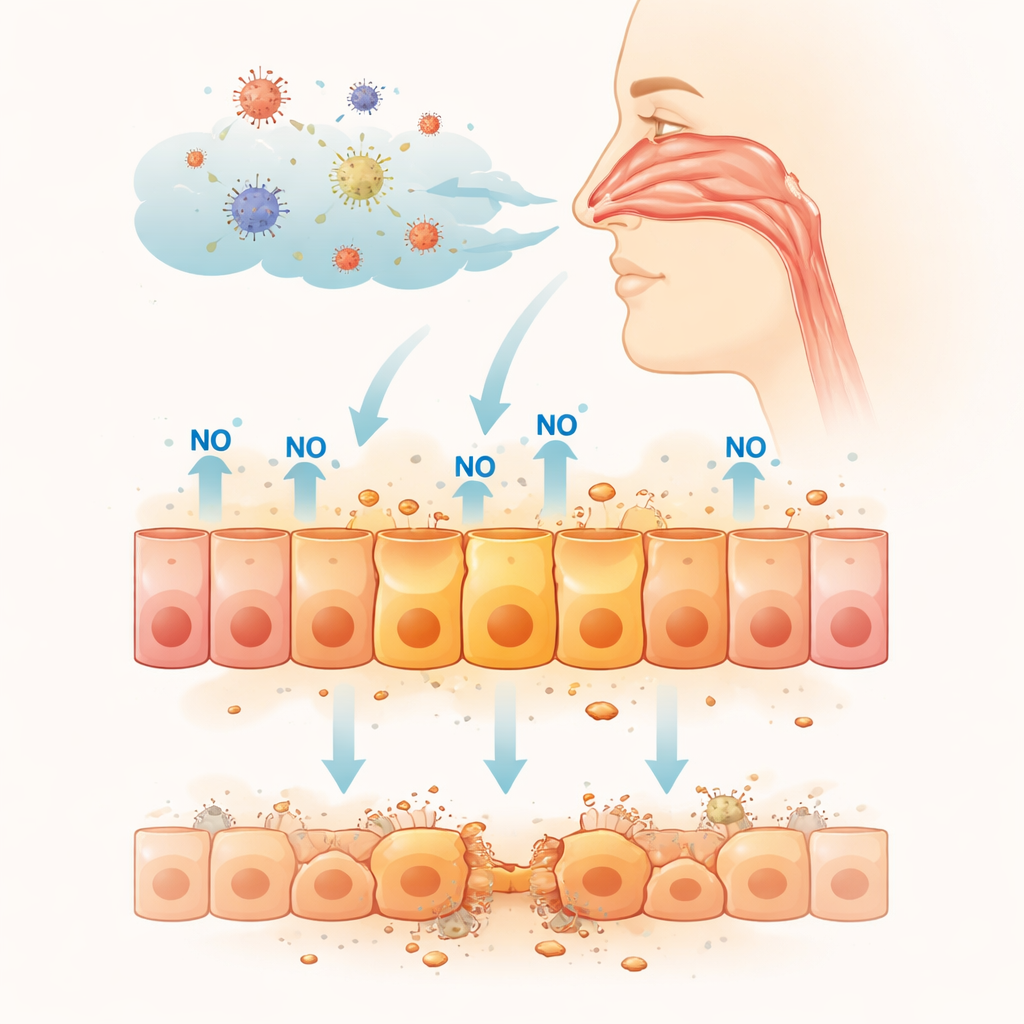
Test av långtidsexponering i näsceller
För att undersöka detta använde forskarna en mänsklig cellinje från nässlemhinna odlad i laboratoriet, ett vanligt använt substitut för nässkyddet. De utsatte dessa celler i upp till tre dagar för en kväveoxidfrigörande förening i nivåer liknande dem som rapporterats i inflammerad vävnad. Med tiden bromsade celltillväxten upp och fler celler dog, vilket tyder på att långvarig kväveoxid är toxisk för denna näsmodell. För att ta reda på vad som hände inne i cellerna analyserade teamet vilka gener som skrevs på eller av efter 48 timmars exponering. Hundratals gener ändrade sin aktivitet, och många av de starkast aktiverade var kopplade till ett centralt cellulärt vakthundsprotein kallat p53, som övervakar DNA-skador och styr om celler reparerar sig, slutar dela sig eller självdör.
Hur cellens väktare vänder sig mot skadade celler
Uppföljande experiment bekräftade att kväveoxid får p53-protein att ackumuleras i näsceller redan inom några timmar, vilket är ett kännetecken för dess aktivering. När p53-nivåerna steg ökade också aktiviteten hos flera av dess målgener som drar celler mot programmerad celldöd och stoppar cellcykeln. Markörer för apoptos, det ordnade självdödsprogrammet som bryter ner celler i små, lättavfallade fragment, ökade över tid. När forskarna använde ett läkemedel som specifikt blockerar p53:s förmåga att kontrollera gener minskade både ökningen av p53-målgener och mängden celldöd betydligt. Det visade att p53 är en huvuddrivkraft bakom kväveoxidinducerad förlust av nässlemhinneceller, även om andra vägar sannolikt också bidrar.
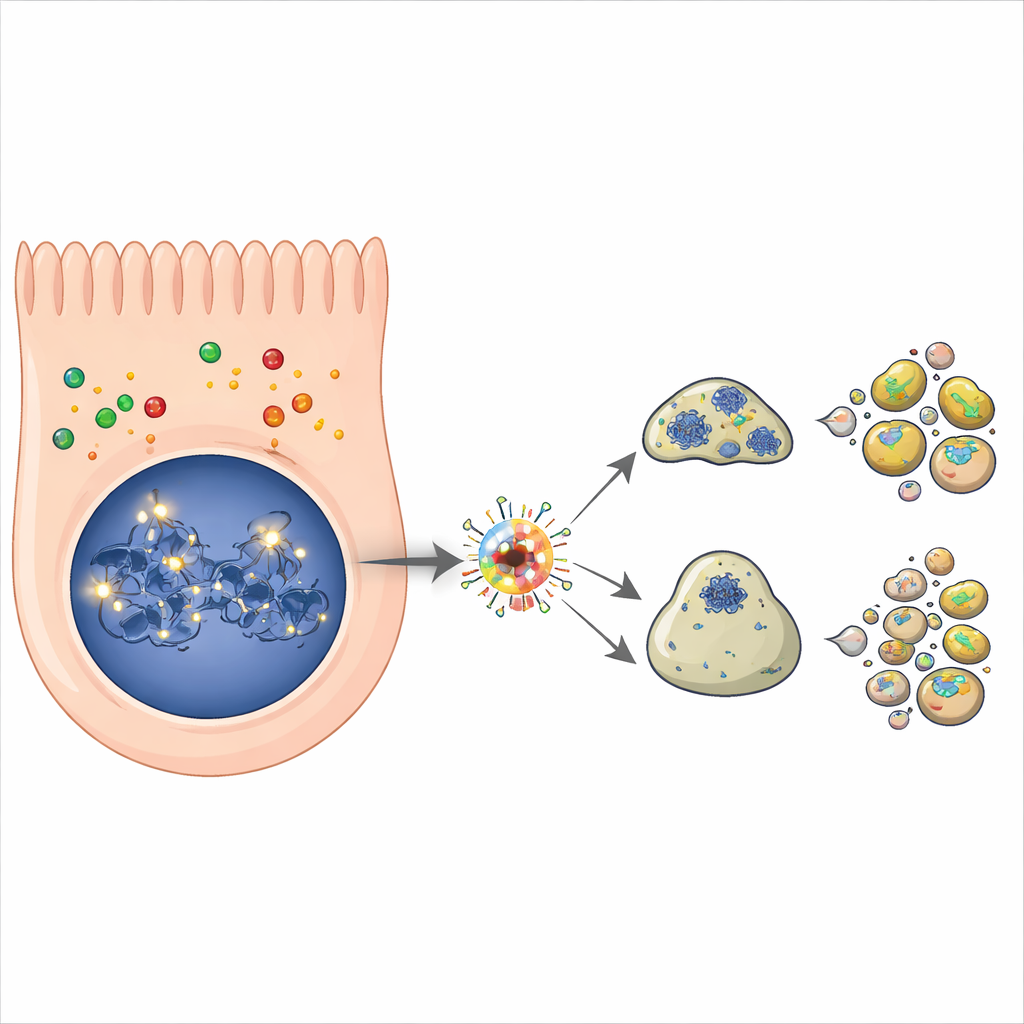
Kopplingar till inflammation, luktförlust och kronisk sjukdom
Resultaten passar in i en större bild där kväveoxid och p53 tillsammans formar hur vävnader svarar på stress och inflammation. Vid tillstånd som COVID-19 är näsinflammation och kväveoxidproducerande enzymer förhöjda, och p53-aktivitet tros öka under intensiva immunsvar. Studien föreslår en plausibel händelsekedja: under en inflammatorisk topp kan långvarig kväveoxid skada DNA i näsceller, aktivera p53 och utlösa deras död. Med tiden kan detta tunna ut eller störa nässlemhinnan, vilket gör det lättare för virus, föroreningar och inflammatoriska signaler att tränga djupare in i luftvägarna eller till och med nå hjärnan. Sådana skador kan bidra till långvariga problem som bestående luktförlust eller kronisk nasal och luftvägssjukdom.
Vad detta betyder för att skydda nässkyddet
Enkelt uttryckt visar studien att när kväveoxid dröjer kvar på höga nivåer kan den få nässlemhinnans celler att aktivera sin interna ”självdestruktions”-knapp via p53, vilket minskar cellantalet och potentiellt försvagar barriären inne i näsan. Även om arbetet utfördes i ett förenklat cellsystem och inte i levande människor understryker det att kroppens egna försvarskemikalier måste vara noggrant balanserade. För lite kväveoxid kan försämra immunförsvaret, men för mycket under för lång tid kan erodera de vävnader som skyddar oss. En bättre förståelse av denna balans kan så småningom informera strategier för att bevara nässlemhinnans hälsa vid svåra infektioner och kronisk inflammation.
Citering: Kamiuezono, S., Kubota, S., Tsuchida, T. et al. Nitric oxide induces p53-mediated cell death in human nasal epithelial cells. Sci Rep 16, 10055 (2026). https://doi.org/10.1038/s41598-026-40908-6
Nyckelord: kväveoxid, nasslemhinna, p53, apoptos, inflammation